
14£ÆpH=2µƒ¡Ω÷÷“ª‘™À·HX∫ÕHYµƒ»Ð“∫∑÷±»°50mL£¨º”»Îπ˝¡øµƒ√æ∑€£¨≥‰∑÷∑¥”¶∫Û£¨ ’ºØH2µƒÃª˝‘⁄œýÕ¨◊¥øˆœ¬∑÷±Œ™V1∫ÕV2£¨»ÙV1>V2£¨œ¬¡–Àµ∑®’˝»∑µƒ «
A£ÆHX“ª∂® «»ıÀ· °°°°°°°°°°°°°°°°B£ÆNaXÀƻГ∫µƒºÓ–‘»ı”⁄NaYÀƻГ∫µƒºÓ–‘
C£ÆHX“ª∂® ««øÀ·°°°°°°°°°° °°°°°°D£Æ∑¥”¶ø™ º ±∂˛’þ…˙≥…H2µƒÀŸ¬ œýÕ¨
13£Æ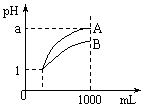 “Œ¬œ¬£¨pH=1µƒ¡Ω÷÷À·»Ð“∫A°¢B∏˜1 mL£¨∑÷±º”ÀÆœ° ÕµΩ1000mL£¨∆‰pH÷µ”λГ∫ê˝µƒπÿœµ»ÁÕº£¨œ¬¡–Àµ∑®’˝»∑µƒ «
“Œ¬œ¬£¨pH=1µƒ¡Ω÷÷À·»Ð“∫A°¢B∏˜1 mL£¨∑÷±º”ÀÆœ° ÕµΩ1000mL£¨∆‰pH÷µ”λГ∫ê˝µƒπÿœµ»ÁÕº£¨œ¬¡–Àµ∑®’˝»∑µƒ «
A£ÆA°¢B¡Ω÷÷À·»Ð“∫µƒŒÔ÷ µƒ¡ø≈®∂»“ª∂®œýµ»
B£Æœ° Õ∫Û£¨AÀ·»Ð“∫µƒÀ·–‘±»BÀ·»Ð“∫«ø£ª
°°°° C£Æ»Ùa = 4£¨‘ÚA ««øÀ·£¨B «»ıÀ·£ª
°°°° D£Æœ° Õ∫Û£¨aø…ƒÐ¥Û”⁄4°£
12£Æ°∞À·ºÓ÷ ◊”¿Ì¬€°±»œŒ™∑≤ «ƒÐπª∏¯≥ˆ÷ ◊”(H+)µƒ∑÷◊”ªÚ¿Î◊”∂º «À·£¨∑≤ «ƒÐπªΩ” Ð÷ ◊”µƒ∑÷◊”ªÚ¿Î◊”∂º «ºÓ£¨ŒÔ÷ À·–‘(ºÓ–‘)µƒ«ø»ı»°æˆ”⁄∑÷◊”ªÚ¿Î◊”∏¯≥ˆ(Ω” Ð)÷ ◊”ƒÐ¡¶µƒ¥Û–°°£∞¥’’°∞À·ºÓ÷ ◊”¿Ì¬€°±£¨œ¬¡–Àµ∑®’˝»∑µƒ «
A£ÆHCO3£≠ º» «À·”÷ «ºÓ£¨NH3º»≤ª «À·”÷≤ª «ºÓ
B£ÆClO£≠+H2O HClO+OH£≠ «À·ºÓ∑¥”¶
HClO+OH£≠ «À·ºÓ∑¥”¶
C£Æ2Na+2H2O = 2NaOH+H2°¸ «À·ºÓ∑¥”¶
D£ÆºÓ–‘«ø»ıÀ≥–ÚŒ™£∫C2H5O£≠ > OH£≠ > C6H5O£≠
11£ÆΩ´pH=3µƒ—ŒÀ·aL∑÷±”Îœ¬¡–»˝÷÷»Ð“∫ªÏ∫œ∫Û£¨»Ð“∫æ˘≥ ÷––‘£∫
¢Ÿ°°°° 1°¡10-3mol/L µƒ∞±ÀÆbL°°°°°°°° °°°°°°°°°°¢⁄c(OH-)=1°¡10-3mol/L µƒ∞±ÀÆcL
¢€°°°° c(OH-)=1°¡10-3mol/L µƒBa(OH)2»Ð“∫dL
∆‰÷–a°¢b°¢c°¢dµƒπÿœµ’˝»∑µƒ «
A£Æb£æa£æd£æc °°°°°°°°°°°°°°°°°°°°°° B£Æb£æa=d£æc°°°°°° °° C£Æa=b£æc£æd°° °°°° D£Æc£æa=d£æb
10£Æ≥£Œ¬œ¬“—÷™¡Ω÷÷“ª‘™»ıÀ·HX∫ÕHY£¨»Áπ˚œÚNaX»Ð“∫÷–Õ®CO2 ∆¯Ã£¨÷ªƒÐ…˙≥…HX∫ÕNaHCO3£ªÕ˘NaY»Ð“∫÷–Õ®»ÎCO2‘Ú…˙≥…HY∫ÕNa2CO3°£”–πÿ– ˆ’˝»∑µƒ «
A£ÆÀ·–‘”…«ø÷¡»ı£∫HX>HY>H2CO3
B£ÆΩ·∫œH+µƒƒÐ¡¶£∫Y®D>CO32®D>X®D>HCO3®D
C£Æ»Ð“∫ŒÔ÷ µƒ¡ø≈®∂»œýÕ¨ ±ºÓ–‘£∫NaX>Na2CO3>NaY>NaHCO3
D£ÆNaX»Ð“∫÷–Õ®»Î◊„¡øCO2∫Ûµƒ¿Î◊”≈®∂»£∫c(X®D)£æc(Na+)£æc(HCO3®D)£æc(OH®D)
9£Æœ¬¡– µ—È≤ªƒÐ¥ÔµΩ‘§∆⁄ƒøµƒµƒ «
|
–Ú∫≈ |
µ—È≤Ÿ◊˜ |
µ—ȃøµƒ |
|
A |
Cl2°¢Br2∑÷±”ÎH2∑¥”¶ |
±»Ωœ¬»°¢‰Âµƒ∑«Ω Ù–‘«ø»ı |
|
B |
MgCl2°¢AlCl3»Ð“∫÷–∑÷±Õ®»ÎNH3 |
±»Ωœ√æ°¢¬¡µƒΩ Ù–‘«ø»ı |
|
C |
≤‚∂®Õ¨≈®∂»Na2CO3°¢Na2SO4¡Ω»Ð“∫µƒpH |
±»ΩœÃº°¢¡Úµƒ∑«Ω Ù–‘«ø»ı |
|
D |
”√Õ¨“ªµÁ¬∑≤‚∂®µ»≈®∂»µƒ—ŒÀ·°¢¥◊À·¡Ω»Ð“∫µƒµºµÁ–‘ |
±»Ωœ—ŒÀ·°¢¥◊À·µƒÀ·–‘«ø»ı |
8£Æº◊À·∫Õ““À·∂º «»ıÀ·£¨µ±À¸√«µƒ≈®∂»æ˘Œ™0.10mol/L ±£¨º◊À·÷–µƒc(H+)‘ºŒ™““À·÷–c(H+)µƒ3±∂°£œ÷”–¡Ω÷÷≈®∂»≤ªµ»µƒº◊À·»Ð“∫a∫Õb£¨“‘º∞0.10mol/Lµƒ““À·£¨æ≠≤‚∂®À¸√«µƒpH¥”¥ÛµΩ–°“¿¥ŒŒ™a°¢““À·°¢b°£”…¥Àø…÷™
A£Æaµƒ≈®∂»±ÿ–°”⁄““À·µƒ≈®∂»°°°° °°°°°°°°°°B£Æaµƒ≈®∂»±ÿ¥Û”⁄““À·µƒ≈®∂»
C£Æbµƒ≈®∂»±ÿ–°”⁄““À·µƒ≈®∂»°°°° °°°°°°°°°°D£Æbµƒ≈®∂»±ÿ¥Û”⁄““À·µƒ≈®∂»
7£Æ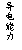
 “ª∂®Œ¬∂»œ¬£¨Ω´“ª∂®÷ ¡øµƒ±˘¥◊À·º”ÀÆœ° Õπ˝≥Ã÷–£¨»Ð“∫µƒµºµÁƒÐ¡¶±‰ªØ»Á”“ÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «
“ª∂®Œ¬∂»œ¬£¨Ω´“ª∂®÷ ¡øµƒ±˘¥◊À·º”ÀÆœ° Õπ˝≥Ã÷–£¨»Ð“∫µƒµºµÁƒÐ¡¶±‰ªØ»Á”“ÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «
A£Æa°¢b°¢c»˝µ„»Ð“∫µƒpH£∫c£ºa£ºb
B£Æa°¢b°¢c»˝µ„¥◊À·µƒµÁ¿Î≥Ã∂»£∫a£ºb£ºc
C£Æ”√ ™»ÛµƒpH ‘÷Ω≤‚¡øa¥¶»Ð“∫µƒpH£¨≤‚¡øΩ·π˚∆´–°
D£Æa°¢b°¢c»˝µ„»Ð“∫”√1mol/L«‚—ıªØƒ∆»Ð“∫÷–∫Õ£¨œ˚∫ƒ«‚—ıªØƒ∆»Ð“∫ê˝£∫c£ºa£ºb
6£Æ“—÷™0.1 mol/Lµƒ¥◊À·»Ð“∫÷–¥Ê‘⁄µÁ¿Î∆Ω∫‚£∫CH3COOH CH3COO£≠+H+£¨“™ π»Ð“∫÷–c(H+)/c(CH3COOH)÷µ‘ˆ¥Û£¨ø…“‘≤…»°µƒ¥Î © «
CH3COO£≠+H+£¨“™ π»Ð“∫÷–c(H+)/c(CH3COOH)÷µ‘ˆ¥Û£¨ø…“‘≤…»°µƒ¥Î © «
A £Æº”…Ÿ¡ø…’ºÓ»Ð“∫°°°° °° B £Æ…˝∏þŒ¬∂»°° °°°°°°°°°°°°°° C £Æº”…Ÿ¡ø±˘¥◊À·°°°°°° °°°°°°°°°°°°°° D £Æº”ÀÆ
5£Æ∂‘∞±ÀƻГ∫÷–¥Ê‘⁄µƒµÁ¿Î∆Ω∫‚NH3°§H2O NH4++OH£≠∑÷Œˆ£¨œ¬¡–– ˆ’˝»∑µƒ «
NH4++OH£≠∑÷Œˆ£¨œ¬¡–– ˆ’˝»∑µƒ «
A£Æº”ÀÆ∫Û£¨»Ð“∫÷–n(OH®C)‘ˆ¥Û
B£Æº”»Î…Ÿ¡ø≈®—ŒÀ·£¨»Ð“∫÷–n(OH®C)‘ˆ¥Û
C£Æº”»Î…Ÿ¡ø≈®NaOH»Ð“∫£¨µÁ¿Î∆Ω∫‚œÚ’˝∑¥”¶∑ΩœÚ“∆∂Ø
D£Æº”»Î…Ÿ¡øNH4ClπÃ㨻Г∫÷–c(NH4+)ºı…Ÿ
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com