
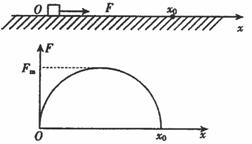
17.静置于光滑水平面上坐标原点处的小物块,在水平拉力F作用下,沿x轴方向运动,拉力F随物块所在位置坐标x的变化关系如图所示,图线为半圆.则小物块运动到x0处时的动能为 ( )
A.0 B.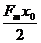 C.
C.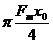 D.
D.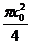
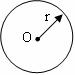
16.如图所示,在宇航员的训练中有一个圆柱形飞船,它的横截面半径为r,使这飞船绕中心轴O自转,从而给飞船内的物体提供了“人工重力”.若飞船绕中心轴O自转的角速度为ω,那么“人工重力”中的“重力加速度g”的值与离开转轴O的距离L的关系是(其中k为比例系数) ( )
A.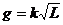 B.g=kL C.g=k/L D.
B.g=kL C.g=k/L D.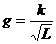
15.一物体做匀加速直线运动,依次通过A、B、C三点,AB=BC.物体在AB段加速度为a1,在BC段加速度为a2,且物体在B点的速度为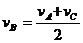 ,则
( )
,则
( )
A.a1> a2 B.a1= a2 C.a1< a2 D.不能确定
14.关于惯性,下述说法是正确的 ( )
A.惯性即是指物体原来静止的总有保持静止,原来运动的总有保持匀速运动的性质
B.静止的火车启动时速度变化缓慢,是因为物体静止时惯性大
C.乒乓球可快速抽杀,是因为乒乓球的惯性小的缘故
D.在宇宙飞船内不存在惯性
13.W g铜投入一定量浓HNO3中,铜完全溶解,共收集到672mL气体(已转化为标准状况)。将盛有此气体的容器倒扣在水中,通入标准状况下224mL的O2恰好使气体完全溶解于水中,则参加反应的硝酸的物质的量为 ( )
A.0.07mol B.0.12 mol C.0.06 mol D.无法计算
12.已知:常温下醋酸铵溶液pH=7。 现有常温下的四组溶液,分别由等体积的两种溶液混合而成:
① pH=2的醋酸 与 pH=12的氢氧化钠溶液
② 10-2 mol /L的醋酸 与10-2 mol /L的氢氧化钠溶液
③ pH=2的盐酸 与 pH=12的氨水
④ 10-2 mol /L的盐酸 与 10-2 mol /L的氨水
下列有关叙述正确的是 ( )
A.pH:④<①<②<③
B.溶液中H2O的电离程度:①=③>②=④
C.在①、②中均存在关系: c (Na+) = c(CH3COO-) + c (CH3COOH )
D.在③、④中均存在关系: c (NH4+) + c (H+)= c(OH-)+ c(Cl-)
11.已知反应:2A(g) 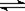 2B(g)+D (?) ;△H< 0 。在一定温度下,将1molA充入恒容密闭容器中充分反应达平衡,以下说法正确的是 ( )
2B(g)+D (?) ;△H< 0 。在一定温度下,将1molA充入恒容密闭容器中充分反应达平衡,以下说法正确的是 ( )
A.升高温度,逆反应速率增大,正反应速率减小,平衡逆向移动。
B.降低温度,当混合气体的平均分子量不变时,说明该反应已达平衡。
C.若D为气体,再加入1mol A,平衡正向移动,A的转化率增大。
D.若D为固体,再加入1mol A,平衡不移动,A在混合气体中的百分含量不变。
10.常温下,下列各组离子在指定溶液中一定能大量共存的是 ( )
①无色溶液中:K+,Cl-,Ca2+, SO42-
②pH=11的溶液中: Na+, NO3-,S2-,SO32-
③水电离的H+ 浓度等于10-12 mol·L-1的溶液中: K+,I-,NO3-,SO32-
④加入Mg生成H2的溶液中:Fe3+ ,NH4+ ,SO42- , NO3-
⑤中性溶液中:Fe3+, NO3-,Cl-,S2-
A.②③④ B.④ C.② D.③④⑤
9.下列反应的离子方程式书写正确的是 ( )
A.将氢碘酸加到Fe(OH)3胶体中:Fe (OH)3 +3H+=Fe3++3H2O
B.碳酸氢钙溶液中加入少量烧碱:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C. 0.03 mol氯气通入100mL 0. 2 mol·L-1的溴化亚铁溶液:
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
D.电解MgCl2溶液:2H++ 2Cl-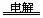 H2↑+ Cl2↑
H2↑+ Cl2↑
8.以下关于物质结构和性质的说法正确的是 ( )
A.因为SiO2相对分子质量大于CO2 ,所以SiO2的熔点高于CO2 。
B.SO3和PCl5都是非极性分子,分子中各原子最外层电子数都为8。
C.由于C60是由分子构成的,所以熔沸点较低。
D.He的构成微粒是原子,原子间的相互作用是共价键。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com