
20.(9分)以下是分析实验室对中草药中可能的残余有毒元素砷(As)的检验方法和步骤(As在中草药中主要以As 2O3的形式存在):
①取1000g中草药样品进行前期处理制得待测溶液,此时样品中可能含有的As 元素将转化为H 3AsO3;
②将待测溶液转移入250 mL锥形瓶中,并加入2-3滴0.2%的 X溶液;
③用标准碘溶液滴定待测溶液至终点,消耗21.40mL标准碘溶液,发生的反应是
请回答下列问题:
(1)0.2%X溶液名称是 ▲ ,滴定到终点时锥形瓶中产生的现象是 ▲
(2)题中所用标准碘溶液并非将碘单质直接溶解于蒸馏水中制得,而是由0.1000g纯KIO3和过量的KI以及酸混合,并将其准确稀释到1000 ml而制得,请用离子方程式说明标准碘溶液的形成: ▲
(3)我国《药用植物及制剂进出口绿色行业标准》中限定:绿色中药的砷含量不超过2.000 mg/kg,试通过计算说明该中草药样品是否合格?
19.(10分)某研究性学习小组在用 CO还原 FeO的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不同、受热不均匀时会生成Fe3O4,也能被磁铁吸引。为探究X的组成,他们进行了如下实验。
Ⅰ.定性检验
|
实验编号 |
实验操作 |
实验现象 |
|
① |
取少量黑色粉末X放入试管1中,注入足量 浓盐酸,微热 |
黑色粉末逐渐溶解,溶液Y呈 黄绿色;有少量气泡产生 |
|
② |
向试管1中滴加几滴KSCN溶液,振荡 |
溶液出现血红色 |
|
③ |
另取少量黑色粉末X放入试管2中.注入足量 硫酸铜溶液,振荡,静置 |
有极少量红色物质析出,仍 有较多黑色固体未溶解 |
(1)实验②的目的是 ▲ ;(2)由上述实验现象推断,黑色粉末X的成分是 ▲ (填化学式)。
Ⅱ.定量测定
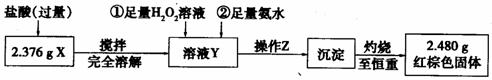
(1)操作Z是 ▲ 。下列仪器中,在灼烧沉淀时必须用到的是 ▲ ;(填名称)。

(2)通过以上数据,得出 2.376 g黑色粉末 X中各成分的物质的量为 ▲ 。
18.(6分)甲基橙和酚酞在水中和有机溶剂中的溶解度不同,当溶剂沿滤纸流经混合物点
样时,甲基橙和酚酞会以不同的速率在滤纸上移动,从而达到分离的目的。某校化学兴趣小组拟通过该原理将甲基橙和酚酞从混合溶液A中分离开来,实验装置及步骤如下:
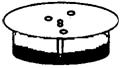 步骤1 把 0.1g甲基橙和 0.1g酚酞溶解在 10 mL 60%的乙醇溶液里,配制混合溶液A另将 10 mL乙醇和4 mL浓氨水充分混合,配成混合溶液B;
步骤1 把 0.1g甲基橙和 0.1g酚酞溶解在 10 mL 60%的乙醇溶液里,配制混合溶液A另将 10 mL乙醇和4 mL浓氨水充分混合,配成混合溶液B;
步骤2 在一张圆形滤纸中心扎一小孔,将滤纸芯插入滤纸中央(如
图).在距滤纸中心约 1cm的圆周上,选择三个点,分别用毛细管将A溶液在该三点处点样;
步骤3 将滤纸覆盖在盛有B溶液的培养皿上,使滤纸芯与溶液接触,放置一段时间,点样逐渐向外扩散,形成黄环;
步骤4 待黄环半径扩散到滤纸半径的二分之一时,取下滤纸,等滤纸稍干后,喷上饱和Na2 CO3 溶液,通过现象判断分离的效果.
试回答下列问题:
(1)本实验采用的分离方法叫 ▲ ,若分离淀粉胶体与氯化钠的混合液
则可选用 ▲ 法。
(2)步骤2中若在滤纸上事先作点样位置标记,宜选用 ▲ 笔(填“钢”或“铅”)
(3)步骤4中喷洒Na2 CO3溶液后,能观察到的现象是 ▲ ,这说明实验中酚酞在滤纸上移动速率更快。酚酞与甲基橙相比,酚酞的 ▲ 强(填“亲水性”或“亲脂性”)。
(4)它们可以通过 ▲ 来判断分离的效果。
17.(13分)A-J均为中学化学中的常见物质,它们之间的转化关系如下图所示(有的转变中省略部分生成物)。已知A为单质,A、C、H、I、J 含有同一种元素,B、D、E、F、G含有同一种元素。化合物X、Y均可由氯碱工业制得;将X、Y分别溶于水所得溶液中的阳离子都是10电子的粒子。
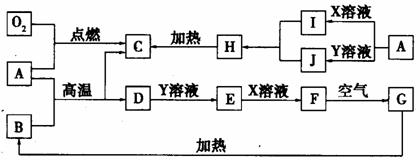
请回答下列问题:
(l)Y 是 ▲ (填‘“极性”或“非极性”)分子;X 的电子式 ▲ ;
C的晶体类型是 ▲ ;D 的化学式是 ▲ 。
(2)A→I的离子方程式是 ▲ ;
F→G的化学方程式是 ▲ 。
(3)A 和B高温下发生置换反应的化学方程式是 ▲ 。
请再写出满足下列两个条件的3个置换反应的化学方程式:
①所涉及的元素的原子序数都小于18
②3个置换反应中6种单质的组成元素分别属于6个不同的主族
▲ ; ▲ ; ▲ 。
16.(12分)关于芳香族化合物A的有关信息如下:
①A 中碳的质量分数为77.77%,氢的质量分数为7.40%,其余为氧;
②光谱法测定时波谱图反映出A的相对分子质量为108;
③A可以与乙酸在浓硫酸加热条件下生成有水果香味的产物;
④A可以与金属钠反应放出氢气,但不能与氢氧化钠反应; 试回答:
(1)测A的相对分子质量的光谱为 ▲ (填代号)。A物质苯环上的一溴代物有 ▲ 种。
A.红外光谱 B.质谱 C.核磁共振谱
(2)A通常有三种不同类别的芳香族同分异构体,试写出另两种不同类别的异构体的结
构简式(各写一种): ▲ ; ▲ ;
(3)A与乙酸反应的化学方程式为 ▲ ;
(4)已知灼热的铜丝伸入装有液体A的试管中,反复几次会闻到一种刺激气味,反应的化学方程式为 ▲ 。
0.09 mol·L-1,当反应到8min时,反应到达平衡,此时三氧
化硫浓度c(SO3)= a mol·L-1。
(1)0min-4min内生成O2平均速率
v(O2)= ▲ mol·L-1·min-1
(2)达到平衡时c(O2)=c(SO2),则a= ▲ mol·L-1,在下列
坐标系中作出0min-8min及之后SO2、O2、SO3浓度随时
间变化曲线。
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于a mol·L-1的是 ▲
|
|
A |
B |
C |
D |
|
SO3 |
1mol |
3mol |
3mol |
0mol |
|
SO2 |
2mol |
1.5mol |
0mol |
6mol |
|
O2 |
2mol |
1mol |
0mol |
5mol |
15.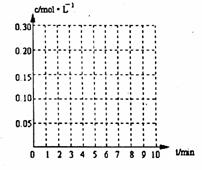 (8分)在20L恒容的密闭容器中,加入3mo1SO3(g)和lmo1氧气,
(8分)在20L恒容的密闭容器中,加入3mo1SO3(g)和lmo1氧气,
在一定温度下使其反应,反应至4min时,氧气的浓度为
14.有机物甲是一种包含有一个六元环结构的化合物,其分子式为C7H12O2,在酸性条件下可以发生水解,且水解产物只有一种。又知甲的分子中含有两个甲基,则甲的可能结构有
A.6种 B.8种 C.10种 D.14种
第Ⅱ卷(共58分)
13.无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2、HCl中的几种,将 100 mL气体甲经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成为
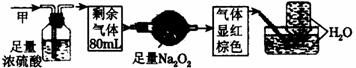
A.NH3、NO2、N2 B.NH3、NO、CO2
C.NH3、NO2、CO2 D. NO、CO2、N2
12.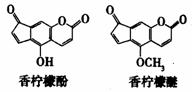 香柠檬油可用于化妆品。香柠檬油含微量的香柠檬酚和
香柠檬油可用于化妆品。香柠檬油含微量的香柠檬酚和
香柠檬醚,其结构如右图。下列说法正确的是
A.香柠檬醚的分子式为C13H6O4
B.lmol香柠檬酚最多可与2molBr2发生反应
C.香柠檬酸通过取代反应可转化成香柠檬醚
D.l mol香柠檬酚在NaOH溶液中水解时能消耗2molNaOH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com