
2.一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ(Q>0),经测定完全吸收生成的二氧化碳需消耗5mol·L-1的KOH溶液100ml,恰好完全反应,则此条件下反应: C4H10(g)+13/2O2(g)== 4 CO2 (g)+ 5 H2O(g)的△H为
A.
+8Q kJ/mol B. 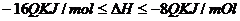
C. -8Q kJ /mol D. -16Q KJ/mol
1.一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ(Q>0),经测定完全吸收生成的二氧化碳需消耗5mol·L-1的KOH溶液100ml,恰好生成正盐,则此条件下反应: C4H10(g)+13/2O2(g)== 4 CO2 (g)+ 5 H2O(g)的△H为
A. +8Q kJ/mol B. +16Q kJ/mol C. -8Q kJ /mol D. -16Q kJ/mol
3.科学家发现,不管化学反应是一步完成或分几步完成,该反应的热效应是相同的。已知在25℃,105Pa时,石墨、一氧化碳的燃烧热分别是393.5 kJ·mol-1和283.0 kJ·mol-1,下列说法或方程式正确的是
A.在相同条件下:2C(石墨)+O2(g)=2CO(g);ΔH=-110.5 kJ·mol-1
B.1 mol石墨不完全燃烧,生成CO2和CO混合气体时,放热504.0 kJ
C.在相同条件下:C(石墨)+CO2(g)=2CO(g); ΔH=+172.5 kJ·mol-1
D.若金刚石燃烧热大于石墨的燃烧热,则石墨转变为金刚石需要吸热
课后训练
2.已知25℃、10lkPa条件下:
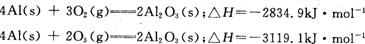
由此得出的正确结论是
A.等质量的02比O3能量低,由O2变O3为吸热反应
B.等质量的02比O3能量低,由02变O3为放热反应
C.O3比02稳定,由02变O3为吸热反应 D.02比O3稳定,由02变O3为放热反应
1.1840年,俄国化学家盖斯(G·H·Hess)从大量的实验事实中总结出了一条规律:化学反应不管是一步完成还是分几步完成,其反应热是相同的,即盖斯定律。盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为Y kJ/mol,则1mol C与O2反应生成CO的反应热△H为
A.-Y kJ/mol B.-(10X-Y) kJ/mol
C.-(5X-0.5Y) kJ/mol D.+(10X-Y) kJ/mo
5.(06盐城期末)设NA表示阿伏加德罗常数,下列有关说法正确的是
A.分解H2O2制O2,每生成1mol O2转移,4NA个电子
B.25℃时1LpH=7的醋酸与醋酸钠的混合溶液中,一定有10-7NA个醋酸分子被电离
C.标准状况下,22gC3H8与N2O混合气体所占体积约为11.2L
D.用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2溶液,当有0.2NA个电子转移时,阴极析出6.4g金属
答案:1C2BC3B 1CD2B3BC4C5C
2010年浙江省高考化学易错题强化训练
热点四 化学反应与能量变化
课堂训练
4.以NA表示阿佛加德罗常数,下列说法中正确的是
A 53g碳酸钠中含NA个CO32-
B 0.1molOH-和0.1mol-OH均含NA个电子
C 9.8gH2SO4和H3PO4 的混合物中所含质子数为0.4NA
D 标准状况下11.2L臭氧中含NA个氧原子
3.设NA表示阿伏加德罗常数,下列叙述中正确的是
A 常温常压下,11.2L氧气所含的原子数为NA
B 1.8g的NH4+离子中含有的电子数为NA
C 常温常压下,48gO3和O2的混合气体含有的氧原子数为3NA
D 2.4g金属镁变为镁离子时失去的电子数为0.1NA
2.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.石英晶体中,有NA个Si就有2NA个Si-Si键
B.0.8gCaCO3、Mg3N2和碳酸氢钾的混合物中所含质子数为0.4NA
C.标准状况下,2.24L乙醛完全燃烧所得CO2分子数为0.2NA
D.在含2molH2SO4的浓H2SO4溶液中加入足量的Zn粉,使其充分反应,则反应结束时转移电子数共4NA
1.NA表示阿伏加德罗常数,下列各组物质在一定条件下充分反应后,生成气体物质的分子数可能大于或等于NA的是
A. 400mL10 mol·L-1的浓盐酸与足量的MnO2反应
B.2molCu与200g98%的浓硫酸反应
C.65gZn与足量的硝酸反应
D.H2O(g)和CO2混合气体2mol与足量的Na2O2反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com