
Ηψ«εΆ§œΒΈοΓΔΆ§Ζ÷“λΙΙΧεΒΡΗ≈ΡνΘΜΑ―Έ’ΝΫ’ΏΒΡ≈–Εœ±ξΉΦΘΜ»œ Ε≤Δ’ΤΈ’Ά§œΒΈοΓΔΆ§Ζ÷“λΙΙΧεΒΡΧΊΒψΚΆ“ΜΑψΙφ¬…ΓΘΓΓΓΓ
1Θ°Ά§œΒΈο (1)Ά§œΒΈο±Ί–κΫαΙΙœύΥΤΘ§Φ¥Ήι≥…‘ΣΥΊœύΆ§Θ§ΙΌΡήΆ≈÷÷άύΓΔΗω ΐ”κΝ§Ϋ”ΖΫ ΫœύΆ§Θ§Ζ÷Ή”Ήι≥…Ά® ΫœύΆ§ΓΘΓΓ
(2)Ά§œΒΈοœύΕ‘Ζ÷Ή”÷ ΝΩœύ≤ν14Μρ14ΒΡ’ϊ ΐ±ΕΓΘ(3)Ά§œΒΈο”–œύΥΤΒΡΜ·―ß–‘÷ Θ§Έοάμ–‘÷ ”–“ΜΕ®ΒΡΒί±δΙφ¬…ΓΘΓΓ
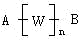 άΐ1Θ°œ¬Ν–ΗςΉιΈο÷ Θ§Τδ÷– τ”ΎΆ§œΒΈοΒΡ «ΘΚ
ΓΓ(1)““œ©ΚΆ±Ϋ““œ©ΓΓ (2)±ϊœ©ΥαΚΆ”ΆΥαΓΓ (3)““¥ΦΚΆ±ϊΕΰ¥ΦΓΓ (4)ΕΓΕΰœ©”κ“λΈλΕΰœ©ΓΓ (5)’αΧ«”κ¬σ―ΩΧ«
ΓΓ ΓΓAΘ°(1)(2)(3)(4)ΓΓ ΓΓBΘ°(2)(4)ΓΓΓΓ CΘ°(1)(2)(4)(5)ΓΓ DΘ°(1)(2)(4)
άΐ1Θ°œ¬Ν–ΗςΉιΈο÷ Θ§Τδ÷– τ”ΎΆ§œΒΈοΒΡ «ΘΚ
ΓΓ(1)““œ©ΚΆ±Ϋ““œ©ΓΓ (2)±ϊœ©ΥαΚΆ”ΆΥαΓΓ (3)““¥ΦΚΆ±ϊΕΰ¥ΦΓΓ (4)ΕΓΕΰœ©”κ“λΈλΕΰœ©ΓΓ (5)’αΧ«”κ¬σ―ΩΧ«
ΓΓ ΓΓAΘ°(1)(2)(3)(4)ΓΓ ΓΓBΘ°(2)(4)ΓΓΓΓ CΘ°(1)(2)(4)(5)ΓΓ DΘ°(1)(2)(4)
άΐ2Θ°»γΙϊΕ®“ε”–ΜζΈοΒΡΆ§œΒΝ– «“ΜœΒΝ–ΫαΙΙΦρ ΫΖϊΚœΘΚ ΓΓ(Τδ÷–n=0ΓΔ1ΓΔ2ΓΔ3Γ≠Γ≠)ΒΡΜ·ΚœΈοΓΘ Ϋ÷–AΓΔB «»Έ“β“Μ÷÷ΜυΆ≈(Μρ«β‘≠Ή”)Θ§wΈΣ2ΦέΒΡ”–ΜζΜυΆ≈Θ§”÷≥ΤΈΣΗΟΆ§œΒΝ–ΒΡœΒ≤νΓΘΆ§œΒΝ–Μ·ΚœΈοΒΡ–‘÷ ΆυΆυ≥ œ÷Ιφ¬…–‘±δΜ·ΓΘœ¬Ν–ΥΡΉιΜ·ΚœΈο÷–Θ§≤ΜΩ…≥ΤΈΣΆ§œΒΝ–ΒΡ «ΘΚ ΓΓAΘ°CH3CH2CH2CH3 ΓΓ CH3CH2CH2CH2CH3ΓΓ ΓΓ ΓΓ CH3CH2CH2CH2CH2CH3 ΓΓBΘ°CH3CHΘΫCHCHO ΓΓ CH3CHΘΫCHCHΘΫCHCHOΓΓ ΓΓ CH3(CH=CH)3CHO ΓΓCΘ°CH3CH2CH3 ΓΓ ΓΓ CH3CHClCH2CH3ΓΓ ΓΓ ΓΓ CH3CHClCH2CHClCH3
2ΓΔ”–ΜζΈοΫαΙΙΒΡ±μ ΨΖΫΖ®
(1)ΫαΙΙ Ϋ ΓΓΕ®“εΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ≤ΜΉψΘΚ
(2)ΫαΙΙΦρ Ϋ Ε®“εΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΉΔ“β ¬œνΘΚ
(3)ΦϋœΏ ΫΘΚΕ®“εΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΉΔ“β ¬œνΘΚ
A.Α¥“Σ«σΧν–¥œ¬±μΘΚ
|
Έο÷ Οϊ≥Τ ΦΑΖ÷Ή” Ϋ |
ΫαΙΙ Ϋ |
ΫαΙΙΦρ Ϋ |
ΦϋœΏ Ϋ |
|
Έλ Άι |
ΓΓ ΓΓ |
ΓΓ |
ΓΓ |
|
1-ΕΓœ© |
ΓΓ |
ΓΓ |
ΓΓ |
|
““¥Φ |
ΓΓ |
ΓΓ |
ΓΓ |
|
““»© |
ΓΓ |
ΓΓ |
ΓΓ |
|
““Υα |
ΓΓ |
ΓΓ |
ΓΓ |
|
““Υα““θΞ |
ΓΓ |
ΓΓ |
ΓΓ |
B.ΈΣ ≤Ο¥‘ΎΫαΙΙΦρ ΫΒΡ ι–¥÷–≤ΜΡή Γ¬‘ΓΑC=CΓ·Γ·ΚΆΓΑCΓ‘CΓ±ΒΡΧΊ’ςΫαΙΙ≤ΩΖ÷ΘΩ


 C.≥Δ ‘±μ ΨΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΚΆΓΓΓΓΓΓ ΒΡΖ÷Ή” ΫΓΔΫαΙΙ ΫΚΆΫαΙΙΦρ ΫΘ§ΧεΜαΫαΙΙΦρ ΫΚΆΦϋœΏ Ϋ‘Ύ≤ΜΆ§«ΑΧαœ¬ΒΡΝιΜν”Π”ΟΓΘ
C.≥Δ ‘±μ ΨΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΚΆΓΓΓΓΓΓ ΒΡΖ÷Ή” ΫΓΔΫαΙΙ ΫΚΆΫαΙΙΦρ ΫΘ§ΧεΜαΫαΙΙΦρ ΫΚΆΦϋœΏ Ϋ‘Ύ≤ΜΆ§«ΑΧαœ¬ΒΡΝιΜν”Π”ΟΓΘ
Ζ÷Ή” Ϋ_____________ΫαΙΙ Ϋ____________________ΫαΙΙΦρ Ϋ____________________
 ΓΓΖ÷Ή” Ϋ_____________ΫαΙΙ Ϋ____________________ΫαΙΙΦρ Ϋ____________________
ΓΓΖ÷Ή” Ϋ_____________ΫαΙΙ Ϋ____________________ΫαΙΙΦρ Ϋ____________________
D.Φ“”Ο…±Ψζ«ΐ≥φΦΝΒΡ’ΝΡ‘“≤ «“Μ÷÷÷Ί“ΣΒΡ”–ΜζΈοΘ§ΤδΫαΙΙ»γΆΦΥυ ΨΘΚ
 ΓΓ
ΓΓ
ΥϋΒΡΖ÷Ή” Ϋ «________________ΦϋœΏ Ϋ «______________
E.““œ©Μυ““»≤(CH2=CH-CΓ‘CH) «“Μ÷÷÷Ί“ΣΒΡ≤Μ±ΞΚΆΧΰΘ§ΤδΖ÷Ή”άοΉνΕύ”–___________Ηω‘≠Ή”Ι≤œΏΘΜΉνΕύ”–___________Ηω‘≠Ή”Ι≤ΟφΓΘΡ«Ο¥Θ§»γΙϊ
 ΓΓ
ΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Ζ÷Ή”÷–Θ§ΉνΕύ”–___________Ηω‘≠Ή”Ι≤œΏΘΜΉνΕύ”–___________Ηω‘≠Ή”Ι≤ΟφΓΘ
4ΓΔ»τΦΉΜυ”κ“ΜΗωΤΫΟφ–ΆΫαΙΙœύΝ§Θ§‘ρΦΉΜυ…œΒΡ«β‘≠Ή”ΉνΕύ”–“ΜΗω«β‘≠Ή””κΤδΙ≤ΟφΓΘ»τ“ΜΗωΧΦ‘≠Ή”“‘ΥΡΗωΒΞΦϋ”κΤδΥϋ‘≠Ή”÷±Ϋ”œύΝ§Θ§‘ρ’βΥΡΗω‘≠Ή”ΈΣΥΡΟφΧεΫαΙΙΘ§≤ΜΩ…ΡήΙ≤ΟφΓΘΆ§ ±Θ§±ΫΜΖΕ‘ΈΜ…œΒΡ2ΗωΧΦ‘≠Ή”ΦΑΤδ”κ÷°œύΝ§ΒΡΝΫΗω«β‘≠Ή”Θ§’βΥΡ‘≠Ή”Ι≤÷±œΏΓΘ
ΓΓάΐ3ΓΔœ¬Ν–Ζ÷Ή”÷–ΒΡ14ΗωC‘≠Ή”Ω…Ρή¥Π”ΎΆ§“ΜΤΫΟφΒΡ «(BC)
ΓΓ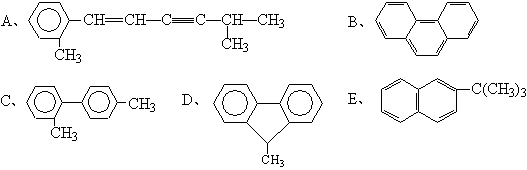 ΓΓΫβΈωΘΚ
ΓΓ
ΓΓΫβΈωΘΚ
ΓΓ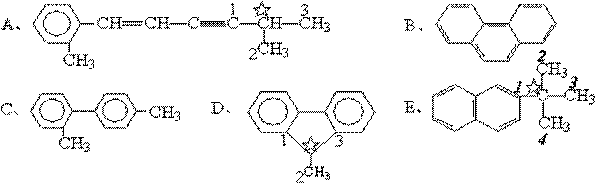
3ΓΔ»τΝΫΗω±ΫΜΖΙ≤±ΏΘ§‘ρΝΫΗω±ΫΜΖ“ΜΕ®Ι≤ΟφΓΘάΐ»γΘ§œ¬Ν–ΗςΫαΙΙ÷–Υυ”–‘≠Ή”ΕΦ‘ΎΆ§“ΜΤΫΟφ…œΓΘ

1ΓΔΓΓ ”–ΜζΈο÷–ΧΦ‘≠Ή”ΒΡ≥…ΦϋΧΊΒψ
(1)ΧΦ‘≠Ή”ΒΡΉνΆβ≤ψ”–ΥΡΗωΒγΉ”Θ§‘Ύ≥…ΦϋΙΐ≥Χ÷–Θ§Φ»Ρ―“‘ ß»Ξ’β–©ΒγΉ”Θ§ΒΪ“≤Ρ―“‘‘ΌΒΟΒΫΥΡΗωΒγΉ”Θ§“ρ¥ΥΘ§‘Ύ”–ΜζΜ·ΚœΈοΖ÷Ή”÷–Θ§ΧΦ‘≠Ή”Ήή «–Έ≥…____________Ηω__________ΦϋΓΘ
(2)ΧΦ‘≠Ή”Υυ–Έ≥…ΒΡ4ΗωΙ≤ΦέΦϋΘ§Ω…“‘≥ωœ÷Εύ÷÷–Έ ΫΘ§»γ–Έ≥…ΧΦΧΦΒΞΦϋΓΔΧΦΧΦ______ΦϋΓΔΧΦΧΦ_______ΦϋΒ»Θ§ΝμΆβΘ§ΧΦ‘≠Ή””κ«β‘≠Ή”÷°Φδ÷ΜΡή–Έ≥…ΧΦ«β________ΦϋΘ§ΧΦ‘≠Ή””κ―θ‘≠Ή”÷°Φδ‘ρΩ…“‘–Έ≥…ΧΦ―θΒΞΦϋ(C-O)ΜρΧΦ―θΥΪΦϋ(C=O)ΓΘ
(3)Β±1ΗωΧΦ‘≠Ή””κΤδΥϊ4Ηω‘≠Ή”Ν§Ϋ” ±Θ§’βΗωΧΦ‘≠Ή”ΫΪ≤…»ΓΥΡΟφΧε»Γœρ”κ÷°≥…ΦϋΘ§’βΗωΧΦ‘≠Ή”ΫΪ¥Π‘ΎΥΡΟφΧεΒΡ________ΈΜ÷ΟΓΘ»γ______Β»ΨΆ «’β―υΒΡΫαΙΙΓΘ
(4)Β±ΧΦ‘≠Ή”÷°ΦδΜρΧΦ‘≠Ή””κΤδΥϋ‘≠Ή”÷°Φδ–Έ≥…ΥΪΦϋ ±Θ§–Έ≥…ΗΟΥΪΦϋΒΡ‘≠Ή”“‘ΦΑ”κ÷°÷±Ϋ”œύΝ§ΒΡ‘≠Ή”ΕΦ¥Π‘Ύ____________…œΓΘ»γ________________________________________ΨΆ «’β―υΒΡΫαΙΙΓΘ
Β±ΧΦ‘≠Ή”÷°ΦδΜρΧΦ‘≠Ή””κΤδΥϋ‘≠Ή”÷°Φδ–Έ≥…»ΰΦϋ ±Θ§–Έ≥…ΗΟΥΪΦϋΒΡ‘≠Ή”“‘ΦΑ”κ÷°÷±Ϋ”œύΝ§ΒΡ‘≠Ή”ΕΦ¥Π‘Ύ____________…œΓΘ»γ________________________________________ΨΆ «’β―υΒΡΫαΙΙΓΘ
(1)ΓΓΓΓΓΓ ±ΞΚΆΧΦ‘≠Ή”ΘΚ____________________________________________
≤Μ±ΞΚΆΧΦ‘≠Ή”ΘΚ____________________________________________
(5)≥ΘΦϊ”–ΜζΈοΒΡΩ’ΦδΙΙ–Ά
|
”–ΜζΈο |
ΦΉΆι |
““œ© |
““»≤ |
±Ϋ |
|
Ζ÷Ή” Ϋ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
|
ΫαΙΙΦρ Ϋ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
|
ΧΦ‘≠Ή”≥… Φϋ ΖΫ Ϋ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
|
ΦϋΓΓ
Ϋ« |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
|
Ζ÷Ή”ΒΡΩ’ Φδ ΙΙ –Ά |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ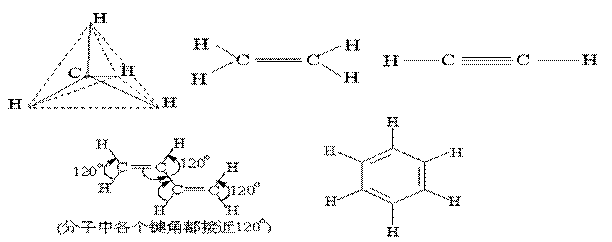
(1)ΦΉΆιΈΣ’ΐΥΡΟφΧεΫαΙΙΘ§ΦϋΫ«109ßύ28ΓδΓΘ(2)““œ©ΈΣΤΫΟφ–ΆΫαΙΙΘ§ΦϋΫ«120ßύΓΘ(3)““»≤ΈΣ÷±œΏ–ΆΫαΙΙΘ§ΦϋΫ«180ßύΓΘ (4)±ΫΈΣΤΫΟφ–ΆΫαΙΙΘ§ΦϋΫ«120ßύΓΘ(5)‘Ύ1,3-ΕΓΕΰœ©Ζ÷Ή”÷–Θ§ΥΡΗωΧΦ‘≠Ή”ΚΆΝυΗω«β‘≠Ή”ΕΦ‘ΎΆ§“ΜΤΫΟφ…œΘ§ΦϋΫ«Ϋ”Ϋϋ120ßύΓΘ
άΐ1ΓΔΦΉΆιΖ÷Ή” «“‘ΧΦ‘≠Ή”ΈΣ÷––ΡΒΡ’ΐΥΡΟφΧεΫαΙΙΘ§Εχ≤Μ «’ΐΖΫ–ΈΒΡΤΫΟφΫαΙΙΘ§άμ”… «ΘΚ(ΓΓ)
ΓΓAΓΔCH3Cl≤Μ¥φ‘ΎΆ§Ζ÷“λΙΙΧεΓΓ
BΓΔCH2Cl2≤Μ¥φ‘ΎΆ§Ζ÷“λΙΙΧεΓΓ
ΓΓCΓΔCHCl3≤Μ¥φ‘ΎΆ§Ζ÷“λΙΙΧεΓΓ DΓΔCH4÷–ΥΡΗωΦέΦϋΒΡΦϋ≥ΛΚΆΦϋΫ«ΕΦœύΒ»
2ΓΔ»τΝΫΗωΤΫΟφ–ΆΫαΙΙΒΡΜυΆ≈÷°Φδ“‘ΒΞΦϋœύΝ§Θ§’βΗωΒΞΦϋΩ…“‘–ΐΉΣΘ§‘ρΝΫΗωΤΫΟφΩ…ΡήΙ≤ΟφΘ§ΒΪ≤Μ «ΓΑ“ΜΕ®Γ±ΓΘ
άΐ2ΓΔ“―÷ΣΓΑC-CΓ±ΒΞΦϋΩ…“‘»Τ÷α–ΐΉΣΘ§ΫαΙΙΦρ ΫΈΣ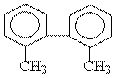 ΒΡΧΰΘ§Κ§±ΫΜΖ«“¥Π”ΎΆ§“ΜΤΫΟφΒΡC‘≠Ή”Ηω ΐ÷Ν…Ό”–(ΓΓ)
ΓΓAΓΔ6ΓΓΓΓ BΓΔ8 ΓΓΓΓCΓΔ9ΓΓΓΓ DΓΔ14
ΓΓΫβΈωΘΚ
ΒΡΧΰΘ§Κ§±ΫΜΖ«“¥Π”ΎΆ§“ΜΤΫΟφΒΡC‘≠Ή”Ηω ΐ÷Ν…Ό”–(ΓΓ)
ΓΓAΓΔ6ΓΓΓΓ BΓΔ8 ΓΓΓΓCΓΔ9ΓΓΓΓ DΓΔ14
ΓΓΫβΈωΘΚ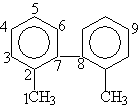
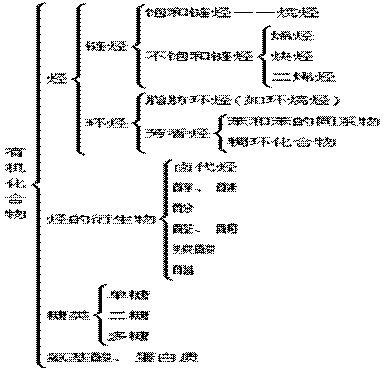
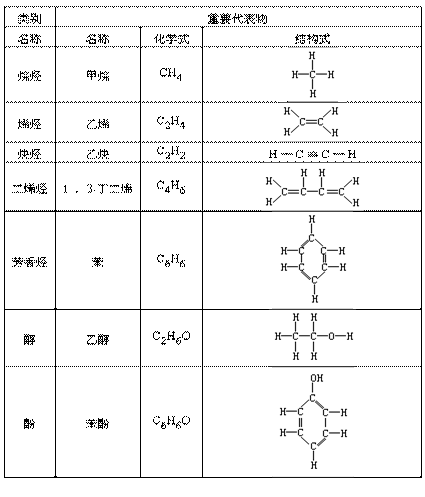
Ε‘Ηςάύ”–ΜζΈοΕΦ“ΣΆ®ΙΐΤδ÷Ί“Σ¥ζ±μΈοΫχ––―ßœΑΒΡΓΘœ÷ΫΪ÷–―ßΩΈ±Ψ÷–Ηςάύ”–ΜζΈο÷–÷ς“Σ¥ζ±μΈοΒΡΉι≥…ΚΆΫαΙΙΝ–”Ύœ¬±μ÷–ΘΚ
 ΓΓ
ΓΓ
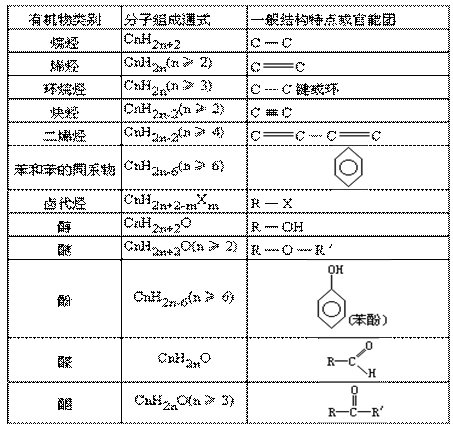
”–ΜζΈοΒΡ÷ς“Σάύ±πΒΡΖ÷Ή”Ήι≥…Ά® ΫΚΆΖ÷Ή”ΫαΙΙΧΊΒψ(Αϋά®ΥυΚ§”–ΒΡΙΌΡήΆ≈)ΓΘ
ΧΰΚΆΧΰΒΡ―ή…ζΈο «÷–―ß”–ΜζΜ·―ßΒΡ÷ΊΒψΡΎ»ίΘ§œ÷ΫΪΤδΗςάύ”–ΜζΈοΒΡΉι≥…ΚΆΫαΙΙΧΊΒψΝ–”Ύœ¬±μ÷–ΓΘ
 ΓΓ
ΓΓ ΓΓ
ΓΓ
ΥΒΟςΘΚ±μ÷–ΧΰΒΡ―ή…ζΈοΖ÷Ή”Ήι≥…Ά® ΫΚΆ“ΜΑψΫαΙΙΧΊΒψΘ§÷ΜΨ÷œό”ΎΧΰΜυΈΣ±ΞΚΆ÷§ΖΨΧΰΜυΘ§ΕχΖ÷Ή”÷–ΙΌΡήΆ≈“≤÷Μ”–“ΜΗωΒΡ”–ΜζΈοΘ§»γ±μ÷–ΒΡΓΑ¥ΦΓ±÷ΗΒΡ «±ΞΚΆ“Μ‘Σ¥ΦΘΜΓΑθΞΓ±“≤÷Η±ΞΚΆ“Μ‘Στ»ΥαΚΆ±ΞΚΆ“Μ‘Σ¥ΦΥυ…ζ≥…ΒΡθΞΓΘ
11.(1)ΫΪ–ΩΤ§ΚΆ“χΤ§Ϋΰ»κœΓΝρΥα÷–Ήι≥…‘≠Βγ≥ΊΘ§ΝΫΒγΦΪΦδΝ§Ϋ”“ΜΗωΒγΝςΦΤΓΘ
–ΩΤ§…œΖΔ…ζΒΡΒγΦΪΖ¥”Π ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ“χΤ§…œΖΔ…ζΒΡΒγΦΪΖ¥”Π ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)»τΗΟΒγ≥Ί÷–ΝΫΒγΦΪΒΡΉή÷ ΝΩΈΣ60 gΘ§ΙΛΉς“ΜΕΈ ±ΦδΚσΘ§»Γ≥ω–ΩΤ§ΚΆ“χΤ§œ¥ΨΜΗ…‘οΚσ≥Τ÷ΊΘ§Ήή÷ ΝΩΈΣ47 gΘ§ ‘ΦΤΥψΘΚ
ΔΌ≤ζ…ζ«βΤχΒΡΧεΜΐ(±ξΉΦΉ¥Ωω)ΘΜ
ΔΎΆ®ΙΐΒΦœΏΒΡΒγΝΩΓΘ(“―÷ΣNA=6.02ΓΝ1023/molΘ§ΒγΉ”ΒγΝΩΈΣ1.60ΓΝ10-19C)
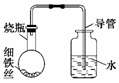
10.Ρ≥―ß…ζ‘ΎAΓΔBΓΔCΓΔDΥΡΗω–Γ…’ΤΩ÷–Ζ÷±πΖ≈»κΗ…‘οΒΡœΗΧζΥΩΓΔΫΰΙΐ ≥―ΈΥ°ΒΡœΗΧζΥΩΓΔΫΰΙΐ«εΥ°ΒΡœΗΧζΥΩΓΔ ≥―ΈΥ°ΦΑœΗΧζΥΩ(≤Δ ΙΧζΥΩΆξ»ΪΫΰΟΜ‘Ύ ≥―ΈΥ°÷–)ΓΘ»ΜΚσΉιΉΑ≥…»γœ¬ΆΦΥυ ΨΒΡΥΡΧΉΉΑ÷ΟΘ§ΟΩΗτ“ΜΕΈ ±Φδ≤βΝΩΒΦΙή÷–Υ°Οφ…œ…ΐΒΡΗΏΕ»Θ§ΫαΙϊ»γœ¬±μ(±μ÷–ΥυΝ– ΐΨίΈΣΒΦΙή÷–Υ°Οφ…œ…ΐΒΡΗΏΕ»/cm)Υυ ΨΘΚΓΓ
|
±Φδ/–Γ ± |
0 |
0.5 |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
|
AΤΩ( ΔΫΰΙΐ ≥―ΈΥ°ΒΡΧζΥΩ) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
BΤΩ( ΔΫΰΙΐ ≥―ΈΥ°ΒΡΧζΥΩ) |
0 |
0.4 |
1.2 |
3.4 |
5.6 |
7.6 |
9.8 |
|
CΤΩ( ΔΫΰΙΐ«εΥ°ΒΡΧζΥΩ) |
0 |
0 |
0 |
0.3 |
0.8 |
2.0 |
3.5 |
|
DΤΩ( ΔΆξ»ΪΫΰΟΜ‘Ύ ≥―ΈΥ°÷–ΒΡΧζΥΩ) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
(1)ΈΣ ≤Ο¥”–ΒΡΒΦΙή÷–Υ°ΟφΜα…œ…ΐΘΩΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)…œ ω Β―ι÷–Θ§Χζ…ζ–βΒΡΥΌ¬ ”…¥σΒΫ–ΓΒΡ≈≈Ν–Υ≥–ρΈΣ(Χν–Γ…’ΤΩΒΡΉ÷ΡΗ±ύΚ≈)ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)”ΑœλΧζ…ζ–βΒΡ“ρΥΊ≥ΐ―θΤχΆβΜΙ”–ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(4)»’≥Θ…ζΜν÷–≥ΘΦϊΒΡΧζ÷ΤΤΖ…ζ≥…Χζ–βΘ§ ‘–¥≥ωΧζ÷ΤΤΖ…ζ≥…Χζ–β(Fe2O3ΓΛxH2O)ΒΡΜ·―ßΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
(5)Ά®Ιΐ…œΟφΒΡ―–ΨΩΘ§Ρψ»œΈΣ‘Ύ»’≥Θ…ζΜν÷–”ΠΗΟ»γΚΈ±ΘΜΛΧζΙχΒ»Χζ÷ΤΤΖΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
9.ΫΪΆ≠Ατ”κ–ΩΑτ”ΟΒΦœΏΝ§Ϋ”Θ§“ά¥Έ≤ε»κΖ÷±π Δ”–ΘΚΔΌΝρΥα»ή“ΚΘΜΔΎΝρΥαΆ≠»ή“ΚΘΜΔέΝρΥαΡΤ»ή“ΚΒΡ»ΐΗω…’±≠÷–Θ§¥Υ ±Θ§
(1)Ά≠Τ§…œΖΔ…ζΒΡ÷ς“ΣΖ¥”Π «ΘΚ
ΔΌΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΔΎΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΜ
ΔέΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)Ά≠÷ΤΤΖ‘ΎΨ≠≥Θœ¬Υα”ξΒΡΒΊ«χΒγΜ·―ßΗ· ¥―œ÷ΊΘ§–¥≥ω¥ΥΒγΜ·―ßΗ· ¥ΒΡΒγΦΪΖ¥”Π ΫΘΚ
’ΐΦΪΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜΗΚΦΪΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)ΫΪ±μΟφ»ΞΒτ―θΜ·ΡΛΒΡΟΨΤ§”κ¬ΝΤ§”Ο¥χΒγΝς±μΒΡΒΦœΏΝ§Ϋ”Θ§≤ε»κ Δ”–…’Φν»ή“ΚΒΡ…’±≠÷–Θ§¥Υ ±ΖΔœ÷ΒγΝςΦΤ÷Η’κΤΪΉΣΘ§≈–Εœ¥Υ‘≠Βγ≥ΊΒΡ’ΐΗΚΦΪΘ§≤Δ–¥≥ωΒγΦΪΖ¥”Π ΫΚΆΉήΖ¥”ΠΖΫ≥Χ ΫΓΘ
’ΐΦΪΘΚΓΓΓΓ Θ§ΒγΦΪΖ¥”Π ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜΗΚΦΪΘΚΓΓΓΓ Θ§ΒγΦΪΖ¥”Π ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§
ΉήΖ¥”Π ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΘ
8.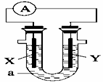 (2009ΓΛ…ΫΕΪΝΡ≥«)»γΆΦXΈΣΒΞ÷ ΙηΘ§YΈΣΫπ τΧζΘ§aΈΣNaOH»ή“ΚΘ§Α¥ΆΦΉιΉΑ≥…“ΜΗω‘≠Βγ≥ΊΘ§‘ρœ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(2009ΓΛ…ΫΕΪΝΡ≥«)»γΆΦXΈΣΒΞ÷ ΙηΘ§YΈΣΫπ τΧζΘ§aΈΣNaOH»ή“ΚΘ§Α¥ΆΦΉιΉΑ≥…“ΜΗω‘≠Βγ≥ΊΘ§‘ρœ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
A. XΈΣΗΚΦΪΘ§ΒγΦΪΖ¥”ΠΈΣSi-4e- Si4+
Si4+
B.YΈΣΗΚΦΪΘ§ΒγΦΪΖ¥”ΠΈΣ4H2O+4e- 4OH-+2H2Γϋ
4OH-+2H2Γϋ
C.XΈΣΗΚΦΪΘ§ΒγΦΪΖ¥”ΠΈΣSi+6OH--4e- SiO
SiO +3H2O
+3H2O
D.YΈΣΗΚΦΪΘ§ΒγΦΪΖ¥”ΠΈΣFe-2e- Fe2+
Fe2+
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com