
6.西方人普遍认为,哥伦布是“一个将要统治世界的慈善的白人帝国主义之父和一个晚近被推举为天主教圣徒的候选人”。在西方人看来,哥伦布开辟新航路的作用是 ①确立欧洲对世界的统治 ②传播天主教 ③掠夺金银财富 ④推动商品输出
A.①② B.②③④ C.③④ D.①②④
5.16世纪葡萄牙著名诗人德·卡蒙斯这样深情地描绘他的祖国:“大陆,在这里是尽头; 大海,在这里才开头。”诗句中反映了他对祖国引以为豪的是
A.成为“海上马车夫” B.垄断欧亚之间的贸易
C.率先开辟新航路 D.处于欧洲商业中心地位
4.平遥是著名“晋商”的发源地之一。清代道光四年(公元1824年),中国第一家现代银行的雏形“日升昌”票号在平遥诞生。三年之后,“日升昌”在中国很多省份先后设立分支机构。19世纪40年代,它的业务更进一步扩展到日本、新加坡、俄罗斯等国家。从上述材料中我们不能得出的结论是
A.我国实现了经济中心的转移 B.晋商善于资本运作
C.晋商是实力非常雄厚的商帮 D.汇兑事业在中国得以发展
3. 乾隆皇帝对英商送给他的时钟不屑一顾,说中国小民无此物者甚众,
乾隆皇帝对英商送给他的时钟不屑一顾,说中国小民无此物者甚众,
但从来没有误了早上起来下地,也从来没有误了晚上回家睡觉。对此
现象,下列评价确切的是
A.乾隆帝为维护国家尊严,痛斥侵略者的野心
B.乾隆帝认为中国农民勤劳自觉,不需要闹钟
C.是小农经济下的一种天朝上国的心态的流露
D.乾隆帝为维护天朝体制,担心小农玩物丧志
2.明朝时,松江有“卖袜店百余家,合郡男妇皆以做袜为业,从店中给酬取直”。对上述材料理解不正确的是
A.松江绝大多数劳动者成了雇佣工人 B.卖袜店商人直接支配生产,变成资本家
C.松江棉纺织业出现了资本主义萌芽 D.当时自然经济已丧失统治地位
1.下列生产工具,按用途划分,不同于其它各项的是

A.杜诗水排 B.高转筒车 C.马钧翻车 D.风力水车
21.(12分)高温超导材料是科学家研究的重点物质之一。
⑴科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如下左图所示。该富勒烯化合物中的K原子和C60分子的个数比为 ▲ 。


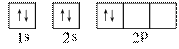
⑵某同学画出的C的核外电子排布(轨道表示式)如上右图所示,该电子排布图(轨道表示式)违背了 ▲ ,请你画出正确的电子排布图(轨道表示式) ▲ 。
⑶金属钾采用的是下列 ▲ (填字母代号)堆积方式。




A B C D
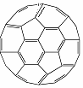 ⑷富勒烯(C60)的结构如右图。
⑷富勒烯(C60)的结构如右图。
①1 mol C60分子中σ键的数目为 ▲ 。
②已知:金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm。有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由: ▲ 。
20.(12分)一般地,晶体类型不同,其结构和性质也不同。
⑴下表是四种同主族元素的氧化物的离子晶体晶格能数据。
|
氧化物 |
MgO |
CaO |
SrO |
BaO |
|
晶格能/ kJ·mol-1 |
3791 |
3410 |
3223 |
3054 |
①将上表中四种氧化物的共熔物冷却,首先析出的是 ▲ 。
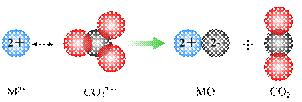
②碳酸盐的热分解示意图如下图。两种碳酸盐的热分解温度CaCO3 ▲ SrCO3(填“高于”或“低于”)
 ⑵已知NH3·H2O的电离方程式为NH3·H2O
⑵已知NH3·H2O的电离方程式为NH3·H2O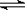 NH4++OH-,当氨水冷却时,可以将NH3·H2O和2NH3·H2O等晶体沉淀出来。
NH4++OH-,当氨水冷却时,可以将NH3·H2O和2NH3·H2O等晶体沉淀出来。
①2NH3·H2O的晶体类型为 ▲ 。
②NH3极易溶于水,其主要原因是 ▲ 。
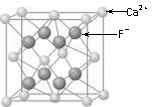
⑶CaF2的晶体结构如右图所示。
①CaF2晶体中钙离子的配位数是 ▲ 。
②一个CaF2晶胞中包含 ▲ 个钙离子。
19.(12分)为比较温室效应气体对全球增温现象的影响,科学家以CO2为相对标准,引入了“温室效应指数”的概念(如下表)。
回答下列问题:
⑴6种气体中,温室效应指数最大的物质属于 ▲ (选填“极性分子”或“非极性分子”)。
⑵在水分子中,O原子上的价层电子对数为 ▲ 。
⑶N2O4分子结构式为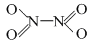 ,分子为平面结构。N2O4分子中N原子的杂化方式为 ▲ ,在N2O4分子的结构式上,将你认为是配位键的共价键上加上箭头 ▲ 。
,分子为平面结构。N2O4分子中N原子的杂化方式为 ▲ ,在N2O4分子的结构式上,将你认为是配位键的共价键上加上箭头 ▲ 。
⑷O3具有吸收紫外光的功能。
①根据等电子原理,判断O3分子的空间构型为 ▲ 。
②紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因: ▲ 。
|
共价键 |
C-C |
C-N |
C-S |
|
键能/ kJ·mol-1 |
347 |
305 |
259 |
18.(12分)已知A、B、C、D、E、F均为周期表中前36号元素,且原子序数依次增大。A、B、C为同一周期的主族元素,B原子p能级电子总数与s能级电子总数相等。A、F原子未成对电子是同周期中最多的,且F基态原子中电子占据三种不同形状的原子轨道。D和E原子的第一至第四电离能如下表所示:
|
电离能/ kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
|
D |
738 |
1451 |
7733 |
10540 |
|
E |
578 |
1817 |
2745 |
11578 |
⑴A、B、C三种元素的电负性最大的是 ▲ (填写元素符号),D、E两元素中D的第一电离能较大的原因是 ▲ 。
⑵F基态原子的核外电子排布式是 ▲ ;在一定条件下,F原子的核外电子从基态跃迁到激发态产生的光谱属于 ▲ 光谱(填“吸收”或“发射”)。
⑶根据等电子原理,写出AB+的电子式: ▲ 。
⑷已知:F3+可形成配位数为6的配合物。组成为FCl3·6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3∶2∶1。则绿色配合物的化学式为 ▲ 。
A.[CrCl (H2O)5]Cl2·H2O B.[CrCl2(H2O)4]Cl·2H2O
C.[Cr(H2O)6]Cl3 D.[CrCl3(H2O)3] ·3H2O
|
物质 |
大气中的含量 (体积百分比) |
温室效应 指数 |
|
CO2 |
0.03 |
1 |
|
H2O |
1 |
0.1 |
|
CH4 |
2×10-4 |
30 |
|
N2O4 |
3×10-5 |
160 |
|
O3 |
4×10-6 |
2000 |
|
CCl2F2 |
4.8×10-8 |
25000 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com