
1. 证明CH3COOH为弱酸,现有药品和仪器;冰醋酸,蒸馏水、pH试纸,请你设计实验证明:
(1)设计的理论依据是 ;
(2)简要步骤是: ;
(3)需要记录的数据是 ;
(4)分析推断:由于 ,说明 ,所以CH3COOH是弱酸。
5. 解题的基本思路
明确目的→弄清原理→具体设计→数据处理
[典型例题]
[例1] 铝粉是铝热剂的主要成份之一,常用铝锭制得的铝粉中含有少量的 和
和 ,用如图所示的装置(甲乙管用橡皮管连接可上下移动)测定铝粉中金属铝的含量,其方法是:用硫酸或氢氧化钠溶液与样品作用,通过产生的气体体积计算样品中金属铝的含量,根据实验原理回答下列问题:
,用如图所示的装置(甲乙管用橡皮管连接可上下移动)测定铝粉中金属铝的含量,其方法是:用硫酸或氢氧化钠溶液与样品作用,通过产生的气体体积计算样品中金属铝的含量,根据实验原理回答下列问题:
(1)如何检验此装置的气密性 。
(2)从硫酸和氢氧化钠溶液两种试剂中挑选,应选用 较好,理由是 。
(3)装置中导管a所起的作用是 。
A. 保证实验装置不漏气 B. 使分液漏斗中的液体顺利滴下
C. 减少气体体积测定的误差
(4)为了较准确测量产生的气体体积,在反应前后读取甲管液面的读数时应注意 。
A. 反应前读取甲管液面数据时应使甲、乙中液面保持水平
B. 反应后读取甲管液面数据时应使甲、乙中液面保持水平
C. 反应后读取甲管液面数据时,甲、乙两管液面无须保持水平
D. 反应后立即读取甲管液面数据,防止液面变动
E. 反应后静止置一会,待反应器恢复原来温度后再读取数据
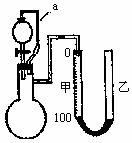
解析:该题的实验目的是测定铝粉中金属铝的含量,且通过产生气体的体积经计算求出--是一道定量题,要求实验的准确性。
(1)凡是有气体参加和生成的实验,都必须检验装置的气密性,根据气密性检查的方法。该题应采用注水法--液封法,关闭分液漏斗的旋钮向乙中注水。并记下液面位置,静置一段时间后,看液面是否下移,若仍维持液面高度则气密性良好。
(2)由于样品中含有SiO2,不与硫酸反应,不能确定铝是否反应完全(有部分铝会包裹在SiO2中,使实验结果产生一定误差,则应选择NaOH,使样品全部溶解,Al可充分反应,减少误差。)
答案:
(1)向乙中注水,使之与甲产生液面差,记下乙中液面位置,静置,乙中液面不下移,即可。
(2)NaOH;可使样品全部反应,减少误差。
(3)B
(4)AE
[例2] 四氯化钛是无色液体,沸点为136℃,它极易水解,遇空气中水蒸气即产生“白烟”(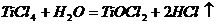 )。四氯化钛可由
)。四氯化钛可由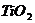 与
与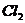 发生置换反应而制得(
发生置换反应而制得(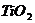 不与HCl反应)。此反应在1000℃高温下进行得很慢,但如果有炭粉存在时,只要650℃-850℃反应便可顺利进行。下面是某同学设计的实验室制备
不与HCl反应)。此反应在1000℃高温下进行得很慢,但如果有炭粉存在时,只要650℃-850℃反应便可顺利进行。下面是某同学设计的实验室制备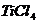 装置:
装置:
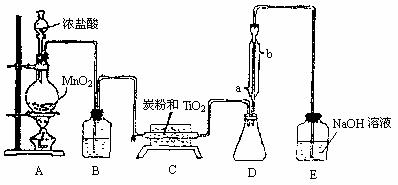
请回答:
(1)A装置中反应的化学方程式是 。
(2)B装置中的试剂为 ,其作用是 。
(3)C装置中的反应方程式为 。
(4)D装置中冷凝水的方向为 进 出,该装置的作用为 。
(5)E装置中NaOH溶液的作用是 。
(6)请指出装置的缺陷和不妥之处,并进行改进 。
解析:根据题,该信息和实验装置可知(1)A装置中发生的是实验室制Cl2的反应。因TiCl4“极易水解,遇水蒸气产生‘白烟’”可推知B装置中应为干燥剂--浓H2SO4。又由题中“TiCl4可由TiO2与Cl2发生置换反应而制得”信息可完成(3)问。并根据竖直使用冷凝管的原理,可得冷凝水的进、出方向。由于产生的Cl2不会完全消耗,必须在实验后吸收,防污染环境。缺点在于E装置无排空气孔,D、E间缺干燥器。
答案:
(1)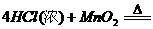
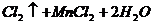
(2)浓H2SO4;吸放Cl2中水蒸气
(3)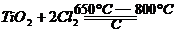
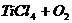
(4)a、b;使TiCl4冷凝回流进入D
(5)吸收Cl2
(6)① E装置无排气孔,应在胶塞上加一支玻璃导管,与大气相通。
② D、E间应加干燥装置
[模拟试题]
4. 装置的改进及一般实验装置的归纳
(1)制备气体的发生装置
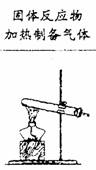
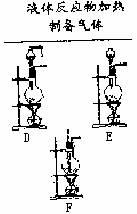


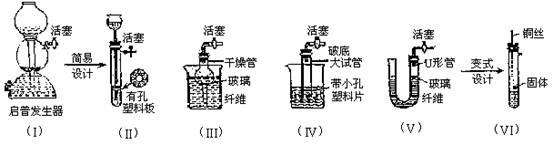
(2)气体的净化和干燥

(3)气体的收集方法
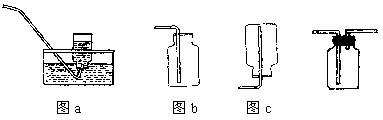
(4)尾气的处理装置

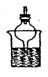
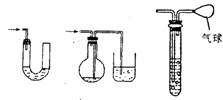
(5)安全瓶
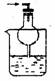
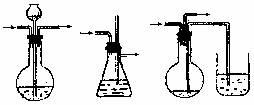
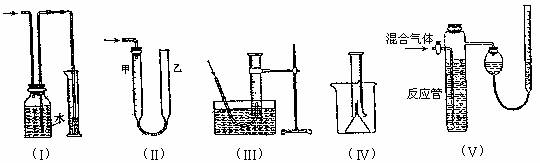
(6)气体体积的测量
 (7)喷泉实验装置的设计
(7)喷泉实验装置的设计
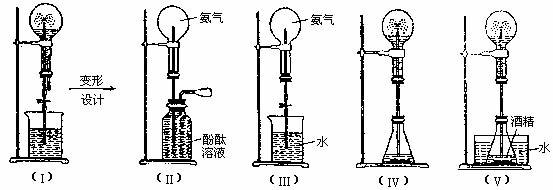
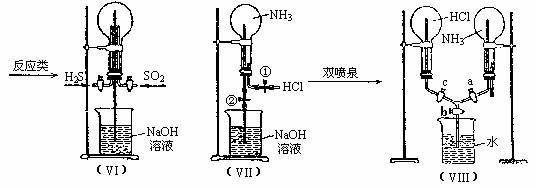
3. 综合实验的创新设计及基本实验原理的灵活应用
2. 综合实验设计的评价:
方案的可制性及优劣
1. 综合实验设计的基本原则是:
实验原理的科学性、安全性、简约性、直观性
化学实验部分(三)综合化学实验设计与评价
15. 在室温下,氯气将氨里的负三价氮元素氧化成零价氮。
(1)写出氨里的氮元素恰好全部被氧化的化学方程式。
根据上述反应原理,在下列①-⑩的十种试剂中选用试剂,(A)-(F)六种装置中选用装置,在实验室里制取纯净、干燥的氮气。
十种试剂是:① 水、② 浓硫酸、③ 浓硝酸、④ 浓盐酸、⑤ 稀氢氧化钠溶液、⑥ 四氯化碳、⑦ 氯化钠固体、⑧ 氯化铵晶体、⑨ 二氧化锰、⑩ 消石灰粉末。六种装置如图所示。
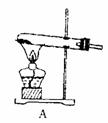
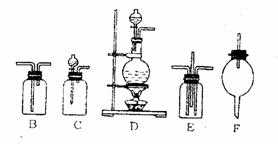
(2)请按下面实验步骤填入要求的内容。
步骤一:分别制氨气和氯气
|
制氨气 |
试剂的编号:
化学反应方程式: 发生装置编号: |
|
制氯气 |
试剂的编号:
化学反应方程式: 发生装置编号: |
步骤二:制氮气反应装置编号:
步骤三:净化
① 尾气部分:当反应装置里的氨气、氯气的物质的量之比大于 时,尾气中一定含有较多的氨气;当反应装置里的氨气、氯气物质的量之比小于 时,尾气一定含有较多的氯气。
② 尾气的处理和氮气的干燥:在制得的气体中含有少量氯化氢和氯气。为了除去氯化氢和氯气并得到干燥的氮气,可将混合气体先通过 ,再通过 处理(以上两空格填试剂编号)。

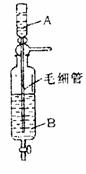
14. 有一种装置是用来制备某种干燥纯净的气体的,如图所示,A中盛放一种密度比B中液体密度小的液体。下表为几种液体的密度:
|
溶液 |
浓盐酸 |
浓硫酸 |
浓氨水 |
浓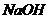 溶液 溶液 |
浓醋酸 |
密度/(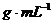 ) ) |
1.19 |
1.84 |
0.89 |
1.41 |
1.06 |
现从表中选出几种适宜的液体,利用该装置制出干燥纯净的气体。
(1)利用该装置可以制备干燥纯净的气体是什么?A、B中分别选择哪种液体?
(2)装置中毛细管的作用是什么?
13. 在下列实验装置示意图中A是简易的氢气发生器,B是大小适宜的圆底烧瓶,C是装有干燥剂的U型管,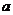 是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞的试管。
是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞的试管。
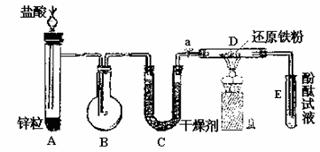
实验前先检查实验装置的气密性。实验开始时,先关闭活塞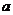 ,并取下烧瓶B;向A中加入一定量浓度适当的盐酸,产生氢气。经必要的“操作”后,在导管的出口处点燃氢气,然后如图所示装上烧瓶B,塞紧瓶塞,氢气在烧瓶中继续燃烧,用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞
,并取下烧瓶B;向A中加入一定量浓度适当的盐酸,产生氢气。经必要的“操作”后,在导管的出口处点燃氢气,然后如图所示装上烧瓶B,塞紧瓶塞,氢气在烧瓶中继续燃烧,用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞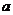 ,气体通过反应管D进入试管E中,使酚酞试液呈红色。请回答下列问题:
,气体通过反应管D进入试管E中,使酚酞试液呈红色。请回答下列问题:
(1)实验前如何检查装置的气密性? 。
(2)点燃氢气前必须进行 操作,进行该操作的方法是 。
(3)写出B、D中分别发生的化学反应方程式:
B中: ,D中: 。
(4)C中所盛干燥剂的名称是 ,该干燥剂的作用是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com