
6. 实验习题
(1)使用仪器的技能
|
仪器名称 |
教学要求 |
仪器名称 |
教学要求 |
|
试管 |
c |
量筒 |
c |
|
试管夹 |
c |
容量瓶 |
a |
|
玻璃棒 |
c |
锥形瓶 |
b |
|
酒精灯 |
c |
胶头滴管(滴瓶) |
c |
|
烧杯 |
c |
滴定管 |
a |
|
烧瓶 |
b |
铁架台 |
b |
(2)实验操作的技能
|
实验操作 |
教学要求 |
实验操作 |
教学要求 |
|
药品的取用 |
c |
过滤 |
b |
|
洗涤玻璃仪器 |
b |
蒸发 |
b |
|
连接仪器装置 |
b |
配制物质的量浓度的 |
a |
|
检查装置气密性 |
b |
溶液 |
a |
|
排水、排气集气 |
c |
中和滴定 |
b |
|
称量 |
c |
焰色反应 |
b |
|
研磨 |
a |
使用指示剂 |
|
(3)对上述两表中所涉及的仪器,还要求了解仪器的名称、形状、用途和操作原理,初步学会绘制简单仪器装置图。
(4)要求学生学会观察并如实记录实验现象及数据,能根据实验现象及实验数据分析得出结论,并书写实验报告。
(5)要求学生遵守实验室规则,注意安全操作,了解实验室一般事故的预防和处理方法。
5. 碱金属及其化合物的性质
4. 浓硫酸的性质 硫酸根离子的检验
3. 氯、溴、碘的性质 氯离子的检验
2. 配制一定物质的量浓度的溶液
高一化学实验复习
全日制普通高级中学化学教学大纲实验部分要求:
必修(化学Ⅰ)学生实验部分,化学实验基本操作(必修)
1. 同周期、同主族元素性质的递变
11. 根据实验室中测定硫酸铜晶体结晶水含量的实验,填写下列空白。
(1)从下列仪器选出所需仪器(用标号字母填写) 。
(A)托盘天平(带砝码)、(B)研钵、(C)试管夹、(D)酒精灯、(E)蒸发皿、(F)玻璃棒、(G)坩埚、(H)干燥器、(I)石棉网、(J)三脚架
除上述仪器外,还需要的仪器是 。
(2)某学生实验后得到以下数据:
|
加热前质量 |
加热后质量 |
|
|
W1(容器) |
W2(容器+晶体) |
W3(容器+无水硫酸铜) |
|
5.4g |
7.9g |
6.8g |
请写出结晶水含量(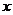 %)的计算公式(用W1、W2、W3表示)
%)的计算公式(用W1、W2、W3表示)
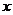 %=
该生测定结果是偏高还是偏低?
。
%=
该生测定结果是偏高还是偏低?
。
从下列分析中选出该学生产生实验误差的原因可能(填写字母) 。
(A)加热前称量时容器未完全干燥
(B)最后两次加热后的质量相差较大(大于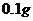 )
)
(C)加热后容器未放入干燥器中冷却
(D)加热过程中晶体有少量溅失

(3)从下列仪器中选出实验所需的仪器(用字母序号填写) ,还需要的仪器是
。
A. 托盘天平 B. 研钵 C. 试管夹 D. 酒精灯 E. 蒸发皿 F. 玻璃棒 G. 坩埚
H. 干燥器 I. 石棉网 J. 三脚架
(4)晶体中如果含有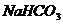 杂质,测得的结晶水含量会
;晶体脱水后,如果没有在干燥器内而在空气中冷却,测得的结晶水含量会 (填偏高或偏低)。
杂质,测得的结晶水含量会
;晶体脱水后,如果没有在干燥器内而在空气中冷却,测得的结晶水含量会 (填偏高或偏低)。
10. 人体血液里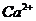 离子的浓度一般采用
离子的浓度一般采用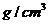 来表示。今抽一血样
来表示。今抽一血样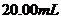 ,加适量的草酸铵
,加适量的草酸铵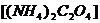 溶液,可析出草酸钙(
溶液,可析出草酸钙(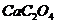 )沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(
)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(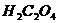 ),再用
),再用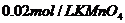 溶液滴定,使草酸转化成
溶液滴定,使草酸转化成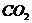 逸出,这时共消耗
逸出,这时共消耗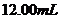
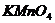 溶液。试回答:
溶液。试回答:
(1)滴定时,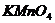 溶液应装在 滴定管中,操作时,左手 ,右手
溶液应装在 滴定管中,操作时,左手 ,右手
,眼睛注视 。
(2)草酸跟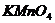 反应的离子方程式为:
反应的离子方程式为: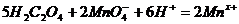
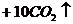
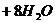 则式中的
则式中的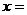 。
。
(3)滴定时,根据现象 ,即可确定反应达到终点。
(4)经过计算,血液样品中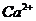 离子的浓度为 mg/cm3。
离子的浓度为 mg/cm3。
9. 测定碳酸钠晶体中结晶水的含量,至少要在天平上进行四次称量。回答下列问题:
(1)第一次称量的是 的质量,第二次称量的是 的质量,第三次称量的是
的质量,第四次称量的是 的质量。
8. 下图是用0.1mol/L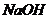 溶液中和某浓度
溶液中和某浓度 溶液时,溶液的
溶液时,溶液的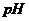 值变化的曲线。依此求:
值变化的曲线。依此求:
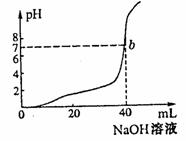
(1) 溶液的物质的量浓度 。
溶液的物质的量浓度 。
(2)滴定到 点,溶液的总体积约为
点,溶液的总体积约为 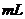 。
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com