
23.将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应
3A(g)+B(g) xC(g)+2D(g),经过4min时,测得D的浓度为0.5 mol/L
xC(g)+2D(g),经过4min时,测得D的浓度为0.5 mol/L
c(A):c(B)=3:5,C的反应速率是0.125 mol·L-1·min-1,
求:(1)A在4 min末的浓度;
(2)x的值。
辽宁省沈阳二中09-10学年高一下学期4月月考
22.(8分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成一种环境无害气体和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
21.(12分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为 (填元素符号)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 (填化学式)
(3)①、④、⑤中的元素可形成既含离子键又含极性共价键的化合物,写出化合物的电子式:
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.Na2SO3 c.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
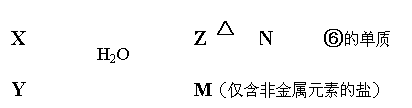

X溶液与Y溶液反应的离子方程式为
N→⑥的单质的化学方程式为
20.(10分)已知热化学方程式:
Mg(OH)2(s)=MgO(s)+H2O(g); △H1=+81.5kJ·mol-1
Al(OH)3(s)=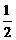 Al2O3(s)+
Al2O3(s)+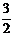 H2O(g); △H2=+87.7kJ·mol-1
H2O(g); △H2=+87.7kJ·mol-1
其中,氧化镁熔点2852℃;氧化铝熔点2050℃ (1)Mg(OH)2和Al(OH)3起阻燃作用的主要原因是
(2)等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
原因是
(3)常用阻燃剂主要有三类:A.卤系,如四溴乙烷(熔点0℃,沸点:243.5℃);B.磷系,如磷酸三苯酯(熔点48.5℃,沸点370℃);C.无机类,主要是Mg(OH)2和Al(OH)3。从环保的角度考虑,应用时较理想的阻燃剂是 (填代号),理由是
19.(10分)几种短周期元素的原子半径及某些化合价见下表:
|
元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
|
化合价 |
–1 |
–2 |
+4、–4 |
+4、–2 |
+5、–3 |
+3 |
+2 |
+1 |
|
原子半径/nm |
0.071 |
0.074 |
0.077 |
0.102 |
0.110 |
0.143 |
0.160 |
0.186 |
分析上表中有关数据,并结合已学过的知识,回答以下问题。涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中位于 周期, 族;
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
(3)A与J所形成化合物中的化学键类型是 用电子式表示其形成过程
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
18.右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
|
|
|
||
|
X |
|
|
|
|
W |
Y |
|
R |
|
|
|
Z |
|
A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强
第Ⅱ卷 (非选择题,共46分)
17.已知反应: ①2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.1L1 mol/L稀硫酸与足量稀NaOH溶液反应的中和热为57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量
16.如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是
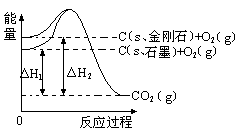
A. 石墨和金刚石的转化是物理变化
B. 石墨的稳定性弱于金刚石
C. C(s、石墨)= C(s、金刚石) △H= +1.9 kJ•mol-1
D. 石墨的总键能比金刚石的总键能小1.9 kJ•mol-1
15.25℃,101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量.下列表示该反应的热化学方程式中正确的是 A.CH4O(l)+3/2O2(g) = CO2(g)+2H2O(l);△H=-725.8kJ/mol B.2CH4O(l)+3O2(g)= 2CO2(g)+4H2O(l);△H=+1451.6kJ/mol C.2CH4O+O2 = 2CO2+4H2O(l);△H=-22.68kJ/mol D. CH4O(l)+3/2O2(g) = CO2(g)+2H2O(g);△H=-725.8kJ/mol
14.有X、Y两种主族元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
A.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
B.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
C.若X(OH)n为强碱,则Y(OH)n也一定为强碱
D.若Y的最高正价为+ m,则X的最高正价一定为+ m
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com