
18.(2009·厦门模拟)“探险队员”--盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。
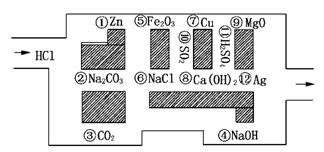
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)。________________________________________________________________________。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,属于氧化还原反应的有________个,其中能“吃掉”盐酸的盐是________,写出该反应的离子方程式________________________________________________________________________
________________________________________________________________________。
(3)在不能与盐酸反应的物质中,属于电解质的是________(填写物质序号),属于非电解质的是________。
(4)如果将盐酸换成氯气,它能沿着盐酸走出的路线“走出”这个迷宫吗?为什么?
________________________________________________________________________。
解析:(1)图中物质③、⑥、⑩、⑦、⑪、⑫均不与盐酸反应,沿该路线可走出迷宫。
(2)盐酸与NaOH、Ca(OH)2的反应属于酸和碱中和反应,与Zn的反应属于氧化还原反应,能“吃掉”盐酸的盐是Na2CO3,该反应的离子方程式为CO+2H+===CO2↑+H2O。
(3)在不能与盐酸反应的物质中,属于电解质的是H2SO4、NaCl,属于非电解质的是CO2、SO2。
(4)如果将盐酸换成氯气, 它沿着盐酸走出的路线不能“走出”这个迷宫,因为氯气或氯水有强氧化性,遇到二氧化硫、铜时都会发生氧化还原反应从而被“吃掉”。
答案:(1)③⑥⑩⑦⑪⑫
(2)2 1 Na2CO3 CO+2H+===CO2↑+H2O
(3)⑥⑪ ③⑩
(4)不能,因为氯气或氯水有强氧化性,遇到二氧化硫、铜时都会发生氧化还原反应从而被“吃掉”
17.(2009·广州河田中学高三月考)A、B、C三只烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:
(1)分别写出三只烧杯中形成分散系的名称:A________,B________,C________。
(2)写出A中形成分散系的离子方程式___________________________________。
(3)写出C中形成分散系的化学方程式__________________________________。
解析:FeCl3溶液滴入NaOH溶液中,发生反应:Fe3++3OH-===Fe(OH)3↓,形成悬浊液;FeCl3溶液滴入KSCN中,发生络合反应,生成血红色溶液;FeCl3溶液滴入煮沸的蒸馏水中,发生反应:FeCl3+3H2O(沸水)Fe(OH)3(胶体)+3HCl。
答案:(1)悬浊液 溶液 胶体
(2)Fe3++3OH-===Fe(OH)3↓
(3)FeCl3+3H2O(沸水)Fe(OH)3(胶体)+3HCl
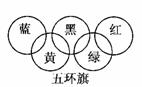
16.(思维拓展题)假定奥运五环旗中的每一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应。且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是 ( )
|
选项 |
蓝 |
黑 |
红 |
黄 |
绿 |
|
A |
SiO2 |
CuSO4 溶液 |
O2 |
NaOH溶液 |
Ag |
|
B |
O2 |
稀H2SO4 |
CO2 |
Fe |
NaOH溶液 |
|
C |
O2 |
稀H2SO4 |
Al(OH)3 |
NH3 |
NaOH溶液 |
|
D |
Mg |
CO2 |
KOH溶液 |
Al |
Fe2O3 |
答案:B
15.某化学兴趣小组欲研究H2SO4、NaCl、KCl、Na2CO3、FeCl3、NaOH的性质,对于如何研究,他们设计了两种研究方案:
方案1:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验。
方案2:将它们按照钠盐、钾盐、铁盐和其他化合物分类,然后分别溶于水得到溶液,进行实验。
下列说法正确的是 ( )
A.按照方案1属于碱的有Na2CO3、NaOH
B.按照方案2属于钠盐的有NaCl、Na2CO3、NaOH
C.方案1中的碱与方案2中的铁盐反应可得到一种红褐色胶体
D.设计方案2的同学另取某种溶液,在其中加入上述溶液中的钾盐溶液有白色沉淀产生,加入稀硝酸沉淀不消失,则该溶液中一定含有Ag+
答案:D
14.下列有关分散系的说法正确的是 ( )
A.根据能否发生丁达尔效应将分散系分为浊液、溶液和胶体
B.在Fe(OH)3胶体中加入过量盐酸不溶解
C.“血液透析”原理同溶液中固体颗粒的过滤原理相似
D.除加入电解质可使胶体聚沉外,将两种带相反电荷胶粒的胶体混合也能发生聚沉
答案:D
13.下列关于胶体和溶液的说法中,正确的是 ( )
A.胶体不均一、不稳定,静置后易产生沉淀;溶液均一、稳定,静置后不产生沉淀
B.布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分开
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.只有胶状物如胶水、果冻类的物质才能称为胶体
答案:C
12.(2009·广州)将某些化学知识用数轴表示,具有直观形象、简明易记的优点。下列用数轴表示的化学知识中不正确的是 ( )
A.分散系的分类:
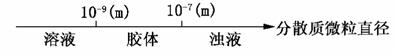
B.AlCl3和NaOH溶液反应后铝元素的存在形式:
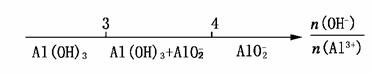
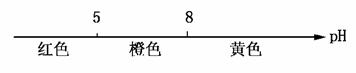
C.常温下甲基橙的变色范围:
D.CO2与NaOH溶液反应的产物:
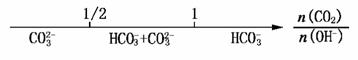
解析:

答案:C
11.(2009·广东)下列说法都正确的是 ( )
①江河入海口三角洲的形成通常与胶体的性质有关 ②四川灾区重建使用了大量钢材,钢材是合金 ③“钡餐”中使用的硫酸钡是弱电解质 ④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 ⑤常用的自来水消毒剂有氯气和二氧化氯,两者都含有极性键 ⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物
A.①②③④ B.①②④⑥
C.①②⑤⑥ D.③④⑤⑥
解析:硫酸钡为强酸强碱盐,属强电解质,Cl2是由非极性键形成的分子,故③⑤说法错误。
答案:B
10.(2009·全国卷Ⅱ)下列关于溶液和胶体的叙述,正确的是 ( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
解析:A项:胶体中胶体粒子可能带电,但胶体仍为电中性;B项:对于某些溶液如蔗糖溶液,其溶质粒子不带电荷;C项:布朗运动是所有分散系中分散质粒子都具有的规律。
答案:D
9.(2009·福建福州一中高三月考)下列关于氧化物的叙述正确的是 ( )
A.酸性氧化物都可以跟强碱溶液反应
B.与水反应可生成酸的氧化物都是酸性氧化物
C.金属氧化物都是碱性氧化物
D.不能跟酸反应的氧化物一定能和碱反应
解析:可以和碱反应只生成盐和水的化合物称为酸性氧化物,所以酸性氧化物都可以和强碱反应,A项正确;二氧化氮可以和水反应生成酸,但它不是酸性氧化物,B项错误;Mn2O7是金属氧化物,但不是碱性氧化物,C项错误;CO不跟酸反应,但也不和碱反应,D项错误。
答案:A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com