
7.下列关于元素周期表的说法正确的是 ( )
A.能生成碱的金属元素都在ⅠA族
B.元素周期表有18个纵行,分列16个族,即8个主族和8个副族。
C.稀有气体元素原子的最外层电子数均为8
D.原子序数为14的元素位于元素周期表的第3周期ⅣA族
6.下列分子中所有原子都满足最外层为8电子结构的是 ( )
A.BF3 B.H2O
C.SiCl4 D.PCl5
5. 下列混合物,能用分液漏斗分离的是 ( )
A. 乙酸乙酯和水 B. 酒精和水 C. 植物油和乙醇 D. 汽油和煤油
4.下列对有机物结构的叙述中不正确的是 ( )
A.硝基、羟基、氯原子、苯环、甲基都是官能团
B.邻二氯苯不存在同分异构体说明苯分子中6个碳原子之间的键是完全一样的
C.乙烯、苯分子中所有原子共平面
D.CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构
3. 某有机物的结构为 , 这种有机物不可能具有的性质是 ( )
A.能使酸性KMnO4溶液褪色 B.能发生酯化反应
C.能发生水解反应 D.能跟NaOH溶液反应
2.下列过程属于物理变化的是 ( )
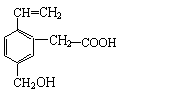 A. 由乙烯变为聚乙烯 B.蛋白质盐析 C.O2转变为O3 D.皂化反应
A. 由乙烯变为聚乙烯 B.蛋白质盐析 C.O2转变为O3 D.皂化反应
1.正确掌握化学用语是学好化学的基础。下列化学用语中正确的是 ( )
A.乙烯的结构简式为CH2CH2 B.羟基的电子式: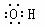
C.Ca2+的结构示意图为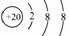 D .乙醇的分子式:CH3CH2OH
D .乙醇的分子式:CH3CH2OH
11.下列说法正确的是(NA表示阿伏加德罗常数) ( )
⑴常温常压下,1mol氮气含有NA个氮分子
⑵标准状况下,以任意比例混合的甲烷和丙烷混合气体22.4L,所含的气体的分子数约为NA个
⑶标准状况下,22.4LNO和11.2L氧气混合,气体的分子总数约为1.5NA个
⑷将NO2和N2O4分子共NA个降温至标准状况下,其体积为22.4L
⑸常温下,18g重水所含中子数为10NA个
⑹常温常压下,1mol氦气含有的核外电子数为4NA
⑺常温常压下,任何金属和酸反应,若生成2g 氢气,则有2NA电子发生转移
⑻标准状况下,1L辛烷完全燃烧后,所生成气态产物的分子数为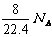
⑼31g白磷分子中,含有的共价单键数目是NA个
⑽1L1 mol•L-1的氯化铁溶液中铁离子的数目为NA
[点拨]⑴正确,1mol氮气的分子数与是否标准状况无关。
⑵正确,任意比例混合的甲烷和丙烷混合气体 22.4L,气体的总物质的量为1mol,因此含有NA个分子。
⑶不正确,因为NO和氧气一接触就会立即反应生成二氧化氮。
⑷不正确,因为存在以下平衡:2NO2 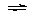 N2O4(放热),降温,平衡正向移动,分子数
N2O4(放热),降温,平衡正向移动,分子数
少于1mol,标准状况下,其体积小于22.4L
⑸不正确,重水分子(D2O)中含有10个中子,相对分子质量为 20,18g重水所含中子数为:10×18g/20g· mol-1=9mol。
⑹正确,1个氦原子核外有4个电子,氦气是单原子分子,所以1mol氦气含有4mol
电子,这与外界温度和压强无关。
⑺正确,不论在任何条件下,2g氢气都是1mol,无论什么金属生成氢气的反应均可表示为:2H++2e=H2↑,因此,生成1mol氢气一定转移 2mol电子。
⑻不正确,标准状况下,辛烷是液体,不能使用标准状况下气体的摩尔体积22.4L/mol这一量,所以1L辛烷的物质的量不是1/22.4mol。
⑼不正确,白磷分子的分子式为P4,其摩尔质量为124g/mol,31g白磷相当于0.25mol,
白磷的分子结构为正四面体,一个白磷分子中含有6个P-P共价键,所以,0.25mol白磷中含有1.5NA个P-P共价键。
⑽不正确,Fe3+在溶液中水解。
10.设NA表示阿伏加德罗常数,下列叙述中正确的是( C H K )
A.1/18mol的1H35Cl分子所含中子数约为6.02×1023
B.标准状况下,1L辛烷完全燃烧后,所生成气体产物的分子数为8NA/22.4
C.常温常压下,20 g D2O和足量的金属钠反应产生气体的分子数为0.5 NA
D.常温常压下,3l g白磷分子中的共价键数为6NA
E. 在25℃时,1 L纯水中含H+的个数为10-7NA
F.500mLl.0mol/L的乙酸溶液中含有的H+数为0.5NA
G.1 molFeCl3制成胶体,所得胶体的粒子数为NA
H.在电解食盐水的实验中,测得电解后溶液的pH为14,又知电解后溶液总体积为1L,则阴极析出的气体的分子数为0.5NA
I.标况下22.4L乙醇所含的分子数必定为NA
J.标准状况下22.4LSO3含有NA个SO3分子 K.60g二氧化硅中含有4NA个Si-O键 L.1.9gD3O+中含有1.1NA个质子 M.1molCL2通入热的NaOH溶液中(主要产物是NaCl、NaClO3),充分反应后,转移电子数 为NA个
9.设NA为阿伏加德罗常数值,下列叙述中不正确的是( B )
A.12.4g白磷晶体中含有的P-P键数是0.6NA
B.2.9g2CaSO4·H2O 含有的结晶水分子数为0.02 NA
C.100 g的98%的浓 H2SO4中所含的硫原子数为2NA
D.2molSO2和1molO2 混合在V2O5存在的条件下密闭容器中加热反应后,容器内物质分子数大于2 NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com