
2.下列生物中,除细胞膜外几乎不含磷脂分子的有 ( )
①乳酸菌 ②变形虫 ③肺炎双球菌 ④蓝藻 ⑤酵母菌
A.②③⑤ B.②③④ C.①③④ D.①④⑤
1.下列不属于叶绿体基质成分的是 ( )
A.可溶性蛋白质 B.核酸 C.光合色素 D.核糖体
18.(2008·东营模拟)加热0.04 mol KMnO4固体,一段时间后,收集到a mol单质气体,此时KMnO4的分解率为x,在反应后的残留固体中加入过量的浓HCl并加热,充分反应后又收集到b mol单质气体,设Mn元素全部以Mn2+存在于反应后的溶液中。
(1)a+b=________(用x表示)。
(2)当x=________时(a+b)取最小值,且最小值为________。
(3)当a+b=0.09时,0.04 mol KMnO4加热后所生成残留固体的质量为________。
解析:n(O2)可由2KMnO4K2MnO4+MnO2+O2↑求得,a=0.02x mol。
由2KMnO4+16HCl===2MnCl2+2KCl+5Cl2↑+8H2O;
K2MnO4+8HCl===MnCl2+2KCl+2Cl2↑+4H2O;
MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
可求得n(Cl2),
b=0.04(1-x) mol×5/2+0.04x mol+0.04x mol/2
=(0.1-0.04x) mol
(1)n(O2)+n(Cl2)=a+b=0.02x mol+0.1 mol-0.04x mol/2
=(0.1-0.02x) mol
(2)在上述推得的数学关系式a+b=0.1-0.02x中,x为分解率。由0<x<100%和数学极值原理可求得:0.08<a+b<0.1,即KMnO4完全分解(x=100%)时,a+b值最小为0.08。
(3)当a+b=0.09时,求得x=50%,由高锰酸钾分解反应式得:n(O2)=0.01 mol,则由质量守恒定律知:加热后剩余固体的质量等于原KMnO4,质量与放出O2质量的差,m(剩)=0.04 mol×158 g·mol-1-0.01 mol×32 g·mol-1=6g。
答案:(0.1-0.02x) (2)100% 0.08 (3)6 g
17.某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答下列问题。
该小组设计的简单实验装置如图所示:
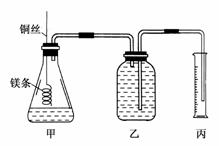
该实验的主要操作步骤如下:
①配制100 mL 1.0 mol·L-1的盐酸溶液;
②用________(填仪器名称并注明规格)量取10.0 mL 1.0 mol·L-1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)用文字表述实验步骤 ④中检查装置气密性的方法:
④中检查装置气密性的方法:
________________________________________________________________________
________________________________________ ________________________________。
________________________________。
(2)实验步骤⑤中应选用________(填序号)的量筒。
A.100 mL B.200 mL C.500 mL
读数时除恢复到室温外,还要注意________________________________________。
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm=________,若未除去镁条表面的氧化膜,则测量结果________(填“偏大”、“偏小”或“无影响”)。
解析:本题以化学计量和化学实验基础知识为背景,通过化学实验的形式考查气体摩尔体积的测定,探究实验中出现的问题,符合当前新课改的探究理念。
考虑到②10 mL量筒的精确度是0.1 mL,故应用10 mL量筒;③因HCl的物质的量为0.01 mol,由反应Mg+2HCl===MgCl2+H2↑知,HCl可与0.005 mol Mg完全反应,为保证HCl完全反应,故镁应不少于0.005 mol×24 g/mol=0.12 g。
(1)本装置可与初中化学制氢气的装置联系,用微热的方法检查装置的气密性。
(2)实验中产生的气体在标准状况下的体积为0.005 mol×22.4 L/mol=0.112 L=112 mL,考虑到室温时气体的体积稍大些,再考虑通常仪器规格应略大且越接近,误差越小,故选B。读数时注意量筒内的液面与集气瓶中液面相平,保证气压相等。
(3)Vm是气体的体积(排出水的体积)与气体的物质的量之比。若未除去表面的氧化膜,导致氧化膜耗酸,从而放出H2的体积变小,则Vm偏小。
答案:②10 mL量筒 ③0.12
(1)两手掌紧贴锥形瓶外壁一会儿,如果观察到广口瓶中长导管内有一段水柱高出液面,表明装置气密性良好。
(2)B 量筒内的液面与集气瓶内液面相平
(3)0.2V L·mol-1 偏小
16.在标准状况下,由CO和CO2组成的混合气体6.72 L,质量为12 g。此混合物中CO和CO2物质的量比是________,CO的体积分数是________,CO的质量分数是________,C和O原子个数比是________,混合气体的平均相对分子质量是________,对氢气的相对密度是________。
答案:1:3 25% 17.5% 4:7 40 20
15.(2009·全国卷Ⅱ)下列叙述中正确的是 ( )
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1?2
C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出
解析:A项中CaCO3+CO2+H2O===Ca(HCO3)2不是可逆反应;B项:等物质的量的Na2CO3与盐酸反应生成NaHCO3(无CO2生成);C项:应为等物质的量的NaHCO3、Na2CO3分别与足量盐酸反应生成CO2的物质的量相同,D项:因生成的NaHCO3溶解度比Na2CO3小,故会结晶析出。
答案:D
14.(2009·江苏)用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2 NA
B.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA
 C.室温下,21.0 g乙烯和
C.室温下,21.0 g乙烯和 丁烯的混合气体中含有的碳原子数目为1.5 NA
丁烯的混合气体中含有的碳原子数目为1.5 NA
D.标准状况下,22.4 L甲醇中含有的氧原子数为1.0 N A
A
解析:A项c(OH-)=mol·L-1=0.1 mol·L-1,故1.0 L溶液中n(OH-)=0.1 NA;B项Cl2+2NaOH===NaCl+NaClO+H2O,每1 mol Cl2参与反应电子转移数目为1 mol,故B项中电子转移数目为0.1 NA;D项中CH3OH在标准状况下不是气态物质。
答案:C
13.(2009·福建)设NA为阿伏加德罗常数,下列叙述正确的是 ( )
A.24 g镁原子的最外层电子数为NA
B.1 L 0.1 mol·L-1乙酸溶液中H+数为0.1 NA
C.1 mol甲烷分子所含质子数为10NA
D.标准状况下,22.4 L乙醇的分子数为NA
解析:A中Mg: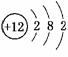 ,故24 g镁即1 mol镁最外层有2NA电子。
,故24 g镁即1 mol镁最外层有2NA电子。
B中:乙酸为弱酸,部分电离,故最终H+数远小于0.1NA。
C中:1个CH4分子中含10个质子,故C项正确。
D中:标准状况下,乙醇为液体,不能使用气体摩尔体积。
答案:C
12. (2009·广东)设nA代表阿伏加德罗常数(NA)的数值,下列说法正确的是 ( )
(2009·广东)设nA代表阿伏加德罗常数(NA)的数值,下列说法正确的是 ( )
A.1 mol硫酸钾中阴离子所带电荷数为nA
B.乙烯和环丙烷(C3H6)组成的28 g混合气体中含有3nA个氢原子
C.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为nA
D.将0.1 mol氯化铁溶于1 L水中,所得溶液含有0.1 nA个Fe3+
解析:乙烯和环丙烷的最简式(实验式)均为CH2,故28 g两者的混合物含4 nA个氢原子;FeCl3溶于水后因Fe3++3H2OFe(OH)3+3H+,0.1 mol FeCl3溶于水后,所得溶液中Fe3+小于0.1 nA个。
答案:C
11.(2009·天津二模5月)下列说法正确的是 ( )
①标准状况下,22.4 L己烯含有的分子数为6.02×1023
②标准状况下,a L的氧气和氮气和混合物含有的分子数约为×6.02×1023 ③7.1 g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.2×6.02×1023 ④60 g SiO2晶体中含有2×6.02×1023个Si-O键 ⑤1 mol乙醇中含有的共价键数约为7×6.02×1023 ⑥500 mL 1 mol·L-1的硫酸铝溶液中含有的硫酸根离子数约为1.5×6.02×1023
A.①④ B.②⑥
C.③⑤ D.②⑤
解析:①标准状况下己烯为液体;③7.1 g Cl2为0.1
mol,与NaOH反应时只有全部变为Cl-时,转移电子数才为0.2×6.02×1023,而Cl2与NaOH反应时不可能全部变为Cl-;④60 g SiO2中应有Si-O键4×6.02×1023个,因为一个Si原子可形成4个Si-O键;⑤乙醇的结构式为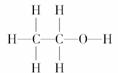 ,应含有8×6.02×1023个共价键。②⑥正确。
,应含有8×6.02×1023个共价键。②⑥正确。
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com