
9.某国议会通过对政府的不信任案时,政府就得辞职或呈请 国家元首解散议会,重新选举,则该国政体肯定不是
国家元首解散议会,重新选举,则该国政体肯定不是
A.议会制共和制 B.议会制君主立宪制 C.民主共和制 D.总统制共和制
随着互联网的快速发展,以网络为媒介的“政府-民间”互动模式已成为我国政治文明的重要元素。回答7-8题。
7.按照《中华人民共和国政府信息公开条例》的要求,行政机关应将主动公开的政府信息,通过政府公报、政府网站、新闻发布会以及报刊、广播、电视等方式公开。这有利于
①增强政府工作的透明度 ②维护和实现公民的知情权
③扩大政府公共服务职能 ④发挥舆论的法律监督作用
A.①② B. ①③ C. ③④ D.②④[
8.“政府-民间”互动模式
①方便了公民直接管理国家事务 ②保障了人民群众对政府的质询权
③拓宽了公民参与民主监督的渠道 ④有利于政府了解民意和汇集民智
A.①② B.②③ C.①④ D.③④
6.我国积极实施“走出去”战略
①是解决我国资金短缺的根本性措施 ②是积极参与国际竞争的具体表现
③可以充分利用国际资源和国际市场发展自己 ④可以减少出口贸易摩擦
A.①② B.②③ C.②③④ D.①②③④
5.世界贸易组织制定了一系列促进世界贸易发展的原则,其中最重要的原则包括
①互惠原则 ②最惠国待遇原则 ③市场准入原则 ④国民待遇原则
A.①③ B.②③ C.②④ D.③④
读下面的人民币外汇牌价表,回答3-4题。
|
时间 |
美元 |
人民币 |
|
2008年3月5日 |
100 |
711.75 |
|
2010年3月5日 |
100 |
682.65 |
3.上述现象表明
A.外汇汇率升高,人民币币值下降 B.外汇汇率降低,人民币币值上升
C.外汇汇率升高,人民币币值上升 D.外汇汇率降低,人民币币值下降
4.上述变化可能带来的影响有
①我国公民出国留学的成本降低 ②单位人民币的购买力下降
③削弱我国出口商品的竞争力 ④海外对华投资增加
A.②③ B.①③ C.①②③ D.①②④
2.人们的消费受相关商品价格变动的影响,如果A商品和B商品的关系如下表,则B商品中①②的需求量应分别是 、 ,这时,生产者、经营者一般会_______
|
关系 |
A商品 |
B商品 |
|
互补商品 |
价格下跌 |
① |
|
互为替代品 |
价格上涨 |
② |
A.增加 减少 调节生产 B.增加 增加 提高诚信意识
C.减少 增加 降低价格 D.增加 增加 增加供应量
1.为克服当前金融危机的影响,许多国家实行宽松的货币政策,增加纸币发行量,向金融机构注资,引发了人们对通货膨胀的担忧。是否发生了通货膨胀,必须看是否出现:
①流通中实际需要的货币量超过纸币的发行量 ②商品价格全面、持续上涨
③国家发行新的纸币 ④物价总水平不断上涨使居民购买力普遍下降
A. ① B. ②④ C. ①②③ D. ②③④
4.Al(OH)3的用途:由于Al(OH)3具有吸附性,既能凝聚水中悬浮物,又能吸附色素,因此Al(OH)3可作净水剂和色素吸附剂。
[例2]使溶液中Ba2+、Mg2+、Al3+、Ag+、Cu2+分步逐一沉淀析出,加入下列试剂的顺序正确的是 ( )
A.NaCl→Na2S→Na2SO4→NaOH→HNO3 B.H2SO4→HCl→H2S→NaOH→CO2
C.HCl→H2SO4→H2S→NaOH→CO2 D.Na2S→Na2SO4→NaCl→NaOH→HCl
[解析]SO42-能同时除去Ba2+和Ag+,S2-能同时除去Ag+和Cu2+,所以不能放在第一位,排除BD;AC相比,在加入前四种试剂后,Al3+以AlO2-形式存在,加酸可使AlO2-以Al(OH)3形式沉淀。但HNO3量 不好控制,所以最好的选项为C。
[答案]C
[规律总结]解除杂题应注意①除杂试剂的选择。本题要求将离子分步逐一除去,所以试剂要一一对应:Ba2+-SO42-,Mg2+-OH-,Ag+-Cl-,Cu2+-S2-,②除杂的顺序。为了将杂质除干净,除杂试剂一般是过量的,这样势必引入新杂质。所以后续的除杂试剂在去除对应杂质的同时,还要有将前一过量除杂试剂清除的作用。
考点3 镁和铝的图像
|
基本坐标图像 |
实验现象及反应原理 |
衍生坐标图像 |
化学反应原理 |
 |
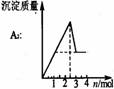
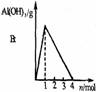
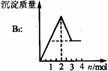
铝盐溶液与强碱反应 现象: 。 原理: |
 |
 |
 |
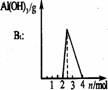
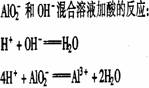
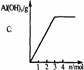
铝酸盐溶液与强酸反应 现象: 。 原理: |
 |
 |
|
|
|
 |
 |
 |
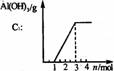
铝盐溶液与弱碱反应 现象: 。 原理: |
 |
 |
 |
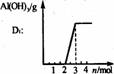
铝酸盐溶液与弱酸反应 现象: 。 原理: |
 |
 |
[例3]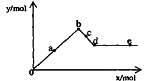 (2006年上海)已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系。下列有关叙述正确的是
( )
(2006年上海)已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系。下列有关叙述正确的是
( )
A.a-b时沉淀的物质的量:A1(OH)3比BaSO4多
B.c-d时溶液中离子的物质的量:AlO2–比Ba2+多
C.a-d时沉淀的物质的量:BaSO4可能小于A1(OH)3
D.d-e时溶液中离子的物质的量:Ba2+可能等于OH–
[解析]采用定量法分析。假设有1molA12(SO4)3则溶液中含有2molA13+、3molSO42–。向溶液中逐滴加入Ba(OH)2溶液时发生的反应为:Al3++3OH- Al(OH)3↓、SO42–+Ba2+
Al(OH)3↓、SO42–+Ba2+
BaSO4↓。则当2molA13+完全沉淀时,消耗Ba(OH)23mol,此时3molSO42–全部沉淀;生成沉淀为2molAl(OH)3和3molBaSO4共5mol,因此,在整个反应过程中BaSO4的物质的量始终大于Al(OH)3的物质的量;再加入Ba(OH)2溶液时发生Al(OH)3+OH-=[Al(OH)4] -,沉淀的量将逐渐减少,因此b点是沉淀的最大值,b-d中Al(OH)3沉淀逐渐溶解转化为Ba(AlO2)2,由于AlO2-微弱水解,因此再b-d中AlO2-的物质的量大于Ba2+;d点时Al(OH)3沉淀恰好完全溶解,此时溶液中只存在Ba(AlO2)2,因此随Ba(OH)2的加入在某一点,当d-e中加入的Ba(OH)2的物质的量等于Ba(AlO2)2的物质的量时,溶液中Ba2+与OH-的量相等。
[答案]BD
[规律总结]析图或作图时不仅要注意加入酸或碱的强弱,而且要注意所加入的量或滴加顺序,正因滴加顺序不同可产生的现象不同。若产生沉淀有多种,则应细细分析相关量间的关系。要持别关注沉淀是否同步完全,沉淀物是否溶于所加入的过量试剂中,同时要注意纵生标的物理量意义。对于一些复杂问题可先分解后组合,进行图像的叠加工作。抓住一些关键点(如最高点,最低点,转折点)和变化趋势,才能较顺利地解决图像问题。
3.Al(OH)3的制取
①铝盐与碱反应:实验室制取氢氧化铝时采用过量的氨水,而不用强碱与可溶性铝盐溶液反应是因为 。
②四羟基合铝酸盐与酸反应:一般用向偏铝酸盐溶液中通入CO2的方法制取Al(OH)3。
当CO2不足或适量时: ;(填离子反应方程式,下同)CO2过量时: 。
|
[特别提醒]:(1)制取Al(OH)3也可用铝盐与强碱作用,但应严格控制加入碱的量,因为强碱过量会使制得的Al(OH)3转化为四羟基合铝酸盐:Al(OH)3+OH-=[Al(OH)4]-。 (2)一般不用强酸,因为强酸的量控制不当会使制得的Al(OH)3溶解:[Al(OH)4] -+H+=Al(OH)3↓+H2O;Al(OH)3+3H+=Al3++3H2O。 |
2.化学性质
①与酸反应:Al(OH)3 +3HCl=AlCl3+3H2O(离子反应方程式: )
②与碱反应:Al(OH)3+NaOH=Na[Al(OH)4](离子反应方程式: )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com