
3.下列说法正确的是 AC
A.s区元素都是主族元素 B.s区元素都是金属元素
C.0族元素在p区 D.所有非金属元素都在p区
s区元素包含ⅠA、ⅡA两族元素,除H外都是金属元素,p区元素包含ⅢA-ⅦA和0族元素,除H外,所有非金属元素都在p区。
2.(2007·威海模拟)目前,人类已经发现的非金属元素除稀有气体元素外共有16种,下列对这16种非金属元素的判断正确的有B
A.都是主族元素,最外层电子数都大于或等于3
B.部分非金属单质在发生反应时既可被氧化也可被还原
C.氢化物常温下都是气态,所以又叫气态氢化物
D.氧化物常温下都可以与水反应生成酸
1.关于非金属元素N、O、Cl、P的叙述,正确的是C
A.在通常情况下其单质均为气体 B.其单质均由双原子分子构成
C.都属于主族元素 D.每种元素仅生成一种氢化物
18.(1)C+2H2SO4(浓)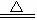 2SO2↑十CO2↑十2H2O↑
2SO2↑十CO2↑十2H2O↑
(2)④→②→①→③
(3)验证产物气流中是否有SO2将SO2全部氧化吸收确证产物中SO2已被B瓶溶液全部氧化
(4)无水CuSO4(或变色硅胶)水蒸气由于产物气流通过①、③时会带出水蒸气,所以②必须在①、③之前
(5)澄清石灰水CO2
解析:木炭与浓硫酸加热反应,生成CO2和SO2。CO2和SO2都跟澄清石灰水中的Ca(OH)2反应,生成CaSO3和CaCO3使澄清石灰水变浑浊,这相互干扰鉴别。在SO2、CO2混合气体中,首先用品红可检查SO2存在,然后将SO2氧化去除,再用澄清石灰水检验CO2的存在。
点评:品红是鉴别SO2的试剂,CO2不与品红作用。CO2和SO2在化学性质上有许多相似处:都是酸性氧化物;都能溶于水得酸;都与Ca(OH)2反应生成沉淀,通入过量的CO2或SO2时,生成的CaCO3、CaSO3沉淀溶解,变成Ca(HCO3)2、Ca(HSO3)2,溶液重新变澄清。CO2中“C”为高价,SO2中“S”为中间价,都可被还原为低价,因此,CO2、SO2有氧化性。
17.D解析:Cu与稀硫酸不反应,在加热条件下铜和浓硫酸发生反应的化学方程式为:
Cu+2H2SO4(浓) CuSO4+SO2↑十2H2O
CuSO4+SO2↑十2H2O
参加反应的H2SO4有一半被还原,在Cu与浓H2SO4的反应过程中,浓硫酸浓度逐渐降低,变成稀H2SO4时反应会停止,所以0.9molH2SO4与足量铜片反应时,被还原的H2SO4小于0.45mol。
点评:浓度不同,发生的化学反应不同,在具体分析、计算时应注意。
16.C 解析:A.Cu-4HNO3(浓)-Cu(NO3)2-2NO2
B.Cu-HNO3(稀)-Cu(NO3)2-NO
C.CuO-2HNO3-Cu(NO3)2-H2O
由以上关系式可以看出:C.既节约原料,同时又不产生有毒气体。D.成本太高亦不可采用。故C为最好的办法。
15.D解析:应用守恒法,反应中消耗的HNO3的物质的量应是转化成Cu(NO3)2和生成的NO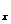 (NO和NO2)气体中N原子的物质的量之和:即
(NO和NO2)气体中N原子的物质的量之和:即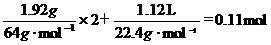 ,故答案选D。
,故答案选D。
14.C解析:铜与稀硫酸不反应,但加入KNO3后,由于溶液中有H+存在,故会发生如下反应:
3Cu+8H++2NO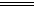 3Cu+2NO↑+4H2O。
3Cu+2NO↑+4H2O。
加入Fe2(SO4)3,也会使铜粉的质量减少,但无气体逸出,故答案选C。
13.A解析:B.王水指的是浓HNO3和浓盐酸按溶液体积之比为1:3所得的混合物。
C.硝酸与金属反应时,被还原的一般是指+5价氮,得到的还原产物是NO2、NO、N2O或N2等。
D.常温下,浓HNO3可使Fe和Al等金属发生钝化现象,故B、C、D均是错误的说法。
12.D解析:A表现了HNO3的氧化性;B表现了HNO3的酸性;C主要表现HNO3的不稳定性。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com