
1.水的电离和水的离子积
⑴水的电离和电离平衡:水是一种 电解质,它能微弱地电离,生成 和 离子,电离方程式为 ,简写为: ;ΔH<0。在一定温度下,纯水电离生成的c(H+)=c(OH-),实验测得在25°C时,c(H+)=c(OH-)= 。 此时水的电离度为 。
⑵影响水的电离平衡的因素:
①温度:当温度升高时,水的电离平衡向 方向移动,这时水中的c(H+)、c(OH-)如何变化?
②浓度:往水中加入酸或碱,水的电离平衡的移动方向是 ,若往水中加入强碱弱酸盐或强酸弱碱盐,水的电离平衡的移动方向是 ,
⑶水的离子积:在一定温度下,水中或 中c(H+)与c(OH-)的乘积是一个常数,用Kw表示,称为水的离子积常数,温度不同,Kw不同,在25°C时,Kw= = ;当温度升高时,Kw将 ,比如在100°C时,Kw= ,此时水的电离度为 。在常温下,c(H+)=0.01mol/L的强酸溶液与c(OH-)=0.01mol/L的强碱溶液中,Kw= ,水的电离度= 。
3.知道溶液pH的调控在工农业生产和科学研究中的重要应用。
知识梳理
2.学会使用滴定管,能进行酸碱滴定,并能绘制滴定过程中的pH变化曲线,了解酸碱中和过程中溶液pH的变化规律。
1.初步掌握测定溶液pH的方法。
4、(理)已知
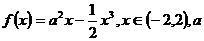 为正常数。
为正常数。
(1)可以证明:定理“若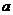 、
、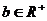 ,则
,则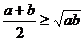 (当且仅当
(当且仅当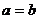 时取等号)”推广到三个正数时结论是正确的,试写出推广后的结论(无需证明);
时取等号)”推广到三个正数时结论是正确的,试写出推广后的结论(无需证明);
(2)若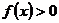 在
在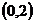 上恒成立,且函数
上恒成立,且函数 的最大值大于
的最大值大于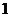 ,求实数
,求实数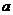 的取值范围,并由此猜测
的取值范围,并由此猜测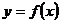 的单调性(无需证明);
的单调性(无需证明);
(3)对满足(2)的条件的一个常数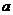 ,设
,设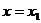 时,
时, 取得最大值。试构造一个定义在
取得最大值。试构造一个定义在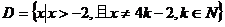 上的函数
上的函数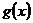 ,使当
,使当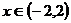 时,
时,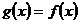 ,当
,当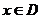 时,
时,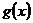 取得最大值的自变量的值构成以
取得最大值的自变量的值构成以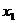 为首项的等差数列。
为首项的等差数列。
(文)已知函数 ,
,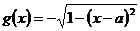 ,
,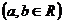
(Ⅰ)当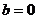 时,若
时,若 在
在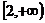 上单调递增,求
上单调递增,求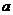 的取值范围;
的取值范围;
(Ⅱ)求满足下列条件的所有实数对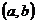 :当
:当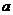 是整数时,存在
是整数时,存在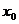 ,使得
,使得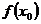 是
是 的最大值,
的最大值,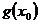 是
是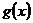 的最小值;
的最小值;
(Ⅲ)对满足(Ⅱ)的条件的一个实数对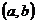 ,试构造一个定义在
,试构造一个定义在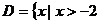 ,且
,且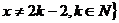 上的函数
上的函数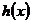 ,使当
,使当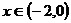 时,
时,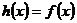 ,当
,当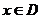 时,
时,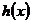 取得最大值的自变量的值构成以
取得最大值的自变量的值构成以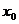 为首项的等差数列。
为首项的等差数列。
(理)解:(1)若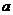 、
、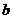 、
、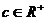 ,则
,则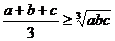 (当且仅当
(当且仅当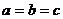 时取等号)。
时取等号)。
(2)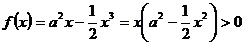 在
在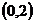 上恒成立,即
上恒成立,即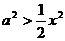 在
在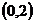 上恒成立,
上恒成立,
∵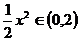 ,∴
,∴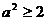 ,即
,即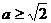 ,
,
又∵
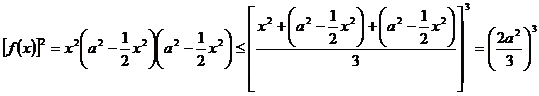 ∴
∴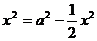 ,即
,即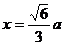 时,
时,
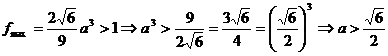 ,
,
又∵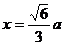
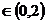 ,∴
,∴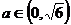 。
综上,得
。
综上,得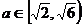 。
。
易知, 是奇函数,∵
是奇函数,∵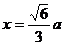 时,函数有最大值,
时,函数有最大值,
∴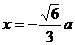 时,函数有最小值。
时,函数有最小值。
故猜测: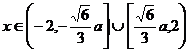 时,
时, 单调递减;
单调递减;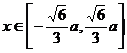 时,
时, 单调递增。
单调递增。
(3)依题意,只需构造以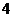 为周期的周期函数即可。
为周期的周期函数即可。
如对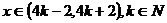 ,
,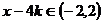 ,此时
,此时
 ,
,
即 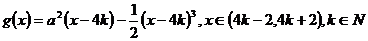 。
。
(文)解:(Ⅰ)当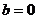 时,
时,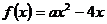 ,
,
若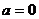 ,
,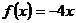 ,则
,则 在
在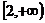 上单调递减,不符题意。
上单调递减,不符题意。
故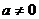 ,要使
,要使 在
在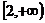 上单调递增,必须满足
上单调递增,必须满足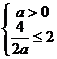 ,∴
,∴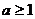 。
。
(Ⅱ)若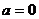 ,
,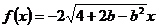 ,则
,则 无最大值,故
无最大值,故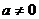 ,
,
∴ 为二次函数,
为二次函数,
要使 有最大值,必须满足
有最大值,必须满足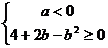 ,即
,即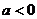 且
且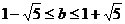 ,
,
此时,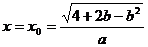 时,
时, 有最大值。
有最大值。
又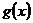 取最小值时,
取最小值时,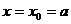 ,依题意,有
,依题意,有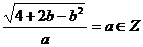 ,则
,则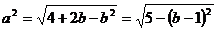 ,
,
∵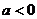 且
且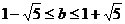 ,∴
,∴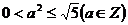 ,得
,得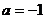 ,此时
,此时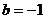 或
或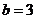 。
。
∴满足条件的实数对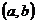 是
是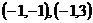 。
。
(Ⅲ)当实数对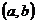 是
是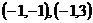 时,
时,
依题意,只需构造以2(或2的正整数倍)为周期的周期函数即可。
如对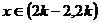 ,
,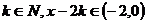 ,
,
此时,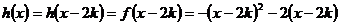 ,
,
故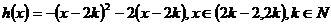

3、(12′=9′+3′)(理)设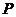 表示幂函数
表示幂函数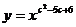 在
在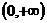 上是增函数的
上是增函数的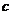 的集合;
的集合;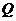 表示不等式
表示不等式 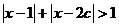 对任意
对任意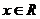 恒成立的
恒成立的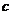 的集合。(1)求
的集合。(1)求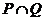 ;(2)试写出一个解集为
;(2)试写出一个解集为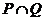 的不等式。
的不等式。
(文)设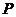 表示幂函数
表示幂函数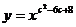 在
在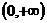 上是增函数的
上是增函数的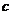 的集合;
的集合;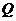 表示不等式
表示不等式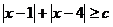 对任意
对任意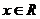 恒成立的
恒成立的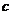 的集合。(1)求
的集合。(1)求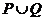 ;(2)试写出一个解集为
;(2)试写出一个解集为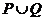 的不等式。
的不等式。
解:(理)(1)∵幂函数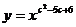 在
在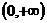 上是增函数,∴
上是增函数,∴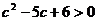 ,即
,即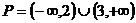 ,
,
又不等式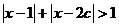 对任意
对任意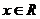 恒成立,∴
恒成立,∴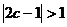 ,即
,即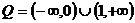 ,
,
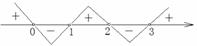 ∴
∴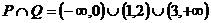 。
。
(2)一个解集为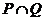 的不等式可以是
的不等式可以是
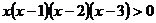 。
。
(文)(1)∵幂函数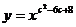 在
在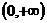 上是增函数,∴
上是增函数,∴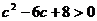 ,即
,即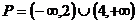 ,
,
又不等式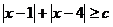 对任意
对任意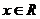 恒成立,∴
恒成立,∴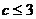 ,即
,即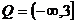 ,
,
∴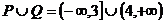 。
。
(2)一个解集为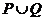 的不等式可以是
的不等式可以是
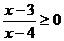 。
。
2、用水清洗一堆蔬菜上残留的农药的效果假定如下:用x单位量的水清洗一次以后,蔬菜上残留的农药量与这次清洗前残留的农药量之比为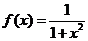 .
.
(Ⅰ)试解释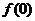 的实际意义;
的实际意义;
(Ⅱ)现有a(a>0)单位量的水,可以清洗一次,也可以把水平均分成2份后清洗两次.哪种方案清洗后蔬菜上残留的农药比较少?请说明理由.
解:(I)f(0)=1.表示没有用水清洗时,蔬菜上的农药量没有变化.……………2'
(Ⅱ)设清洗前蔬菜上的农药量为1,那么用a单位量的水清洗1次后.残留的农药量为 W1=1×f(a)=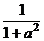 ;……………………………………………………………………4'
;……………………………………………………………………4'
又如果用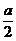 单位量的水清洗1次,残留的农药量为1×f(
单位量的水清洗1次,残留的农药量为1×f(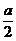 )=
)=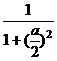 ,
,
此后再用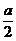 单位量的水清洗1次后,残留的农药量为
单位量的水清洗1次后,残留的农药量为
W2=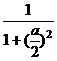 ·f(
·f(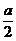 )=[
)=[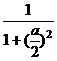 ]2=
]2=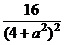 .……………………………8'
.……………………………8'
由于W1-W2=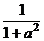 -
-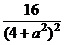 =
=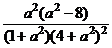 ,………………………9'
,………………………9'
故当a>2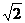 时,W1>W2,此时,把a单位量的水平均分成2份后,清洗两次,残留的农药量较少;当a=2
时,W1>W2,此时,把a单位量的水平均分成2份后,清洗两次,残留的农药量较少;当a=2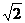 时,W1=W2,此时,两种清洗方式效果相同;当a<2
时,W1=W2,此时,两种清洗方式效果相同;当a<2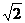 时,W1<W2,此时,把a单位量的水清洗一次,残留的农药量较少.…………………………12'
时,W1<W2,此时,把a单位量的水清洗一次,残留的农药量较少.…………………………12'
20.写出有关的化学反应方程式,是离子反应写出离子方程式。
①
②
③
④
⑤
⑥
⑦
19.(8分)用地壳中某主要元素生产的多种产品在现代高科技中占有重要位置,足见化学对现代物质文明的重要作用。例如:
(1)计算机芯片的主要成分是 ;
(2)光导纤维的主要成分是 :
(3)目前应用最多的太阳能电池的光电转化材料是 ;
(4)用作吸附剂、干燥剂、催化剂或催化剂载体的人造分子筛大多是一类称为 的化合物 ;
18.(14分)某学生兴趣小组想利用高岭土[其主要成分是Al2O3·2SiO2·2H2O]试验新型的净水剂。试验程序如下:
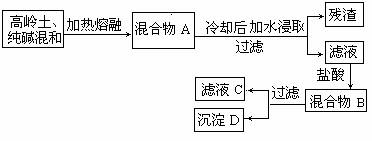
其中滤液E就是欲求的净水剂。试回答下列问题:
①写出混合物A、B,滤液C、D的主要成分
A: ;B: ;C: ;D: 。
②写出高岭土与纯碱熔融的两个化学方程式 ;
③该试验中,熔融高岭土可以选用的坩埚有
A.玻璃坩埚 B.瓷坩埚 C.氧化铝坩埚 D.铁坩埚
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com