
4.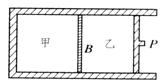 如图所示,内壁光滑的固定容器及可动活塞 P
都是绝热的,中间有一导热的可动隔板 B,B
的两边分别盛有完全相同的同一种气体甲和乙。现将活塞 P
缓慢地向左移动一段距离,已知气体的温度随其内能的增加而升高,则在移动 P
的过程中,
如图所示,内壁光滑的固定容器及可动活塞 P
都是绝热的,中间有一导热的可动隔板 B,B
的两边分别盛有完全相同的同一种气体甲和乙。现将活塞 P
缓慢地向左移动一段距离,已知气体的温度随其内能的增加而升高,则在移动 P
的过程中,
A.甲的内能不变,乙的内能不变。
B.甲的内能增加,乙的内能不变。
C.甲的内能增加,乙的内能增加。
D.隔板 B与活塞 P 移动的距离相等。
3.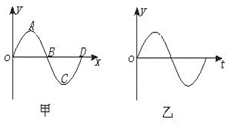 如图所示,甲图为一列简谐横波在某时刻的波形图,乙图是这列波传播介质中某质点此后一段时间内的振动图象,则
如图所示,甲图为一列简谐横波在某时刻的波形图,乙图是这列波传播介质中某质点此后一段时间内的振动图象,则
A.若波沿x轴正方向传播,图乙为A质点的振动图象
B.若波沿x轴正方向传播,图乙为B质点的振动图象
C.若波沿x轴负方向传播,图乙为质点C的振动图象
D.若波沿x轴负方向传播,图乙为质点D的振动图象
2.2008年奥运会上,光纤通信网将覆盖所有的奥运场馆,为各项比赛提供安全、可靠的通信服务,光纤通信是利用光的全反射将大量信息高速传输。若采用的光导纤维是由内芯和包层两层介质组成,下列说法正确的是
A.内芯和包层折射率相同,折射率都大
B.内芯和包层折射率相同,折射率都小
C.内芯和包层折射率不同,包层折射率较大
D.内芯和包层折射率不同,包层折射率较小
1.铀裂变的产物之一氪90(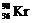 )是不稳定的,它经过一系列衰变最终成为稳定的锆90(
)是不稳定的,它经过一系列衰变最终成为稳定的锆90(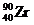 ),这些衰变是
),这些衰变是
A.1次α衰变,6次β衰变 B.4次β衰变
C.2次α衰变 D.2次α衰变,2次β衰变
22.化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素;少量A与水反应可完全水解而不被氧化或还原,所有反应产物均可溶于水;将A配成水溶液稀释后分成几份,分别加入一系列0.1mol/L的试剂,现象如下:
①加入硝酸和硝酸银,产生白色沉淀 ;
②加入氯化钡溶液,无沉淀生成;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀;
(1)由此判断组成该化合物的元素中,可能存在的卤素有 ,A与水反应后生成的溶液中含有的离子可能有 。
(2)要确定该化合物的分子式,称取11.90g A溶于水稀释至250.0mL,取25.00mL溶液加入足量的高锰酸钾溶液和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重,为2.33g,试确定A的化学式,写出计算过程。
天津市2010届高三 十校联考 第一次考试
21.(14分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。这一材料是由江苏华信塑业发展有限公司最新研发成功的新材料,并成为公安部定点产地。PETG的结构简式为:
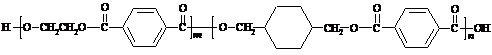
EG TPA CHDM TPA
已知:Ⅰ.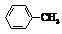
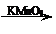

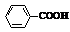
Ⅱ.RCOOR1+R2OH→RCOOR2+R1OH (R、R1、R2表示烃基)
这种材料可采用下列合成路线
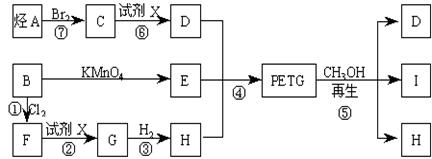 试回答下列问题:
试回答下列问题:
(1)反应②、⑥中加入的试剂X是_____________________;
(2)⑤的反应类型是________________;
(3)写出结构简式:B______________________,I________________________;
(4)合成时应控制的单体的物质的量n(D):n(E):n(H)=_____:_______:_______(用m、n表示)。
(5)写出化学方程式:
反应③:____________________________________________________;
反应⑥:_____________________________________________________。
20.(12分)硫酸钡是惟一无毒的钡盐,工业上以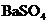 等为原料通入下列流程反应可以制备锌钡白和过氧化氢:
等为原料通入下列流程反应可以制备锌钡白和过氧化氢:
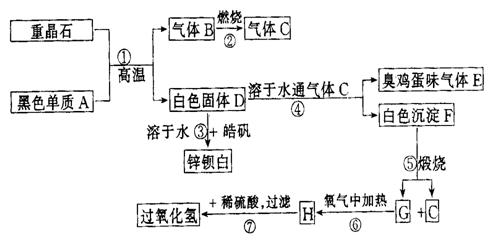
(1)上述流程中共有7个化学反应,其中_______(填编号)属于氧化还原反应.
(2)写出物质H的电子式_____________.
(3)写出下列化学反应方程式:
反应①:__________________________________________________________.
反应③:__________________________________________________________.
反应④:__________________________________________________________.
反应⑦:__________________________________________________________.
19.(6分)元素周期表是20世纪科学技术发展的重要理论依据之一,是我们学习化学的重要工具。假设NH4+是“元素”NH4的阳离子,则“元素” NH4在周期表中的位置应该是第 周期第 族;“元素” NH4的单质常温常压下应为 (填“固”、“液”或“气”)体;熔点 (填“高”或“低”) ; (填“能”或“不能”)导电;NH4的碳酸盐应 (填“易”或“不易”)溶于水。
18.(6分)氯、溴、碘同属于周期表中的VII A族,在上个世纪,人们很早就制得高碘酸及其盐,但得不到含+7价溴的化合物,1968年,化学家用发现不久的XeF2和KBrO3首先制得纯净的KBrO4晶体。
(1)高碘酸盐(IO65-)能在酸性条件下将Mn2+氧化为MnO4-(本身被还原成I03-),其反应平稳而迅速,写出离子反应方程式: 。
(2)在25℃,已知pH=2的高碘酸溶液与pH=12的NaOH溶液等体积混合,所得混合液显酸性;0.01mol·L-1的碘酸或高锰酸溶液与pH=12的NaOH溶液等体积混合,所得混合液显中性。则高碘酸是 ;高锰酸是 (填“强酸”或“弱酸”)。
(3)写出XeF2和含KOH、KBrO3的水溶液反应得到KBrO4的离子方程式 。
17.某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(忽略N2O4的存在,图中铁架台等夹持仪器均已略去):
Ⅰ.实验装置如下图1所示
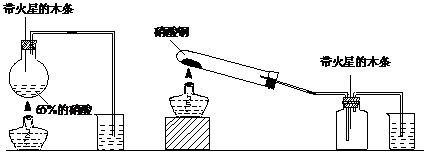
图1 图2
(1)浓硝酸受热分解的化学方程式是 。
(2)实验开始后木条上的火星逐渐熄灭,有的同学得出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确),理由是 。
Ⅱ.实验装置如上图2所示
(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气,该反应的化学方程式是 。
(2)当集气瓶中充满红棕色气体时,木条复燃了,有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确”),理由是 。
Ⅲ.为了更直接说明“NO2能否支持木条的燃烧”这一问题,请你重新设计一个简单的实验方案,简述实验原理和主要操作。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com