
2£®(2007º£ÄÏ¡¤23)ÓĂ¼Û²ăµç×Ó¶Ô»¥³âÀíÂÛÔ¤²âH2SºÍBF3µÄÁ¢̀å½á¹¹£¬Á½¸ö½áÂÛ¶¼ƠưÈ·µÄÊÇ(¡¡ )
A£®Ö±ÏßĐΣ»Èư½Ç׶ĐΡ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡ B£®VĐΣ»Èư½Ç׶ĐÎ
C£®Ö±ÏßĐΣ»Æ½ĂæÈư½ÇĐΡ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡D£®VĐΣ»Æ½ĂæÈư½ÇĐÎ
´đ°¸£ºD
¿¼µă£º±¾̀⿼²éÁ˼۲ăµç×Ó¶Ô»¥³âÀíÂÛµÄÓ¦ÓĂ¡£
½âÎö£ºH2SΪVĐΣ»BF3ΪƽĂæÈư½ÇĐΡ£
1£®(2007º£ÄÏ¡¤22)ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ(¡¡ )
A£®·Ö×Ó¾§̀åÖеÄĂ¿¸ö·Ö×ÓÄÚ̉»¶¨º¬ÓĐ¹²¼Û¼ü
B£®Ô×Ó¾§̀åÖеÄÏàÁÚÔ×Ó¼äÖ»´æÔڷǼ«ĐÔ¹²¼Û¼ü
C£®Àë×Ó¾§̀åÖĐ¿ÉÄܺ¬ÓĐ¹²¼Û¼ü
D£®½đÊô¾§̀åµÄÈÛµăºÍ·Đµă¶¼ºÜ¸ß
´đ°¸£ºC
¿¼µă£º±¾̀⿼²éÁ˾§̀åµÄ½á¹¹ÓëĐÔÖÊ¡£
½âÎö£º±¾̀âÖĐÏ¡ÓĐÆø̀åΪµ¥Ô×Ó·Ö×ÓÎ̃¹²¼Û¼ü£»Ô×Ó¾§̀åÖĐÈçSiO2 ̉²´æÔÚSi£O¼«ĐÔ¹²¼Û¼ü£¬B´í£»ÔÚï§ÑÎÖĐ¼È´æÔÚÀë×Ó¼üÓÖ´æÔÚ¹²¼Û¼ü£¬CƠưÈ·¡£½đÊô¹¯µÄÈÛµăºÜµÍ£¬D´í¡£
19£®(09Äêɽ¶«Àí×Û¡¤10)ÏÂÁĐ¹ØÓÚÂȵÄ˵·¨ƠưÈ·µÄÊÇ
A£®Cl2¾ßÓĐºÜÇ¿µÄÑơ»¯ĐÔ£¬ÔÚ»¯Ñ§·´Ó¦ÖĐÖ»ÄÜ×÷Ñơ»¯¼Á
B£®Èô35 17Cl¡¢37 17ÈôClΪ²»Í¬µÄºËËØ£¬ÓĐ²»Í¬µÄ»¯Ñ§ĐÔÖÊ ѧ¿Æ
ѧ¿Æ
C£®ÊµÑéỂÖƱ¸Cl2£¬¿ÉÓĂÅŷźÍʳÑÎË®¼¯Æø·¨ÊƠ¼¯
D£®1.12LCl2º¬ÓĐ1.7NA¸öÖÊ×Ó(NA ±íʾ°¢·üÙ¤µÂẪ³£Êư)
´đ°¸£ºC
½âÎö£º±¾̀ẩÔÂÈÔªËØΪÔØ̀壬´ÓÑơ»¯»¹Ô¡¢Ô×ӽṹ¡¢ÊƠ¼¯·½·¨²»Í¬½Ç¶È½øĐĐ¿¼²é£¬̀åÏÖÁËɽ¶«Àí×Û»¯Ñ§Ñ¡Ôñ̀âµÄĂǜâģʽ¡£ÂÈÆøÓëË®µÄ·´Ó¦¼ÈÊÇÑơ»¯¼Á̉²ÊÇ»¹Ô¼Á£»Í¬̉»ÔªËصIJ»Í¬ºËËØ»¯Ñ§ĐÔÖʼ¸ºơÍêÈ«Ïàͬ¶øÎïÀíĐÔÖʲ»Í¬£»DÖĐ̀áCl2µÄ̀å»ưδָĂ÷ÊDZê×¼×´¿ö¡£ÊµÑéỂÖƱ¸Cl2£¬¿ÉÓĂÅű¥ºÍʳÑÎË®¼¯Æø·¨ÊƠ¼¯̉²¿ÉÓĂÆ¿¿ÚỊ̈ÉÏÅÅ¿ƠÆø·¨ÊƠ¼¯£¬¹ÊCƠưÈ·¡£
20 £®(09Ä꺣ÄÏ»¯Ñ§¡¤8)ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ(ÓĂNA´ú±í°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ)
£®(09Ä꺣ÄÏ»¯Ñ§¡¤8)ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ(ÓĂNA´ú±í°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ)
 A£®2.4g½đÊôĂ¾±äÎªĂ¾Àë×ÓʱʧȥµÄµç×ÓÊưΪ0.1NA
A£®2.4g½đÊôĂ¾±äÎªĂ¾Àë×ÓʱʧȥµÄµç×ÓÊưΪ0.1NA
 B£®1molHClÆø̀åÖеÄÁ£×ÓÊưÓë0.5 mo1/LÑÎËáÖĐÈÜÖÊÁ£×ÓÊưÏàµÈ
B£®1molHClÆø̀åÖеÄÁ£×ÓÊưÓë0.5 mo1/LÑÎËáÖĐÈÜÖÊÁ£×ÓÊưÏàµÈ
 C£®ÔÚ±ê×¼×´¿öÏ£¬22.4LCH4Óë18gH2OËùº¬Óеĵç×ÓÊư¾ùΪ10 NA
C£®ÔÚ±ê×¼×´¿öÏ£¬22.4LCH4Óë18gH2OËùº¬Óеĵç×ÓÊư¾ùΪ10 NA
 D£®COºÍN2ΪµÈµç×Ó̀壬22.4LµÄCOÆø̀åÓëlmol N2Ëùº¬µÄµç×ÓÊưÏàµÈ
D£®COºÍN2ΪµÈµç×Ó̀壬22.4LµÄCOÆø̀åÓëlmol N2Ëùº¬µÄµç×ÓÊưÏàµÈ
´đ°¸£ºC¡¡
½âÎö£ºAÖĐĂ¾Îª0.1mol£¬Ê§È¥µÄµç×ÓÊưΪ0.2 NA£»BÖĐÑÎËáÎ̃̀å»ư£¬²»ÄܼÆËă³öÁ£×ÓÊư£»DÑ¡ÏîÖĐʹÓĂÆø̀åĦ¶û̀å»ư²»ÊÇÔÚ±ê×¼×´¿öÏ¡£
21 £®(09Ä꺣ÄÏ»¯Ñ§¡¤11)ÔÚ5mL 0.05 mo1/LµÄij½đÊôÂÈ»¯ÎïÈÜ̉ºÖĐ£¬µÎ¼Ó0.1 mo1/L AgNO3ÈÜ̉º£¬Éú³É³ÁµíÖÊÁ¿Óë¼ÓÈëAgNO3ÈÜ̉º̀å»ư¹ØϵÈçͼËùʾ£¬Ộ¸ĂÂÈ»¯ÎïÖĐ½đÊôÔªËصĻ¯ºÏ¼ÛΪ£º
£®(09Ä꺣ÄÏ»¯Ñ§¡¤11)ÔÚ5mL 0.05 mo1/LµÄij½đÊôÂÈ»¯ÎïÈÜ̉ºÖĐ£¬µÎ¼Ó0.1 mo1/L AgNO3ÈÜ̉º£¬Éú³É³ÁµíÖÊÁ¿Óë¼ÓÈëAgNO3ÈÜ̉º̀å»ư¹ØϵÈçͼËùʾ£¬Ộ¸ĂÂÈ»¯ÎïÖĐ½đÊôÔªËصĻ¯ºÏ¼ÛΪ£º

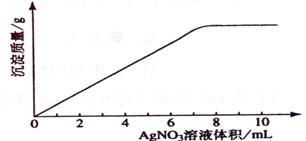
 A£®+1¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®+2¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®+3¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®+4
A£®+1¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®+2¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®+3¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®+4
´đ°¸£ºC¡¡
½âÎö£ºÉèÂÈ»¯ÎﻯѧʽΪMClx
MClx¡¡¡¡ --¡¡¡¡ x AgNO3
¡¡¡¡¡¡¡¡ 1¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ x
5mL¡Á0.05 mol¡¤L-1¡¡¡¡¡¡ 0.1 mol¡¤L-1¡Á7.5mL
x = 3
18£®(09ÄêÄ₫ÏÄÀí×Û¡¤7)½«22.4LijÆø̀¬µªÑơ»¯ºÏÎïÓë×ăÁ¿µÄ×ÆÈÈÍ·ÛÍêÈ«·´Ó¦ºó£¬Æø̀å̀å»ư11.2L(̀å»ư¾ùÔÚÏàͬ̀ơ¼₫ϲⶨ)£¬Ộ¸ĂµªÑơ»¯ºÏÎïµÄ»¯Ñ§Ê½Îª
A£®NO2¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®N2O2¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®N2O¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®N2O4
´đ°¸£ºA
½âÎö£º¸ù¾Ư2NxOy+2yCu=2yCuO+xN2£¬̉Ô¼°̀âÖĐÊư¾Ư·´Ó¦ºóÆø̀å̀å»ưΪ·´Ó¦Ç°Æø̀å̀å»ưµÄ̉»°ë£¬¿É̉Եõ½x=1£¬̣̉´ËÖ»ÓĐAÑ¡Ïî·ûºÏ̀ẩâ¡£
[µăÆÀ]±¾̀âÖ÷̉ª¿¼²éÆø̀åĦ¶û̀å»ư£¬°¢·üÙ¤µÂẪ³£ÊưµÈ֪ʶ£¬̀âÄ¿½ÏΪÀÏ̀×£¬¶øÇ̉ƠâÖÖ̀âÄ¿ÔÚÈô¸ÉÄêÇ°¾Í̉Ѿ¾³£³öÏÖÁË¡£
16£®(09Äê¹ă¶«Àí»ù¡¤20)ÉèNA´ú±í°¢·ü¼ÓµÂẪ³£Êư(NA)µÄÊưÖµ£¬ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A£®22£®4 L Cl2ÖĐº¬ÓĐNA¸öC12·Ö×Ó
B£®1 L 0£®1 mol¡¤L-1
Na2SO4ÈÜ̉ºÖĐÓĐ0£®1 NA¸öNa+
C£®1 mol H2Óë1 mol C12·´Ó¦Éú³ÉNA¸öHCl·Ö×Ó
D£®1 mol Ca±ä³ÉCa2+ʱʧȥµÄµç×ÓÊưΪ2NA
´đ°¸£ºD
½âÎö£ºAÑ¡ÏîĂ»ÓĐÖ¸³ö̀ơ¼₫ÊÇ·ñΪ±ê×¼×´¿ö£»BÑ¡ÏîÖĐNa+ µÄÎïÖʵÄÁ¿Îª0.2mol£¬̣̉´ËNa+
µÄÎïÖʵÄÁ¿Îª0.2mol£¬̣̉´ËNa+ ӦΪ0.2NA¸ö£»CÑ¡ÏîÖĐH2ºÍCl2·´Ó¦µÄ»¯Ñ§·½³̀ʽΪH2+Cl2=2HCl£¬̣̉´Ë1 mol
H2Óë1 mol C12·´Ó¦Éú³É2NA¸öHCl·Ö×Ó£»DÑ¡ÏîÖĐCaʧµç×ӵķ´Ó¦ÎªCa£2e£=Ca2+£¬̣̉´Ë1 mol
Caʧȥ2NA¸öµç×ÓÊư±ä³ÉCa2+¡£Ëù̉ÔDÑ¡ÏîƠưÈ·¡£
ӦΪ0.2NA¸ö£»CÑ¡ÏîÖĐH2ºÍCl2·´Ó¦µÄ»¯Ñ§·½³̀ʽΪH2+Cl2=2HCl£¬̣̉´Ë1 mol
H2Óë1 mol C12·´Ó¦Éú³É2NA¸öHCl·Ö×Ó£»DÑ¡ÏîÖĐCaʧµç×ӵķ´Ó¦ÎªCa£2e£=Ca2+£¬̣̉´Ë1 mol
Caʧȥ2NA¸öµç×ÓÊư±ä³ÉCa2+¡£Ëù̉ÔDÑ¡ÏîƠưÈ·¡£
 17
17 £®(09Äê½ËƠ»¯Ñ§¡¤4)ÓĂNA±íʾ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ¡£ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ
£®(09Äê½ËƠ»¯Ñ§¡¤4)ÓĂNA±íʾ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ¡£ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ
 A£®25¡æʱ£¬pH=13µÄ1.0L Ba(OH)2ÈÜ̉ºÖĐº¬ÓеÄOH£ÊưĿΪ0.2NA
A£®25¡æʱ£¬pH=13µÄ1.0L Ba(OH)2ÈÜ̉ºÖĐº¬ÓеÄOH£ÊưĿΪ0.2NA
 B£®±ê×¼×´¿öÏ£¬2.24L Cl2Óë¹ưÁ¿Ï¡NaOHÈÜ̉º·´Ó¦£¬×ª̉Ƶĵç×Ó×ÜÊưΪ0.2NA
B£®±ê×¼×´¿öÏ£¬2.24L Cl2Óë¹ưÁ¿Ï¡NaOHÈÜ̉º·´Ó¦£¬×ª̉Ƶĵç×Ó×ÜÊưΪ0.2NA
 C£®ỂÎÂÏ£¬21.0g̉̉Ï©ºÍ¶¡Ï©µÄ»́ºÏÆø̀åÖĐº¬ÓеÄ̀¼Ô×ÓÊưĿΪ1.5NA
C£®ỂÎÂÏ£¬21.0g̉̉Ï©ºÍ¶¡Ï©µÄ»́ºÏÆø̀åÖĐº¬ÓеÄ̀¼Ô×ÓÊưĿΪ1.5NA
 D£®±ê×¼×´¿öÏ£¬22.4L ¼×´¼ÖĐº¬ÓеÄÑơÔ×ÓÊưΪ1.0NA
D£®±ê×¼×´¿öÏ£¬22.4L ¼×´¼ÖĐº¬ÓеÄÑơÔ×ÓÊưΪ1.0NA
 ´đ°¸£ºC
´đ°¸£ºC
 ½âÎö£ºAÏpH=13̉²¾ÍÊÇ̉âζ×Åc(H+)=1¡Á10-13mol¡¤L-1£¬Ộc(OH-)=1¡Á10-1mol¡¤L-1£¬Ëù̉Ôn(OH£)=n(OH£)¡ÁV=1¡Á10-1mol¡¤L-1¡Á1L=0.1mol£¬Ëù̉ÔN(OH£)=0.1NA£»BÏ·¢ÉúµÄ»¯Ñ§·´Ó¦·½³̀ʽΪCl2+2NaOH=NaCl+NaClO+H2O(¸Ă·´Ó¦ÎªÆ绯·´Ó¦)£¬n(Cl2)=0.1mol£¬ÄÇĂ´×ª̉Ƶç×ÓµÄÊưÄ¿Ó¦¸ĂΪ0.1NA£»CÏ̉̉Ï©ºÍ¶¡Ï©µÄ×î¼̣ʽ¶¼ÊÇCH2£¬Ộn(CH2)=
½âÎö£ºAÏpH=13̉²¾ÍÊÇ̉âζ×Åc(H+)=1¡Á10-13mol¡¤L-1£¬Ộc(OH-)=1¡Á10-1mol¡¤L-1£¬Ëù̉Ôn(OH£)=n(OH£)¡ÁV=1¡Á10-1mol¡¤L-1¡Á1L=0.1mol£¬Ëù̉ÔN(OH£)=0.1NA£»BÏ·¢ÉúµÄ»¯Ñ§·´Ó¦·½³̀ʽΪCl2+2NaOH=NaCl+NaClO+H2O(¸Ă·´Ó¦ÎªÆ绯·´Ó¦)£¬n(Cl2)=0.1mol£¬ÄÇĂ´×ª̉Ƶç×ÓµÄÊưÄ¿Ó¦¸ĂΪ0.1NA£»CÏ̉̉Ï©ºÍ¶¡Ï©µÄ×î¼̣ʽ¶¼ÊÇCH2£¬Ộn(CH2)=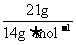 =1.5mol£¬Ëù̉Ôn(C)=01.5mol£¬N(C)=1.5NA£»DÏ±ê×¼×´¿öÏ£¬¼×´¼Îª̉º̀¬£¬ÄÇĂ´¼×´¼µÄÎïÖʵÄÁ¿¾Í²»ÊÇ1mol£¬ỘËùº¬ÓеÄÑơÔ×Ó¸öÊử²²»ÎªNA¡£
=1.5mol£¬Ëù̉Ôn(C)=01.5mol£¬N(C)=1.5NA£»DÏ±ê×¼×´¿öÏ£¬¼×´¼Îª̉º̀¬£¬ÄÇĂ´¼×´¼µÄÎïÖʵÄÁ¿¾Í²»ÊÇ1mol£¬ỘËùº¬ÓеÄÑơÔ×Ó¸öÊử²²»ÎªNA¡£
 [¿¼µă·ÖÎö]̉Ô°¢·üÙ¤µÂẪ³£ÊưΪÔØ̀忼²́ÈçÏÂ֪ʶµă¢Ù¿¼²é22.4L/molµÄƠưȷʹÓĂ£»¢Ú¿¼²éÔÚÑơ»¯»¹Ô·´Ó¦ÖеĂʧµç×ÓÊưµÄ¼ÆËă£»¢ÛƠưÈ·±íʾ̉»¶¨ÎïÖʵÄÁ¿µÄijÎïÖÊ΢Á£Ëùº¬Ä³ÖÖ΢Á£µÄ¸öÊư£»¢Ü¿¼²éÔÚ±ê×¼×´¿öÏẨ»¶῭å»ưµÄÆø̀å·Ö×ÓËùº¬µÄ·Ö×ÓÊưºÍÔ×ÓÊư¡£
[¿¼µă·ÖÎö]̉Ô°¢·üÙ¤µÂẪ³£ÊưΪÔØ̀忼²́ÈçÏÂ֪ʶµă¢Ù¿¼²é22.4L/molµÄƠưȷʹÓĂ£»¢Ú¿¼²éÔÚÑơ»¯»¹Ô·´Ó¦ÖеĂʧµç×ÓÊưµÄ¼ÆËă£»¢ÛƠưÈ·±íʾ̉»¶¨ÎïÖʵÄÁ¿µÄijÎïÖÊ΢Á£Ëùº¬Ä³ÖÖ΢Á£µÄ¸öÊư£»¢Ü¿¼²éÔÚ±ê×¼×´¿öÏẨ»¶῭å»ưµÄÆø̀å·Ö×ÓËùº¬µÄ·Ö×ÓÊưºÍÔ×ÓÊư¡£
15£®(09Äê¹ă¶«»¯Ñ§¡¤6)ÉèNA ´ú±í°¢·ü¼ÓµÂẪ³£Êư(NA )µÄÊưÖµ£¬ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A£®1 mol Ạ́Ëá¼ØÖĐ̉ơÀë×ÓËù´øµçºÉÊưΪNA
B£®̉̉Ï©ºÍ»·±ûÍé(C3H6¡¡ )×é³ÉµÄ28g»́ºÏÆø̀åÖĐº¬ÓĐ3NA ¸öÇâÔ×Ó
C£®±ê×¼×´¿öÏ£¬22.4LÂÈÆøÓë×ăÁ¿ÇâÑơ»¯ÄÆÈÜ̉º·´Ó¦×ª̉Ƶĵç×ÓÊưΪNA
D£®½«0.1molÂÈ»¯̀úÈÜÓÚ1LË®ÖĐ£¬ËùµĂÈÜ̉ºº¬ÓĐ0.1NA¡¡ Fe3+
´đ°¸£ºC
½âÎö£º K2SO4ÖĐ̉ơÀë×ÓΪẠ́Ëá¸ù£¬1molẠ́Ëá¸ùËù´øµçºÉΪ2mol£¬A´íÎó¡£̉̉Ï©ºÍC3H6µÄ×î¼̣ʽÏàͬ¾ùΪCH2£¬28g»́ºÏÆøÓĐ2molCH2£¬Ëù̉Ôº¬4molHÔ×Ó£¬B´íÎó¡£Fe3+ÔÚÈÜ̉ºÖĐ·¢ÉúË®½â£¬0.1molFeCl3ÈÜ̉ºÖĐ£¬Fe3+µÄÎïÖʵÄÁ¿̉ªĐ¡ÓÚ0.1mol£¬D´íÎó¡£
14£® (09Ä긣½¨Àí×Û¡¤8)ÉèNAΪ°¢·üÙ¤µÂẪ³£Êư£¬ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ
(09Ä긣½¨Àí×Û¡¤8)ÉèNAΪ°¢·üÙ¤µÂẪ³£Êư£¬ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ
 A£®24gĂ¾µÄÔ×ÓÁ¿×îÍâ²ăµç×ÓÊưΪNA
A£®24gĂ¾µÄÔ×ÓÁ¿×îÍâ²ăµç×ÓÊưΪNA
B£®1L0.1mol¡¤L-1̉̉ËáÈÜ̉ºÖĐH+ÊưΪ0.1NA
 C£®1mol¼×Íé·Ö×ÓËùº¬ÖÊ×ÓÊưΪ10NA
C£®1mol¼×Íé·Ö×ÓËùº¬ÖÊ×ÓÊưΪ10NA
D£®±ê×¼×´¿öÏ£¬22.4L̉̉´¼µÄ·Ö×ÓÊưΪNA
´đ°¸£ºC
½âÎö£ºAÏî£¬Ă¾µÄ×îÍâ²ăµç×ÓÊưΪ2£¬¹Ê´í£»BÏ̉̉ËáΪÈơµç½âÖÊ£¬²¿·ÖµçÀ룬¹ÊH+Đ¡ÓÚ0.1NA£¬´í£»CÏCH4µÄÖÊ×ÓÊưΪ10£¬ƠưÈ·£»DÏ̉̉´¼±ê״ϲ»ÊÇÆø̀壬´í¡£
13£®(08Äêɽ¶«Àí×Û¡¤13)NA´ú±í°¢·üÙ¤µÂẪ³£Êư£¬ÏÂÁĐĐđÊö´íÎóµÄÊÇA
¡¡A£®10 mLÖÊÁ¿·ÖÊưΪ98%µÄH2SO4£¬ÓĂˮϡÊÍÖÁ100 mL£¬H2SO4µÄÖÊÁ¿·ÖÊưΪ9.8%
¡¡B£®ÔÚH2O2+Cl2=2HCl+O2·´Ó¦ÖĐ£¬Ă¿Éú³É32 gÑơÆø£¬Ộת̉Æ2 NA¸öµç×Ó¡¡¡¡
¡¡C£®±ê×¼×´¿öÏ£¬·Ö×ÓÊưΪNAµÄCO¡¢C2H4»́ºÏÆø̀å̀å»ưԼΪ22.4 L£¬ÖÊÁ¿Îª28 g
¡¡D£®̉»¶¨Î¶ÈÏ£¬1 L 0.50 mol¡¤L-1NH4ClÈÜ̉ºÓë2 L0.25mol¡¤L-1NH4ClÈÜ̉ºº¬NH4+ÎïÖʵÄÁ¿²»Í¬
´đ°¸£ºA
½âÎö£ºÑ¡ÏîAÖиù¾ƯÏ¡ÊÍÇ°ºóÈÜÖʵÄÖÊÁ¿²»±äµĂ£º10mL¡Á¦Ñ(Ç°)¡Á98%£½100mL¡Á¦Ñ(ºó)¡Á¦Ø(ºó)£¬Ëù̉Ô¦Ø(ºó)£½£¬ÓÉÓÚ·´Ó¦Ç°ºóÈÜ̉ºµÄĂܶȲ»ÄÜÈ·¶¨£¬Ëù̉ÔÆäÖÊÁ¿·ÖÊử²²»ÄÜÈ·¶¨£»Ñ¡ÏîBÖĐn(O2)£½1mol£¬OÔªËصĻ¯ºÏ¼Û´Ó£1¼Û±äΪ0¼Û£¬Ëù̉ÔĂ¿¸öOÔ×Óʧȥ1¸öµç×Ó£¬¹Ê·´Ó¦ÖĐת̉Ƶĵç×ÓÊưΪ2NA£»Ñ¡ÏîCÖĐ·Ö×ÓÊưΪNAµÄCOºÍC2H4ÆäÎïÖʵÄÁ¿Îª1mol£¬ỘÔÚ±ê×¼×´¿öÏÂËùƠ¼µÄ̀å»ưΪ22.4L£¬ÓÉÓÚËüĂǵÄĦ¶ûÖÊÁ¿¶¼ÊÇ28g¡¤mol£1£¬¼´Æ½¾ùĦ¶ûÖÊÁ¿̉²Îª28g¡¤mol£1£¬Ëù̉ÔÆäÖÊÁ¿Îª28g£»Ñ¡ÏîDÖĐÓÉÓÚNH4++H2O NH3¡¤H2O+OH££¬Å¨¶ÈÔ½Đ¡£¬Ë®½â³̀¶ÈÔ½´ó£¬Ëù̉ÔÈÜ̉ºÖĐËùº¬NH4+µÄÎïÖʵÄÁ¿²»Í¬¡£
NH3¡¤H2O+OH££¬Å¨¶ÈÔ½Đ¡£¬Ë®½â³̀¶ÈÔ½´ó£¬Ëù̉ÔÈÜ̉ºÖĐËùº¬NH4+µÄÎïÖʵÄÁ¿²»Í¬¡£
12£®(08Äê½ËƠ»¯Ñ§¡¤3)ÓĂNA±íʾ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ¡£ÏÂÁĐĐđÊöƠưÈ·µÄÊÇC
A£®³£Î³£Ñ¹ÏµÄ33.6 LÂÈÆøÓë27 gÂÁ³ä·Ö·´Ó¦£¬×ª̉Ƶç×ÓÊưΪ3NA
B£®±ê×¼×´¿öÏ£¬22.4 L¼ºÍéÖĐ¹²¼Û¼üÊưĿΪ19NA
C£®ÓÉCO2ºÍO2×é³ÉµÄ»́ºÏÎïÖĐ¹²ÓĐNA¸ö·Ö×Ó£¬ÆäÖеÄÑơÔ×ÓÊưΪ2NA
D£®1 LŨ¶ÈΪ1 mol¡¤L-1µÄNa2CO3ÈÜ̉ºÖĐº¬ÓĐNA¸öCO32-
´đ°¸£ºC
½âÎö£ºÑ¡ÏîAÖĐn(Al)=1mol£¬Cl2µÄÎïÖʵÄÁ¿²»ÄÜÈ·¶¨£¬µ±Cl2µÄÎïÖʵÄÁ¿Đ¡ÓÚ1.5molʱ£¬×ª̉Ƶĵç×ÓÊưĐ¡ÓÚ3NA£¬µ±Cl2µÄÎïÖʵÄÁ¿µÈÓÚ»̣´óÓÚ1.5molʱ£¬×ª̉Ƶĵç×ÓÊưΪ1.5mol£»¼ºÍéÔÚ±ê×¼×´¿öÏÂΪ̉º̀壬Ëù̉ÔÆäÎïÖʵÄÁ¿²»ÄÜÓĂn£½À´È·¶¨£»Ñ¡ÏîCÖĐº¬ÓĐNA¸ö·Ö×ÓµÄCO2ºÍO2£¬ÆäÎïÖʵÄÁ¿Îª1mol£¬¶ø²»¹ÜÊÇCO2»¹ÊÇO2 1molÖĐ¾ùº¬ÓĐ2molµÄO£¬NA¸öCO2ºÍO2µÄ»́ºÏÆø̀åËùº¬µÄOÊưΪ1mol£»Ñ¡ÏîDÖĐCO32£ÎªÈơËá¸ùÀë×Ó£¬Ë®½âºóʹµĂCO32£µÄÎïÖʵÄÁ¿Đ¡ÓÚ1mol£¬CO32£µÄ¸öÊưĐ¡ÓÚNA¡£
11£®(08Ä꺣ÄÏ»¯Ñ§¡¤5)ÉèNAΪ°¢·ü¼ÓµÂẪ³£Êư£¬ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ£º
A£®±ê×¼×´¿öÏ£¬5.6 LËÄÂÈ»¯̀¼º¬ÓеķÖ×ÓÊưΪ0.25NA
B£®±ê×¼×´¿öÏ£¬14 gµªÆøº¬ÓĐµÄºËÍâµç×ÓÊưΪ5NA
C£®±ê×¼×´¿öÏ£¬22.4 LÈÎ̉â±ÈµÄÇâÆøºÍÂÈÆøµÄ»́ºÏÆø̀åÖĐº¬ÓеķÖ×Ó×ÜÊư¾ùΪNA
D£®±ê×¼×´¿öÏ£¬ÂÁ¸úÇâÑơ»¯ÄÆÈÜ̉º·´Ó¦Éú³É1 molÇâÆøʱ£¬×ª̉Ƶĵç×ÓÊưΪNA
´đ°¸£ºC
½âÎö£ºÑ¡ÏîAÖĐCCl4ÔÚ±ê×¼×´¿öÏÂΪ̉º̀壬Ëù̉ÔÆäÎïÖʵÄÁ¿Ê±²»ÄÜÓĂn£½V/22.4¼ÆËă£¬Ñ¡ÏîBÖĐn(N2)=0.5mol£¬1molN2ÖĐº¬ÓĐ14molµç×Ó£¬Ëù̉Ô0.5molN2º¬ÓĐ7NA£»Ñ¡ÏîCÖĐÔÚ±ê×¼×´¿öÏ£¬22.4LµÄÆø̀åΪ1mol£¬²»¹ÜÊÇ»́ºÏÆø̀廹ÊÇ´¿¾»µÄÆø̀壬Ëùº¬µÄ·Ö×ÓÊư¾ùΪNA£»Ñ¡ÏîDÖĐÉú³É1molH2£¬×ª̉Ƶĵç×ÓÊư±Ø¶¨Îª2NA¡£
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com