
 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
Na2O2
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
Na2O2
 ΓΓ
ΓΓ



 Na
Na
 ΓΓΓΓΓΓΓΓ Na2OΓΓΓΓΓΓ NaO HΓΓΓΓΓΓ Na2CO3ΓΓΓΓΓΓΓΓ NaHCO3
ΓΓΓΓΓΓΓΓ Na2OΓΓΓΓΓΓ NaO HΓΓΓΓΓΓ Na2CO3ΓΓΓΓΓΓΓΓ NaHCO3
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΖΫ≥Χ Ϋ–¥‘Ύ±≥Οφ)ΓΓ
2ΓΔNa2CO3 ”κNaHCO3
Na2CO3ΓΓ ΥΉΟϊΘΚΓΓΓΓ…ΪΧ§ΘΚΓΓΓΓ»ήΫβ–‘ΘΚΓΓΓΓ»»Έ»Ε®–‘ΘΚΓΓΓΓ
NaHCO3ΥΉΟϊΘΚΓΓΓΓ…ΪΧ§ΘΚΓΓΓΓ»ήΫβ–‘ΘΚΓΓΓΓ»»Έ»Ε®–‘ΘΚΓΓΓΓ
Na2CO3 ΚΆNaHCO3Ζ÷±π”κΥαΖ¥”ΠΓΓΥΌ¬ ΘΚV(Na2CO3)ΓΓV(NaHCO3)
1ΓΔNa2O2ΘΚ―’…ΪΉ¥Χ§ΓΓΓΓΓΓΓΓΓΓ ΒγΉ” Ϋ:ΓΓΓΓΓΓΓΓΓΓΓΓ ”ΟΆΨ:ΓΓΓΓΓΓΓΓΓΓΓΓ
”κH2O ΓΔCO2Μ·―ßΖΫ≥Χ Ϋ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
1ΓΔΡΤΒΡΜ·―ß–‘÷ ΓΓΓΓ ΡΤΒΡ‘≠Ή”ΫαΙΙ Ψ“βΆΦΘΚ ΓΓΓΓΓΓΓΓΓΓ
ΗζΖ«Ϋπ τΖ¥”ΠΘΚ(O2ΓΔCl2ΓΔS)Ε‘”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΔΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΔΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(2)”κH+Ζ¥”Π(H2OΓΔΥαΓΔ―Έ»ή“Κ)
ΔΌΡΤ”κΥ°Ζ¥”ΠΘ§±ξ≥ωΒγΉ”ΉΣ“ΤΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
œ÷œσΦΑΫβ ΆΘΚΗΓΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ »έΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓ ”ΈΘΚ≤ζ…ζΤχΧεΘ§‘ΎΥ°Οφ…œœρΗςΖΫ―ΗΥΌ”ΈΕ·ΉνΚσœϊ ß .ΥΜ
Κλ:ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΔΎΡΤ”κ―ΈΥαάκΉ”ΖΫ≥Χ Ϋ:ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΔέΡΤΆΕ»κΝρΥαΆ≠»ή“Κ÷–Μ·―ßΖΫ≥Χ Ϋ:ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(3)”κ”–ΜζΈοΖ¥”Π(¥ΦΓΔΖ”ΓΔτ»Υα)”κ““¥ΦΜ·―ßΖΫ≥Χ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
21Θ°AΓΔBΓΔCΓΔDΨυΈΣΕΧ÷ήΤΎ÷ςΉε‘ΣΥΊΘ§AΚΆBΆ§÷ήΤΎœύΝΎΘ§AΚΆCΆ§÷ςΉεœύΝΎΘ§»ΐ÷÷‘ΣΥΊΒΡ‘≠Ή”–ρ ΐ÷°ΚΆΈΣ31ΓΘD‘ΣΥΊ”κAΓΔBΓΔC»ΐ‘ΣΥΊΦ»≤ΜΆ§÷ήΤΎΓΔ“≤≤ΜΆ§÷ςΉεΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)–¥≥ωœ¬Ν–‘ΣΥΊΒΡΟϊ≥ΤΘΚ
A________Θ§B________Θ§C________Θ§D________ΓΘ
(2)AΚΆCΒΡΒΞ÷ Ω…÷±Ϋ”Μ·Κœ…ζ≥…Μ·ΚœΈοXΘ§Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ__________________________ΘΜXΕ‘ΜΖΨ≥ΒΡ”ΑœλΈΣ____________________________ΓΘ
(3)AΓΔBΓΔDΩ…Ήι≥…άκΉ”Μ·ΚœΈοΘ§ «“Μ÷÷≥ΘΦϊΒΡΥΌ –ßΜ·Ζ Θ§ΤδΜ·―ß ΫΈΣ________ΘΜ≥ΛΤΎ Ι”ΟΗΟΜ·Ζ ΫΪΒΦ÷¬ΆΝ»άΥαΜ·Θ§Τδ‘≠“ρ”ΟάκΉ”ΖΫ≥Χ Ϋ±μ ΨΈΣ_______________
–ßΜ·Ζ Θ§ΤδΜ·―ß ΫΈΣ________ΘΜ≥ΛΤΎ Ι”ΟΗΟΜ·Ζ ΫΪΒΦ÷¬ΆΝ»άΥαΜ·Θ§Τδ‘≠“ρ”ΟάκΉ”ΖΫ≥Χ Ϋ±μ ΨΈΣ_______________ ________ΘΜ
________ΘΜ
‘ΎΗΟΜ·ΚœΈοΒΡΥ°»ή“Κ÷–Θ§ΗςάκΉ”≈®Ε»”…¥σΒΫ–ΓΒΡ’ΐ»ΖΥ≥–ρ «___________________ΓΘ
ΫβΈωΘΚ±ΨΧβ «Ϋ®ΝΔ‘Ύ‘ΣΥΊΆΤΕœΜυ¥Γ…œΒΡΉέΚœΧβΘ§ Ήœ»ΗυΨίΧβ…ηΧθΦΰΆΤΕœ≥ωΥΡ÷÷‘ΣΥΊ « ≤Ο¥Θ§‘ΌΫχ––ΉέΚœΫβΧβΓΘAΚΆBΆ§÷ήΤΎœύΝΎΘ§«“‘≠Ή”–ρ ΐœύ≤ν1Θ§AΚΆCΆ§÷ςΉεœύΝΎΘ§‘ρ‘≠Ή”–ρ ΐœύ≤ν8Θ§»ΐ÷÷‘ΣΥΊΒΡ‘≠Ή”–ρ ΐ÷°ΚΆΈΣ31Θ§‘ρ»ΐ÷÷‘ΣΥΊΖ÷±πΈΣOΓΔNΓΔSΓΘD‘ΣΥΊ”κAΓΔBΓΔCΦ»≤ΜΆ§÷ήΤΎ”÷≤ΜΆ§÷ςΉεΘ§”ΠΈΣH‘ΣΥΊΘ§”…¥ΥΩ…Ϋβ¥πœ¬Ν–ΗςΧβΓΘ
¥πΑΗΘΚ(1)―θΓΓΒΣΓΓΝρΓΓ«β
(2)S+O2¥ΏΜ·ΦΝΓςSO2ΓΓΒΦ÷¬Υα”ξ
(3)NH4NO3
NH+H2ONH3ΓΛH2O+H+
c(NO)>c(NH)>c(H+)>c(OHΘ≠)
20Θ°ΕΧ÷ήΤΎ‘ΣΥΊAΓΔBΓΔCΓΔD,0.5 mol A‘ΣΥΊΒΡάκΉ”ΒΟΒΫ6.02ΓΝ1023ΗωΒγΉ”Κσ±ΜΜΙ‘≠ΈΣ÷––‘‘≠Ή”Θ§0.4 g AΒΡ―θΜ·Έο«ΓΚΟ”κ100 mL 0.2 mol/LΒΡ―ΈΥαΆξ»ΪΖ¥”ΠΘ§A‘ΣΥΊ‘≠Ή”ΚΥΡΎ÷ Ή” ΐ”κ÷–Ή” ΐœύΒ»ΘΜB‘ΣΥΊ‘≠Ή”ΚΥΆβΒγΉ” ΐ±»A‘ΣΥΊ‘≠Ή”ΚΥΆβΒγΉ” ΐΕύ1ΘΜCΘ≠ΚΥΆβΒγΉ”≤ψ ΐ±»A‘ΣΥΊΒΡάκΉ”ΚΥΆβΒγΉ”≤ψ ΐΕύ1ΘΜD‘ΣΥΊ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒΡ2±ΕΓΘ«κΧν–¥œ¬Ν–Ω’ΗώΘΚ
(1)AΓΔBΓΔCΓΔDΥΡ÷÷‘ΣΥΊΒΡΖϊΚ≈ «A________Θ§B________Θ§C________Θ§D________ΓΘ
(2)CΓΔDΝΫ‘ΣΥΊΉι≥…ΒΡΈο÷ Θ§Ζ÷Ή”ΡΎΚ§”–________Φϋ(ΧνΓΑΦΪ–‘Γ±ΜρΓΑΖ«ΦΪ–‘Γ±Θ§œ¬Ά§)ΓΘ
(3)B”κDΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·ΈοΒΡΥα–‘«Ω»θB______ __D(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑΘΫΓ±)ΓΘ
__D(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑΘΫΓ±)ΓΘ
(4)BΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·ΈοΧεœ÷________(ΧνΓΑΥα–‘Γ±ΓΔΓΑΦν–‘Γ±ΜρΓΑΝΫ–‘Γ±)Θ§Ρή÷ΛΟςΗΟ–‘÷ ΒΡάκΉ”ΖΫ≥Χ Ϋ±μ ΨΈΣ___________________________________________ΓΘ
ΫβΈωΘΚ0.5 mol A‘ΣΥΊΒΡάκΉ”ΒΟΒΫ6.02ΓΝ1023ΗωΒγΉ”±ΜΜΙ‘≠ΈΣ÷––‘‘≠Ή”Θ§‘ρA‘ΣΥΊ–Έ≥…ΒΡάκΉ”ΈΣA2+Θ§―θΜ·Έο–Έ ΫΈΣAOΘ§ΗυΨίAO”κ―ΈΥαΖ¥”ΠΒΡΝΩΒΡΙΊœΒΘΚ
M(AO)ΘΫΘΫ40 gΓΛmolΘ≠1Θ§Υυ“‘A‘ΣΥΊ‘≠Ή”ΒΡ÷ ΝΩ ΐΈΣ40Θ≠16ΘΫ24Θ§“ρΈΣA‘ΣΥΊ‘≠Ή”ΚΥΡΎ÷ Ή” ΐΚΆ÷–Ή” ΐœύΒ»Θ§Υυ“‘AΈΣMgΘ§”…Χβ“β“ά¥ΈΆΤ÷ΣBΈΣAlΘ§CΈΣClΘ§DΈΣCΓΘ
¥πΑΗΘΚ(1)MgΓΓAlΓΓClΓΓC
(2)ΦΪ–‘ΓΓ(3)<
(4)ΝΫ–‘
Al(OH)3+3H+===Al3++3H2O
Al(OH)3+OHΘ≠===AlO+2H2O
19Θ°(2009ΓΛΥό÷ίΡΘΡβ)”–ΔΌ-ΔύΑΥ÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§Τδ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–ΔΎΓΔΔΏΓΔΔύ»ΐ÷÷‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΒΡœύΕ‘ΈΜ÷Ο»γœ¬Θ§«“‘ΣΥΊΔΎΥυ¥Π÷ςΉεΒΡΈΜ÷ΟΈΣΥυ”–÷ςΉεΒΡ’ΐ÷–ΦδΓΘ
|
ΔΎ |
ΓΓ |
ΓΓ |
ΓΓ |
|
ΓΓ |
ΓΓ |
 ΔΏ |
ΓΓ Δύ |
(1)‘ΣΥΊΔΎ‘Ύ÷ήΤΎ±μ÷–ΒΡ ΈΜ÷ΟΈΣ________ΘΜΔΎΓΔΔΏΓΔΔύ»ΐ÷÷‘ΣΥΊΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘”…«ΩΒΫ»θΒΡΥ≥–ρ «______________________(”ΟΜ·―ß Ϋ±μ Ψ)ΓΘ
ΈΜ÷ΟΈΣ________ΘΜΔΎΓΔΔΏΓΔΔύ»ΐ÷÷‘ΣΥΊΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘”…«ΩΒΫ»θΒΡΥ≥–ρ «______________________(”ΟΜ·―ß Ϋ±μ Ψ)ΓΘ
(2)»γΆΦΥυ ΨΘ§ΦΉΓΔ““ΓΔ±ϊΓΔΕΓΨυΈΣΔΌ-Δύ÷–Ρ≥–©‘ΣΥΊ–Έ≥…ΒΡΒΞ÷ ΜρΜ·ΚœΈοΘ§Ζ¥”ΠaΈΣ÷ΟΜΜΖ¥”ΠΘ§Ζ¥”ΠbΈΣΜ·ΚœΖ¥”ΠΓΘΒΞ÷ ““”κΒΞ÷ ±ϊΥυΚ§‘ΣΥΊΈΜ”ΎΆ§“Μ÷ςΉεΘ§ ‘–¥≥ωΖϊΚœΧθΦΰΒΡΖ¥”ΠaΒΡΝΫΗωΜ·―ßΖΫ≥Χ ΫΘΚ____________________________________________________ΓΔ
______________________________ __________________________________________ΓΘ
__________________________________________ΓΘ
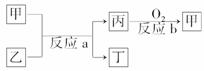
ΫβΈωΘΚ”…‘ΣΥΊΔΎΥυ¥Π÷ςΉε’ΐ÷–ΦδΘ§«“ΈΣΒΎΕΰ÷ήΤΎΘ§Ω…÷ΣΔΎΈΣΧΦ‘ΣΥΊΘ§‘ρΔΏΈΣΝρ‘ΣΥΊΘ§ΔύΈΣ¬»‘ΣΥΊΘ§ΔΎΔΏΔύ»ΐ÷÷‘ΣΥΊΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘”…«ΩΒΫ»θΒΡΥ≥–ρ « HClO4>H2SO4>H2CO3ΓΘ
HClO4>H2SO4>H2CO3ΓΘ
ΕΧ÷ήΤΎ‘ΣΥΊ÷–ΡήΖΔ…ζ÷ςΉεΦδΒΡ÷ΟΜΜΖ¥”ΠΒΡ”–ΔΌ2Na+2H2O===2Na OH+H2ΓϋΘ§ΔΎSiO2+2CSi+2COΓϋΘ§Δέ2H2S+O22H2O+2SΘ§ΖϊΚœ…œ ωΧθΦΰΒΡ «ΔΌΓΔΔΎΓΘ
OH+H2ΓϋΘ§ΔΎSiO2+2CSi+2COΓϋΘ§Δέ2H2S+O22H2O+2SΘ§ΖϊΚœ…œ ωΧθΦΰΒΡ «ΔΌΓΔΔΎΓΘ
¥πΑΗΘΚ(1)ΒΎΕΰ÷ήΤΎΔτAΉε
HClO4>H2SO4>H2CO3
(2)2Na+2H2O===2NaOH+H2Γϋ
SiO2+2CSi+2COΓϋ
18Θ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ°ΉνΆβ≤ψΒγΉ” ΐΈΣ¥ΈΆβ≤ψΒγΉ” ΐ“ΜΑκΒΡ‘ΣΥΊ“ΜΕ® τ”ΎΦνΫπ τ‘ΣΥΊ
BΘ°‘ΣΥΊ÷ήΤΎ±μ÷–¥”ΒΎΔσBΉεΒΫΒΎΔρBΉε÷°Φδ10ΗωΉί––ΒΡ‘ΣΥΊΕΦ «Ϋπ τ‘ΣΥΊ
CΘ°Ά§÷ήΤΎΒΎΔρAΉε”κΒΎΔσAΉε‘ΣΥΊΒΡ‘≠Ή”–ρ ΐœύ≤ν1Μρ11Μρ25
DΘ°»τ÷ςΉε‘ΣΥΊΒΡΉε–ρ ΐΈΣaΘ§÷ήΤΎ ΐΈΣbΘ§Β±<1 ±Θ§ΗΟ‘ΣΥΊΈΣΖ«Ϋπ τ‘ΣΥΊ
¥πΑΗΘΚBC
17Θ°(2009ΓΛ’ψΫ≠÷ντΏΗΏΕΰΤΎΡ©)ΉνΫϋΘ§ΩΤ―ßΦ“ΖΔœ÷ΝΥ―θ‘ΣΥΊΒΡ“Μ÷÷–¬ΒΡΝΘΉ”O4Θ§≤Δ”Ο÷ ΤΉ“«ΧΫ≤βΒΫΝΥΥϋ¥φ‘ΎΒΡ÷ΛΨίΓΘ»τΗΟ―θΖ÷Ή”ΨΏ”–Ω’ΦδΕ‘≥ΤΫαΙΙΘ§œ¬Ν–ΙΊ”ΎΗΟ―θΖ÷Ή”ΒΡΥΒΖ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ° «―θ‘ΣΥΊΒΡ“Μ÷÷Ά§ΈΜΥΊ
BΘ° «―θΤχΒΡΆ§ΥΊ“λ–ΈΧεΘ§Ζ÷Ή”ΡΎ≤ΜΚ§”–ΦΪ–‘Φϋ
CΘ° «“Μ÷÷–¬ΒΡ―θΜ·Έο
DΘ° «≥τ―θΒΡΆ§Ζ÷“λΙΙΧε
¥πΑΗΘΚB
16Θ°œ¬Ν–”–ΙΊΦνΫπ τ‘ΣΥΊΒΡ–π ω÷–Θ§’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ°ΦνΫπ τ‘ΣΥΊΒΡάκΉ”ΨΏ”–Κή«ΩΒΡ―θΜ·–‘
BΘ°ΦνΫπ τ‘ΣΥΊΒΡΒΞ÷ «Κή«ΩΒΡΜΙ‘≠ΦΝ
CΘ°ο°”κΥ°ΒΡΖ¥”Π±»ΡΤ”κΥ°ΒΡΖ¥”ΠΨγΝ“
DΘ°οΛΒΡ»έΒψ±»ΡΤΒΆ
¥πΑΗΘΚBD
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com