
16、可逆反应、不可逆反应
15、化学反应速率的典型实验 P20实验2-1锌与不同浓度硫酸的反应 P22实验2-2 过氧化氢分解 (催化剂是MnO2、FeCl3、CuSO4) P25探究 不同浓度的KMnO4与H2C2O4反应速率;唾液、H2SO4溶液对淀粉水解的催化作用
14、化学反应速率的典型表格
2A B+D (B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化) B+D (B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化) |
||||||||
 实验序号 实验序号 |
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
800℃ |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
3 |
800℃ |
c3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
13、化学反应速率的典型曲线
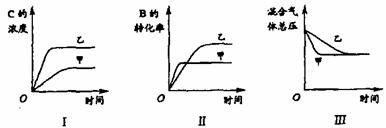
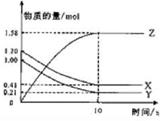
12、影响化学反应速率的因素 浓度、压强、温度、催化剂(光辐射、放射线、粉碎、等)
11、如何计算化学反应速率
定义: , 列三项求解(开始、变化、t时候)
, 列三项求解(开始、变化、t时候)
10、在化学反应中,各物质的反应速率之比等于方程式中化学计量数之比
9、化学反应速率、表达式、单位
8、盖斯定律 计算2C+O2 = 2CO的反应热,并写出热化学方程式(P13);
计算2C+2H2+O2=CH3COOH的反应热,并写出热化学方程式(P14)。
7、新能源
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com