
31Θ°(8Ζ÷)¥πΑΗ. (1) CO2 ΓΔCCl4 (ΤδΥϊΚœάμ¥πΑΗ≤Έ’’ΗχΖ÷)(Ης2Ζ÷)
(2) ΓΓ7ΓΓ 1(Ης2Ζ÷)
30ΓΔ(9Ζ÷)ΓΓ Δ≈N2O5 (2Ζ÷)ΓΓΓΓ ΔΤNH4++ΓΓΓΓΓΓ OHΘ≠ΓΓ (ΤδΥϊΚœάμ¥πΑΗ≤Έ’’ΗχΖ÷)(4Ζ÷)
ΓΓ Δ«ΓΓΓΓ NH4NO3ΓΓΓΓ Υα–‘(3Ζ÷)ΓΓ
28Θ°(16Ζ÷)(1)Cl2 +ΓΓ H2OΓΓ ΘΫ HCl + HClOΓΓΓΓ (2)ΓΟIΓΟBrΓΟΓΓΓΓ Π“Φϋ
(3) ΔΌ1s22s22p63s23p63d54s1 +6ΘΜΔΎ 4ΘΜΔέ1s2 2s2 2p6 3s2 3p6 3d5 Μρ[Ar] 3d5
(4)N2(g)ΓΓ
+ΓΓ 3H2(g)ΓΓ  ΓΓ2NH3
(g)ΓΓ ΓΓΓΓΓςH=Θ≠93kJΓΛmolΘ≠1
29Θ°(12Ζ÷)
ΓΓ2NH3
(g)ΓΓ ΓΓΓΓΓςH=Θ≠93kJΓΛmolΘ≠1
29Θ°(12Ζ÷)
ΓΓ (1)3s2 3p5
(2)S2Θ≠ΘΨO2Θ≠ΘΨNa+
ΓΓ(3)V–ΈΓΓ ÷±œΏ–ΈΓΓ SO2ΓΓ “ρΈΣCO2 «Ζ«ΦΪ–‘Ζ÷Ή”Θ§SO2ΚΆH2OΕΦ «ΦΪ–‘Ζ÷Ή”Θ§ΗυΨίΓΑœύΥΤœύ»ήΓ±‘≠άμΘ§SO2‘ΎH2O÷–ΒΡ»ήΫβΕ»Ϋœ¥σ
27.(8Ζ÷)(1)κ≤ΓΓ (2)ClΘ≠(3)K+(4)S2Θ≠
26Θ°(5Ζ÷)(1)C(2)A(3)C(4)C (5)B
33Θ°(6Ζ÷) “―÷Σ
“―÷Σ
|
ΓΓ |
Li |
Na |
K |
|
»έΒψ |
180 |
98 |
63 |
|
Ζ–Βψ |
1347 |
881 |
756 |
ΜΊ¥πΈ ΧβΘΚ(M±μ ΨΦνΫπ τ)(Χν> Μρ < ΓΓΓΓ ΜρΘΫ)
(1)ΓςH2(Li)ΓΓΓΓΓΓΓΓ ΓΓΓςH2(Na)Θ§ΓΓ ΓςH3(Li)ΓΓΓΓΓΓ ΓΓΓςH3(Na)Θ§
(2)“―÷ΣΫπ τΜνΕ·–‘Υ≥–ρΫπ το°±»ΡΤΜνΤΟΘ§‘ρΓςH4(Li)ΓΓΓΓΓΓ ΓΓΓςH4(Na)ΓΘ
32Θ°(6Ζ÷) AΓΔBΓΔCΓΔDΥΡ÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§ΥϋΟ«ΒΡΒΞ÷ ‘Ύ“ΜΕ®ΧθΦΰœ¬ΕΦΡή”κΥ°Ζ¥”ΠΓΘA‘ΣΥΊΒΞ÷ ”κΥ°’τΤχΖ¥”ΠΒΡ≤ζΈο «Υ°ΟΚΤχΒΡ÷ς“Σ≥…Ζ÷Θ§1 molB‘ΣΥΊΒΞ÷ ”κΥ°Ζ¥”Π≤ζ…ζ0.5molΤχΧεFΘ§1 molC‘ΣΥΊΒΞ÷ ”κΥ°Ζ¥”Π≤ζ…ζ0.5molΤχΧεEΘ§EΓΔFœύΜΞΜ·Κœ…ζ≥…Υ°Θ§D‘ΣΥΊΒΞ÷ ”κΥ°Ζ¥”Π…ζ≥…ΝΫ÷÷ΥαΓΘ
(1)CΒΞ÷ ”κΥ°Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ___________________________________
(2)A ΉνΗΏΦέ―θΜ·Έο”κCΒΡ“Μ÷÷―θΜ·ΈοΡήΖ¥”Π…ζ≥…ΤχΧεFΘ§‘ρΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(3)ΥΡ÷÷‘ΣΥΊ÷–ΉνΗΏΦέ―θΜ·ΈοΥ°Μ·ΈοΥα–‘Ήν«ΩΒΡ «_______________ΓΘ(ΧνΥαΒΡΜ·―ß Ϋ)
31Θ° (8Ζ÷)œ¬±μΝ–≥ω«Α20Κ≈‘ΣΥΊ÷–ΒΡΡ≥–©‘ΣΥΊ–‘÷ ΒΡ“Μ–© ΐΨίΘΚ
(8Ζ÷)œ¬±μΝ–≥ω«Α20Κ≈‘ΣΥΊ÷–ΒΡΡ≥–©‘ΣΥΊ–‘÷ ΒΡ“Μ–© ΐΨίΘΚ
|
‘ΣΥΊ –‘÷ ΓΓ |
A |
B |
C |
D |
E |
F |
G |
H |
I |
J |
|
‘≠Ή”ΑκΨΕ(10-10m) |
1.02 |
2.27 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.86 |
0.75 |
1.17 |
|
ΉνΗΏΦέΧ§ |
+6 |
+1 |
- |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
+4 |
|
ΉνΒΆΦέΧ§ |
-2 |
- |
-2 |
- |
-4 |
-3 |
-1 |
- |
-3 |
-4 |
‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)”……œ ωCΓΔEΓΔG»ΐ÷÷‘ΣΥΊ÷–ΒΡΡ≥ΝΫ÷÷‘ΣΥΊ–Έ≥…ΒΡΜ·ΚœΈο÷–Θ§ΟΩΗω‘≠Ή”ΒΡΉνΆβ≤ψΕΦ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΒΡΩ…Ρή «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (–¥Ζ÷Ή” ΫΘ§–¥≥ωΝΫ÷÷Φ¥Ω…),
(2)‘ΣΥΊE”κCΦΑ«β‘ΣΥΊΩ…–Έ≥…“Μ÷÷œύΕ‘Ζ÷Ή”÷ ΝΩΈΣ60ΒΡ“Μ‘Στ»ΥαΖ÷Ή”ΓΘΤδΖ÷Ή”÷–Ι≤–Έ≥…
ΓΓΓΓΓΓ ΗωΠ“ΦϋΘ§ΓΓΓΓ ΓΓΓΓΓΓΗωΠ–ΦϋΓΘ
30Θ°(9Ζ÷)“―÷ΣXΓΔYΓΔZΕΦ «ΕΧ÷ήΤΎΒΡ‘ΣΥΊΘ§ΥϋΟ«ΒΡ‘≠Ή”–ρ ΐ“ά¥ΈΒί‘ωΘ§X‘≠Ή”ΒΡΒγΉ”≤ψ ΐ”κΥϋΒΡΚΥΆβΒγΉ”Ήή ΐœύΆ§Θ§ΕχZ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒγΉ” ΐΒΡ»ΐ±ΕΘ§YΚΆZΩ…“‘–Έ≥…Εύ÷÷ΤχΧ§Μ·ΚœΈοΘ§‘ρ
(1)”…YΚΆZΉι≥…Θ§«“YΚΆZ÷ ΝΩ±»ΈΣ7ΓΟ20ΒΡΜ·ΚœΈοΒΡΜ·―ß Ϋ(Ζ÷Ή” Ϋ) «ΓΓΓΓΓΓΓΓ
(2)”…XΓΔYΓΔZ÷–ΒΡΝΫ÷÷‘ΣΥΊΉι≥…Θ§«“”κX2ZΖ÷Ή”ΨΏ”–œύΆ§ΒγΉ” ΐΒΡΝΫ÷÷άκΉ” «ΓΓΓΓΓΓΓΓΓΓ ΚΆ
ΓΓΓΓΓΓΓΓΓΓ
(3)XΓΔYΓΔZΩ…“‘–Έ≥…“Μ÷÷―ΈΘ§¥Υ―Έ÷–XΓΔYΓΔZ‘ΣΥΊΒΡ‘≠Ή”ΒΡΗω ΐ±»ΈΣ4ΓΟ2ΓΟ3Θ§ΗΟ―ΈΒΡΜ·―ß Ϋ(Ζ÷Ή” Ϋ) «ΓΓΓΓΓΓΓΓΓΓ
Θ§ΗΟ―Έ»ή“Κ≥ ΓΓΓΓΓΓΓΓ
–‘(ΧνΥα–‘ΜρΦν–‘)
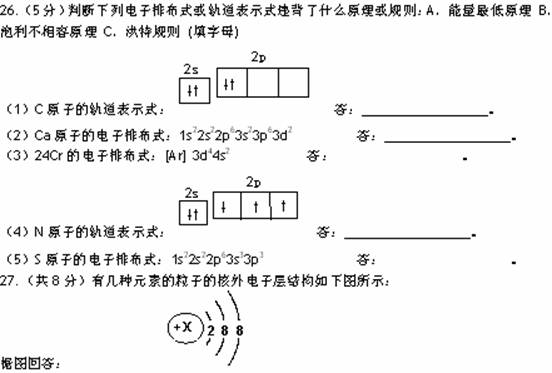
(1)ΤδΒγ÷––‘ΝΘΉ”Θ§“ΜΑψ≤ΜΚΆΤδΥϋ‘ΣΥΊΒΡ‘≠Ή”Ζ¥”ΠΘ§’β÷÷ΝΘΉ”ΒΡΟϊ≥Τ «ΓΓΓΓΓΓΓΓ ΓΘ
(2)Ρ≥ΝΘΉ”ΒΡ―Έ»ή“ΚΘ§Φ”»κAgNO3»ή“Κ ±Μα≥ωœ÷ΑΉ…ΪΜκΉ«Θ§’β÷÷ΝΘΉ”ΖϊΚ≈ «ΓΓΓΓΓΓΓΓ ΓΓΓΘ
(3)Ρ≥ΝΘΉ”―θΜ·–‘…θ»θΘ§ΒΪΒΟΒΫΒγΉ”ΚσΜΙ‘≠–‘Ϋœ«ΩΓΘ«“’β÷÷‘≠Ή”ΉνΆβ≤ψ÷Μ”–“ΜΗω≥…ΒΞΒγΉ”Θ§’β÷÷ΝΘΉ”ΖϊΚ≈ «ΓΓΓΓΓΓΓΓΓΓ ΓΘ
(4)Ρ≥ΝΘΉ”ΨΏ”–ΜΙ‘≠–‘Θ§«“’β÷÷ΝΘΉ” ß»Ξ2ΗωΒγΉ”Φ¥±δ≥…‘≠Ή”Θ§’β÷÷ΝΘΉ”ΖϊΚ≈ «ΓΓΓΓΓΓΓΓ ΓΘ
28Θ°(16Ζ÷)œ¬±μΈΣ‘ΣΥΊ÷ήΤΎ±μΒΡ“Μ≤ΩΖ÷Θ§aΓΔbΓΔcΓ≠Γ≠ΈΣ≤ΩΖ÷‘ΣΥΊΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
|
a |
ΓΓ |
ΓΓ |
|||||||||||||||
|
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
f |
h |
i |
ΓΓ |
|||||||||
|
ΓΓ |
b |
ΓΓ |
e |
ΓΓ |
ΓΓ |
ΓΓ |
j |
ΓΓ |
|||||||||
|
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
c |
ΓΓ |
d |
ΓΓ |
ΓΓ |
g |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
k |
ΓΓ |
|
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
l |
ΓΓ |
(1)«κ–¥≥ωjΒΡΒΞ÷ ”κaΓΔh–Έ≥…ΒΡΜ·ΚœΈοΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
(2)jΓΔkΓΔl»ΐ÷÷‘ΣΥΊ÷°ΦδΡή“‘‘≠Ή”Ηω ΐ±»1ΓΟ1ΝΫΝΫ–Έ≥…ΜΞΜ·ΈοΘ§’β–©ΜΞΜ·ΈοΒΡ–‘÷ άύΥΤ”Ύ’β–©‘ΣΥΊΒΞ÷ ΒΡ–‘÷ ΓΘ«κ–¥≥ωkΓΔlΒΡΜΞΜ·ΈοΒΡΒγΉ” ΫΓΓΓΓΓΓΓΓΓΓ Θ§Υϋ «”…ΓΓΓΓΓΓΓΓΓΓ Φϋ(ΗυΨί‘≠Ή”ΙλΒάΒΡ÷ΊΒΰ≥ΧΕ»Χν–¥)–Έ≥…Μ·ΚœΈο
(3)ΔΌ«κ–¥≥ω…œ ω‘ΣΥΊc‘≠Ή”ΒΡΜυΧ§ΒγΉ”≈≈≤Φ ΫΈΣΘΚΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ§ΗΟ‘ΣΥΊΒΡΉνΗΏ’ΐΜ·ΚœΦέΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
ΔΎΡ≥‘ΣΥΊΒΡ‘≠Ή”ΜυΧ§ ±”–6ΗωΒγΉ”¥Π”Ύ3dΙλΒά…œΘ§‘ρΗΟ‘ΣΥΊ‘≠Ή”ΒΡ3dΙλΒά…œΒΡΈ¥≥…Ε‘ΒγΉ””–___________ΗωΓΘ
ΔέΡ≥‘ΣΥΊΒΡΜυΧ§‘≠Ή” ß»Ξ3ΗωΒγΉ”ΚσΘ§ΥϋΒΡ3dΙλΒάΡΎΒγΉ”«ΓΚΟΑκ≥δ¬ζΘ§ΤδάκΉ”ΒΡΒγΉ”≈≈≤Φ ΫΈΣ___ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ _______ΓΘ
(4)Α± «ΒΣ―≠ΜΖ÷–ΒΡ÷Ί“ΣΈο÷ Θ§Α±ΒΡΚœ≥… «ΡΩ«ΑΤ’±ι Ι”ΟΒΡ»ΥΙΛΙΧΒΣΖΫΖ®ΓΘ “―÷ΣΘΚH-HΦϋΡήΈΣ436kJΓΛmol-1Θ§NΓ‘NΦϋΡήΈΣ945kJΓΛmol-1Θ§N-HΦϋΡήΈΣ391kJΓΛmol-1ΓΘ–¥≥ωΚœ≥…Α±Ζ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓ 29Θ°(12Ζ÷)ΕΧ÷ήΤΎ÷ςΉε‘ΣΥΊAΓΔBΓΔCΓΔDΓΔEΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–BΓΔDΆ§÷ςΉεΘ§CΓΔDΓΔEΆ§÷ήΤΎΘ§A‘≠Ή”ΚΥΆβΒΡL≤ψΒγΉ” ΐ «K≤ψΒΡΝΫ±ΕΘ§B «ΒΊΩ«÷–Κ§ΝΩΉνΗΏΒΡ‘ΣΥΊΘ§C «ΕΧ÷ήΤΎ‘ΣΥΊ÷–‘≠Ή”ΑκΨΕΉν¥σΒΡ÷ςΉε‘ΣΥΊΓΘ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)E‘≠Ή”ΒΡΦέΒγΉ”≈≈≤Φ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2)BΓΔCΓΔD»ΐ÷÷‘ΣΥΊ–Έ≥…ΒΡΦρΒΞάκΉ”ΒΡΑκΨΕ”…¥σΒΫ–ΓΒΡΥ≥–ρ «ΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ(”ΟάκΉ”ΖϊΚ≈±μ Ψ)
(3)AB2”κDB2Ζ÷Ή”ΒΡΩ’ΦδΝΔΧεΫαΙΙΖ÷±π «ΓΓΓΓΓΓΓΓΓΓ ΚΆΓΓΓΓΓΓΓΓΓΓ Θ§œύΆ§ΧθΦΰœ¬ΝΫ’Ώ‘ΎΥ°÷–ΒΡ»ήΫβΕ»Ϋœ¥σΒΡ «ΓΓΓΓΓΓΓΓΓΓ (–¥Ζ÷Ή” Ϋ)Θ§άμ”… «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com