
30. (5分)某化学研究性学习小组为测定市场出售的食醋总酸量(国家规定食醋中总酸量3.5g/100mL-5g/100mL),拟配制一定质量分数的氢氧化钠溶液,然后进行测定。请你参与该小组的实验研究,并回答相关问题。
(1)配制100g质量分数为5%的氢氧化钠溶液需要水 ▲ mL(水的密度为1g/cm3)。
(2)若食醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的方程式为:
CH3COOH + NaOH = CH3COONa + H2O
现有食醋500mL,甲同学从中取出10mL食醋,加入5%的氢氧化钠溶液4.8g,恰好完全反应。请通过计算判断该食醋是否合格?(写出计算过程)
|
29.(4分)某品牌果汁的包装盒上标明维生素C含量≥50mg/100mL。
(1)中学生每天需要约60 mg维生素C。若完全从果汁补充,则需要该品牌果汁 ▲ mL。
(2)已知:维生素C的相对分子质量为176,维生素C中C、H、O三种元素的质量比为9∶1∶12。则维生素C的化学式为 ▲ 。
28.(9分)我们在学习碳酸钠和碳酸氢钠的时候,做过如下图装置的实验。
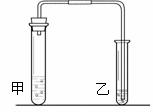
向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中,观察现象。
用碳酸氢钠代替碳酸钠进行上述实验,观察现象。
(1)通过比较试管甲中的两次反应,填写下表:
|
|
碳酸钠+盐酸 |
碳酸氢钠+盐酸 |
|
实验现象 |
反应迅速,生成大量气体。 |
反应 ▲ ,生成气体更多。 |
|
实验结论 |
▲ |
写出乙中反应的化学方程式: ▲ 。
(2)某同学对碳酸钠和碳酸氢钠与盐酸反应的快慢进一步研究。在老师的指导下,设计了下面的实验探究方案。
实验用品:相同型号的U型管2支、橡皮塞2个、5mL一次性注射器2支、气球个。
实验装置:如图。
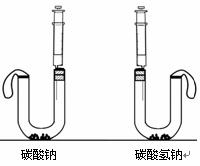
实验操作:在U型管中分别加入一定量碳酸钠和碳酸氢钠固体,在两支注射器中分别吸入同溶质质量分数、同体积的足量稀盐酸。将注射器插入橡皮塞中,然后同时迅速将盐酸分别注入U型管中。请对上述实验方案分析评价。
①若取用碳酸钠0.53g,为控制实验中产生气体的量相同,应取用碳酸氢钠 ▲ g;
②该同学设计的实验方案是运用了 ▲ 研究的方法;
③实验过程中需要观察的现象是 ▲ 。
27.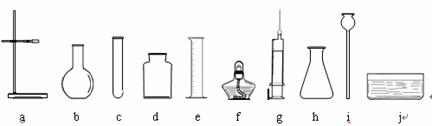 (8分)请你根据提供的实验仪器和药品参与实验室气体制备的研究与实践。实验仪器如下图所示(导管、橡皮塞等未画出):
(8分)请你根据提供的实验仪器和药品参与实验室气体制备的研究与实践。实验仪器如下图所示(导管、橡皮塞等未画出):
实验药品:氯酸钾、5%双氧水、大理石、稀盐酸、稀硫酸、高锰酸钾
[比较研究] 请填写下表
|
制取气体 |
反应物的状态 |
反应条件 |
收集方法和依据 |
|
|
氧气 |
固体 |
加热 |
排水集气法 |
O2难溶于水 |
|
二氧化碳 |
固体和液体 |
常温 |
▲ |
▲ |
[实践研究]
(1)某同学选用a、c、d、f、j等组装制取和收集氧气的装置,该同学选用的药品是 ▲ 。
下列是该同学部分实验操作,其中不合理的是 ▲ 。
A.先检查装置的气密性,后加药品 B.先固定试管,后放置酒精灯
C.先将导管伸入集气瓶,后加热试管 D.实验结束先将导管移出水面,后熄灭酒精灯
(2)四位同学根据提供的实验仪器分别设计了下列四套制取和收集二氧化碳的装置。
|
|


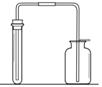
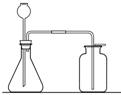

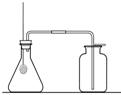
A B C D
|
|
气体制取和收集装置的选择依据
26.(4分)请将体现下列实验操作目的的正确选项,填在对应的横线上。
A.防止药品污染 B.防止试管破裂 C.防止实验误差 D.防止液体溅出
(1)加热试管时,先均匀加热,后集中加热。 ▲
(2)滴管使用后,及时清洗并放在试管架上。 ▲
(3)过滤时,混合液沿玻璃棒慢慢倒入漏斗中。 ▲
(4)量取液体时,视线与凹液面最低处保持平视。 ▲
25.(10分)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。请回答下列问题:
 (1)下列说法正确的是 ▲ 。
(1)下列说法正确的是 ▲ 。
A.煤是复杂的混合物,主要含碳元素
B.由煤加工成焦炭发生的是物理变化
C.家用“液化石油气”就是煤隔绝空气加热得到的产品
D.煤燃烧排放的二氧化硫、二氧化氮是形成酸雨的主要物质
(2)煤的加工产品有很多用途,其中焦炭广泛应用于炼铁。
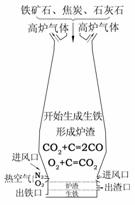
右图是高炉炼铁的示意图。请根据图例回答:
①焦炭在炼铁过程中的主要作用是 ▲ ;
②请用化学方程式表示炼铁的原理 ▲ ;
③高炉炼铁会产生大量的高炉气体,其主要成分是高浓度
的CO和氧化铁尘粒。请你对高炉气体的处理提出合理化
的建议 ▲ 。
(3)化肥厂生产合成氨的原料是煤、空气、水。生产简要流程如下:
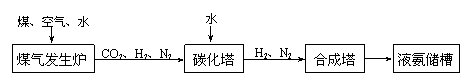
煤气发生炉中主要反应:① C + O2 = CO2;② C + H2O = CO + H2。两个反应必须进行调控才能保持一定的炉温。判断:反应② ▲ (填“放出”或“吸收”)热量。
将合成的氨气部分通入碳化塔,既除去了二氧化碳又得到了化肥NH4HCO3,试写出该反应的化学方程式 ▲ 。
24.(6分)下图中的A→K分别代表初中化学中的常见物质。已知:A、C两物质组成元素相同; G溶液为某物质的稀溶液,G的浓溶液能使小木棍变黑。图中部分生成物未标出。
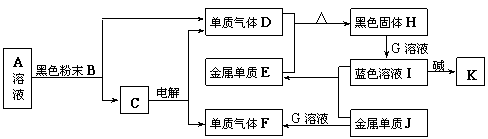
请回答下列问题:
(1)写出J可能的化学式: ▲ (任写一种)。
 (2)写出下列反应的化学方程式:
(2)写出下列反应的化学方程式:
① A C + D: ▲ ;
② F + H → E + C: ▲ ;
③ I + 碱 → K: ▲ (任写一种)。
(3)写出实验室制取D的另一种反应的化学方程式: ▲ 。
23.(4分)将化学知识系统化,有助于对问题的认识。请你参与下列有关分类问题的讨论。
(1)无机化合物可根据其组成和性质进行分类。在K、H、O、N四种元素中任意选择三种组成合适物质,将其化学式分别填在下面②、⑥的横线上。

请将上面③、④两种碱继续分类,可分为 ▲ 。
(2)化学反应之间、化学物质之间具有包含、并列、交叉等关系。下表中X、Y符合下图所示关系的是 ▲ (选填下列表中选项)。
|
|
A |
B |
C |
D |
|
X |
化合反应 |
置换反应 |
化合物 |
钠盐 |
|
Y |
氧化反应 |
复分解反应 |
氧化物 |
碳酸盐 |

22.(4分)(1)汽油与酒精分别加入蒸馏水中,能形成溶液的是 ▲ 。
(2)白糖固体放入口中有清凉感觉。请从溶解现象推测其可能原因是 ▲ 。
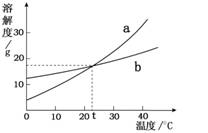 (3)右图是a、b两种固体物质的溶解度曲线。
(3)右图是a、b两种固体物质的溶解度曲线。
① 当温度低于20℃时,溶解度:a ▲ b
(选填“>”“<”或“=”);
② t℃时,将a、b两物质的饱和溶液均加热至
40℃(a、b不分解,水分未蒸发),两种溶液中
溶质的质量分数:a ▲ b(选填“>”“<”或“=”)。
21.(6分)(1)历史上,道尔顿认为,原子是一个个简单的、不可分割的实心球体。现在你认为
该观点 ▲ (选填“正确”或“错误”)。
|
示意图分别表示为:
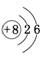
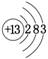
右图是元素周期表的一部分(数字表示相应元
素的原子序数),请用元素符号将两种元素填入表中相应位置。
(3)上表中硫元素的每个原子需要得到 ▲ 个电子形成相对稳定结构的离子,该离子与Na+形成化合物的化学式为 ▲ 。
(4)亚氯酸钠(NaClO2)是一种重要的消毒剂,其中氯元素的化合价为 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com