
3.用分子的知识解释下列现象,正确的是
A.缉毒犬能根据气味发现毒品,是由于分子不断运动
B.石灰石能被研磨成粉末,说明分子很小
C.变瘪的乒乓球放入热水中能鼓起来,是由于分子受热变大
D.降温能使水结成冰,是因为在低温下水分子静止不动
2.达菲是抗击甲型H1N1流感的有效药物,合成达菲的重要中间体为莽草酸(化学式C7H10O5)。下列有关莽草酸的说法不正确的是
A.莽草酸是一种有机化合物 B.莽草酸中氧元素的质量分数为50%
C.莽草酸由三种元素组成 D.莽草酸分子中C、H、O的原子个数比为7∶10∶5
1.“关爱生命,拥抱健康”是永恒的主题。下列做法有利于身体健康的是
A.为避免受到黄曲霉毒素的伤害,霉变的花生米可以油炸后食用
B.常食新鲜水果和蔬菜,保证人体有充足的维生素
C.食品厂用CuSO4溶液浸泡粽叶,使粽叶变得鲜绿
D.使用聚氯乙烯薄膜包装食品
29.(8分)有三种白色粉末,分别是碳酸钠、碳酸钙和氯化钠中的一种。请设计一个实验方案,把这三种粉末区分开来。叙述实验操作、预期现象和结论。
|
实验操作 |
预期现象与结论 |
|
|
|
|
|
|
28.(12分)实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气。
(1)查阅资料。
20℃时不同质量分数硫酸的密度(g/mL)
|
质量 分数 |
0% (纯水) |
1% |
4% |
10% |
16% |
24% |
32% |
36% |
44% |
49% |
60% |
98% |
|
密度 |
1.00 |
1.01 |
1.02 |
1.07 |
1.11 |
1.17 |
1.24 |
1.27 |
1.34 |
1.39 |
1.50 |
1.84 |
分析以上数据,可以得出结论(写2条)
① ;
② ;
(2)计算。
配制200g24.5%的稀硫酸,需 g98%浓硫酸和 g水。实际操作时,取98%浓硫酸 mL(精确到1mL);
(3)配制稀硫酸。
分别用量筒量取所需水和浓硫酸,先将 倒入烧杯中,然后
;
(4)制取氢气。
①下图中可用于制取、收集氢气的装置是(填字母) ;
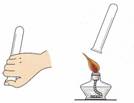
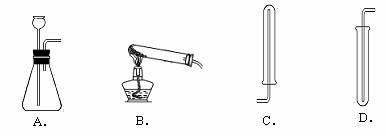
②检验氢气纯度的方法如图所示,标明氢气不纯的现象
是 。
27.(7分)某同学设计下表所示实验,探究金属铜对H2O2分解速率的影响。
|
操作 |
装置 |
 现象 现象 |
|
1、取一小块铜丝网,卷成筒形,固定在铜丝上。 |
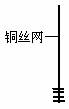 |
|
|
2、分别向①和②中注入15mL、30%的H2O2,并放入盛有热水的③中。 |
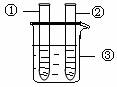 |
约1min后可观察到① 和②中都有少量气泡产生 |
|
3、把铜丝插入①中。 |
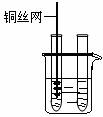 |
①中有大量气泡产生,约5min后不再有气泡产生;此时②中 仍然有少量气泡产生 |
回答下列问题:
(1)仪器的①名称是______________,仪器③的名称是______________;
(2)仪器②中实验的目的是 ;
(3)根据上述实验,可以得出的结论是 ;
(4)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是________。
A.称量实验前铜丝网的质量
B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰
D.将实验后的铜丝网插入AgNO3溶液中
26.(3分)
 (1)用pH试纸测定液体的pH时,所需用品除玻璃片、pH试纸外,还需要______________;
(1)用pH试纸测定液体的pH时,所需用品除玻璃片、pH试纸外,还需要______________;
(2)用量筒量取一定体积液体时,液面如右图所示,该液体的体积
是 mL。
25.(10分)CO2是一种常见的氧化物。
(1)CO2能与碱反应,写出它与Ba(OH)2溶液反应的化学方程式:
(2)CO2有广泛的用途。工业上可用CO2生产小苏打:一定条件下,向饱和氯化钠溶液中通入氨气(NH3)和CO2,即可析出碳酸氢钠固体,此时溶液变浑浊;过滤,滤液中含有氯化铵。该反应的化学方程式是(提示:方程式配平后,物质化学式前的化学计量数均为1)
;
(3)化石燃料燃烧产生大量CO2。大气中CO2含量过高会导致温室效应等环境问题。
①天然气(主要成分为CH4)完成燃烧的化学方程式是 ;
②计算1g CH4完全燃烧产生CO2的质量m(精确到0.01g);
③从下表数据分析,与煤相比,用天然气做燃料的优点是 。
|
|
1g物质完全燃烧产生CO2的质量 |
1g物质完全燃烧放出的热量 |
|
CH4 |
m |
56KJ |
|
C |
3.67g |
32KJ |
24.(5分)A、B、C、D、E五瓶无色透明溶液,分别是HCl溶液、Na2CO3溶液、MgCl2溶
液、NaNO3溶液、NaOH溶液中的一种。分别进行下列实验:
Ⅰ.将A分别滴入B、C、D、E中,均没有明显现象。
Ⅱ.将B分别滴入A、C、D、E中,C、E中均产生白色沉淀,其余没有明显现象。
Ⅲ.将C分别滴入A、B、D、E中,B中产生白色沉淀,D中有气泡冒出,其余没有明显现象。
(1)A是____________,B是____________,C是____________;
(2)B加入E中的化学方程式是____________ ;
(3)C加入D中的化学方程式是____________ 。
23.(6分)将下列两组中的两种反应物混合,回答下列问题:
(1)根据实验事实完成下表(没有发生反应的,化学方程式一栏“/”)
|
编号 |
反应物1 |
反应物2 |
现象 |
化学方程式 |
|
1 |
稀盐酸 |
氢氧化钾溶液 |
没有明显现象 |
|
|
2 |
稀硫酸 |
氢氧化钡溶液 |
有白色沉淀生成 |
|
|
3 |
稀硝酸 |
澄清石灰水 |
|
|
(2)分析上述实验,反应能够发生的共同原因是:反应物1中都含有(填化学用语,下同)___________,反应物2中都含有___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com