
4.下列反应的离子方程式正确的是( )
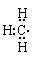 |
D.甲基的电子式为
3.下列有关说法中,错误的是( )
A.NH4H是一种离子晶体,其中氢离子的核外电子排布与氦原子相同
B.在SiO2晶体中,一个Si原子周围有4个Si-O键
C.三种烷烃的沸点高低:丙烷>丁烷>异丁烷
2.下列物质中既能和盐酸反应又能和氢氧化钠溶液反应的化合物是( )
A.Al B.SiO2
C.Al2O3 D.NaHCO3溶液
1.为实现“节能降耗、保护环境”这一目标,下列举措不当的是( )
A.用“绿色化学”工艺,使原料完全转化为产物
B.大量使用农药化肥提高粮食产量
C.推广垃圾的分类存放、回收、处理
D.推广燃煤脱硫技术,防治SO2污染
S:32 Cl:35.5 Fe:56 Cu:64
第I卷(选择题,共50分)
(3)当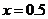 ,溶液中
,溶液中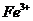 与
与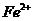 的物质的量相等时,在标准状况共产生672mL气体。求a、b的值。(要有必要的计算过程)
的物质的量相等时,在标准状况共产生672mL气体。求a、b的值。(要有必要的计算过程)
试卷类型:B
唐山市2008―2009学年度高三年级第一学期期末考试
化 学 试 卷
本试卷分第I卷和第II卷,第I卷为选择题,共50分,第II卷为非选择题,共60分,满分110分,考试时间为90分钟。将第I卷选择题的答案涂在答题卡中。
可能用到的相对原子质量:H:
(2)当溶液中金属离子只有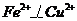 时,则b的取值范围是(用a、x表示)
。
时,则b的取值范围是(用a、x表示)
。
28.(7分)现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为a mol,Cu的物质的量分数为x;研成粉末后,全部投入含b mol HNO3的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)若剩余的残渣只有Cu,则溶液中含有的金属离子为 。(写出所有可能情况)
2SO2(g)+O2(g) 2SO3(g),一段时间后反应达到平衡,生成a mol SO3(g)。
2SO3(g),一段时间后反应达到平衡,生成a mol SO3(g)。
(1)原混合气体与平衡混合气体的压强之比为 。
(2)达到平衡时,SO2和O2的转化率之比为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com