
③当电路中转移0.02 mol 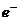 时,阳极质量减小
时,阳极质量减小
④a口产生的是氢气,b口产生的是氧气
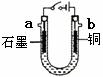 ①电解过程中,阴极区溶液pH增大
①电解过程中,阴极区溶液pH增大
②电解一段时间后U型管内将有蓝色沉淀产生
(3)若A为非极性分子,灼烧B、D、Y时火焰均为黄色。写出D+Y→B的离子方程式
。现将标准状况下
(4)现用右图装置电解某浓度Y的水溶液,则下列叙述中不正确的是(填序号) 。
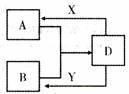 常见的强碱,它们的相互转化关系如右图(部分生成物和水略去)
常见的强碱,它们的相互转化关系如右图(部分生成物和水略去)
(1)若A、B均为气体,在水溶液中反应生成D,其中A具有漂
白性,则A的化学式为 ,B发生催化氧化的化学方程式
为 。
(2)若A、B、D含有相同的金属元素,工业用电解熔融氧化物的
方法制取该金属单质。则此金属元素在周期表中的位置为
。现将X滴入B的溶液中至过量,观察到
的现象是 。
27.(15分)A、B、D、X、Y是由短周期元素组成的化合物,其中X是常见的强酸、Y是
③Z与Fe可组成FeZ2的化合物,是工业制备W的重要原料,假定由FeZ2生成W的每一步原料利用率均为90.0%,请求出用含FeZ2 1.20 t的矿石制备浓度为80.0%的W溶液的质量。(要求写出详细计算过程,结果保留3位有效数字)
②
A.
C.
|