
题目列表(包括答案和解析)
22.(18分)实验题
(1)有一根很细的均匀空心金属管线重约1N、长约50cm、电阻约为30-40Ω,现需测定
它的内径d,已知这种金属的电阻率为ρ。实验室中可以提供下列器材:
A.厘米刻度尺;B.毫米刻度尺;C.螺旋测微器;D.电流表(300mA,约10Ω);E.电流表(3A,约0.1Ω);F.电压表(3V,6KΩ);C.滑动变阻器(200Ω,0.5A);H.滑动变阻器(5Ω,2A);I.蓄电池(6V,0.05Ω);J.开关一个及带夹的异线若干。
请设计一个实验方案,回答以下问题:
①实验中应测物理量的名称及符号是_____________________;
②应选用的实验器材有(只填字母代号):____________________。
③在方框中画出实验电路图并将图中所示仪器连成实际测量电路;
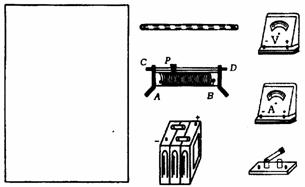
④用测得的物理量和已知的物理常数推导出计算金属管线内径d的表达式。
(2)如图,在很长的水平桌面上放置的弹簧一端固定在墙上,另一端紧靠一木块,并用手
水平向左压住木块,由于弹簧劲度系数很大,故压缩量很小。请利用一架天平、一块秒
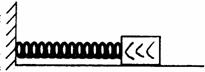 表和一把直尺,测出弹簧的弹性势能。
表和一把直尺,测出弹簧的弹性势能。
①写出测量方法_______。
②推导出根据测量所得的量计算弹性势能的表达式。
21.氢原子的核外电子从距核较近的轨道跃迁到距核较远的轨道的过程中( )
A.原子要吸收光子,电子的动能增大,原子的电势能增大
B.原子要放出光子,电子的动能减小,原子的电势能减小
C.原子要吸收光子,电子的动能增大,原子的电势能减小
D.原子要吸收光子,电子的动能减小,原子的电势能增大
第Ⅱ卷(非选择题 共174分)
20.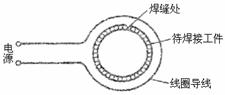 在生产自行车车架等产品时,需要进行焊接操作。如图为一种焊接操作示意图,需要焊接的物体放在线圈导线中间,且与线圈导线绝缘,当线圈导线与电源接通后,使待焊接工件产生电流,由于焊缝处的接触电阻较大,致使温度升高,将金属熔化,焊接在一起。关于这种焊接原理正确的说法是( )
在生产自行车车架等产品时,需要进行焊接操作。如图为一种焊接操作示意图,需要焊接的物体放在线圈导线中间,且与线圈导线绝缘,当线圈导线与电源接通后,使待焊接工件产生电流,由于焊缝处的接触电阻较大,致使温度升高,将金属熔化,焊接在一起。关于这种焊接原理正确的说法是( )
A.电源在线圈中产生较大的恒定电流,该电流流过焊接工件产生较大的焦耳热
B.电流在线圈中产生适当的恒定电流,该电流使焊接工件产生感应电流而产生焦耳热
C.电源在线圈中产生高频交变电流,该电流使焊接工件产生感应电流而产生焦耳热
D.电源在线圈中产生高频交变电流,该电流产生的高频微波辐射,深入焊接工件内部,
产生焦耳热
19.1994年3月,中国科学技术大学研制成功了比较先进的HT-7型超导托卡马克。托卡马克(ToKamak)是研究受控核聚变的一种装置,这个词是torodal(环形的),Kamera(真空室),magnit(磁)的头两个字母以及Katushka(线圈)的第一个宇母组成的缩写词,根据以上信息,下述判断中肯定不正确的是 ( )
A.核反应原理是氢的原子核在装置中聚变成氦粒,同时释放出大量的能量,和太阳发
光的原理类似
B.线圈的作用是通电产生磁场使氘核等带电粒子在磁场中旋转而不溢出
C.这种装置同我国秦山、大亚湾核电站所使用核装置核反应原理相同
D.这种装置可以控制热核反应速度,使聚变能缓慢而稳定的释放
18.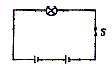 在生活中会遇到这样的事:电筒里的电池用旧了,舍不得扔掉,便装一节新电池配一节旧电池继续使用,测量可以发现新旧电池的电动势确实相差不大,而新旧电池的内阻相差较大,设数据如下:新电池E1=1.5V,r1=1.0Ω,旧电池的电动势仍近似认为E2=1.5V,r1=5.0Ω(实际可能更大),手电筒小电珠为“3V,3W”,如图连接(提示:电池串联E总=E1+E2,r总=r1+r2)以后,下列说法正确的是( )
在生活中会遇到这样的事:电筒里的电池用旧了,舍不得扔掉,便装一节新电池配一节旧电池继续使用,测量可以发现新旧电池的电动势确实相差不大,而新旧电池的内阻相差较大,设数据如下:新电池E1=1.5V,r1=1.0Ω,旧电池的电动势仍近似认为E2=1.5V,r1=5.0Ω(实际可能更大),手电筒小电珠为“3V,3W”,如图连接(提示:电池串联E总=E1+E2,r总=r1+r2)以后,下列说法正确的是( )
A.新电池电源的总功率比旧电池电源总功率大
B.如此连接能更充分地利用旧电池的电能
C.小灯泡的亮度比用一节新电池来供电稍有增加
D.旧电池变成了消耗电能的用电器
17.如图所示,F1、F2等大反向,同时作用在静止于光滑水平面上的A、B两物体上,已知
MA>MB,经过相等时间撤去两力,以后两物体粘为一体,这时A、B将( )
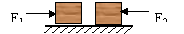 A.停止运动
A.停止运动
B.向右运动
C.向左运动
D.仍运动但方向不能确定
16.如图所示,S点为振源,其频率为100Hz,所产生的横波波速为80m/s,P、Q是波传播
途中的二点,且SP?5.4m,SQ?6.6m,当S通过平衡位置向上运动时 ( )
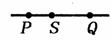 A.P在波谷,Q在波峰
A.P在波谷,Q在波峰
B.P在波峰,Q在波谷
C.P、Q都在波峰
D.P通过平衡位置向上运动,Q通过平衡位置向下运动
15.在冬季,剩有半瓶热水的暖水瓶经过一个夜晚后,第二天拔瓶口的软木塞时感觉很紧,
不易拔出来,这主要是因为 ( )
A.软木塞受潮膨胀 B.瓶口因温度降低而收缩变小
C.白天气温升高,大气压强变大 D.瓶内气体因温度降低而压强减小
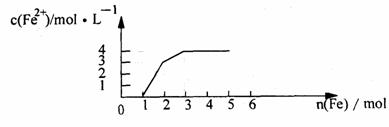
14.某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度
和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3
物质的量浓度之比为 ( )
A.1:1:1 B.1:3:1 C.3:3:8 D.1:1:4
13.下列反应的离子方程式正确的是 ( )
A.将氢碘酸加到Fe(OH)3胶体中:Fe (OH)3 +3H+=Fe3++3H2O
B.碳酸氢钙溶液中中入少量烧碱:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O
C.新制氯水中滴入少量溴化亚铁溶液:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
D.锌与1mol«L-1HNO3溶液反应:Zn+2H+=2 Zn2++H2↑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com