
����Ŀ������������������������ǻ�ѧ���صı�ʾ���ʼ���仯�ķ����������ɷ��ӡ�ԭ�ӻ����ӹ���
��1�����������ɷ��ӹ��ɵ���_____��
A ͭ B ˮ C �Ȼ��� D �Ҵ�
��2����ͼ��ij��Ӧ���̵���ʾ��ͼ�������������ֱ��ʾ���ֲ�ͬ��ԭ��
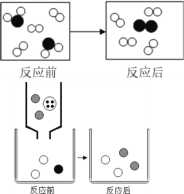
�������Ϸ������߿��л����ʵ�������ͼ�Σ������������Ӧ���̵���ʾ��ͼ_____��
��д��һ������������ʾ��ͼ�Ļ�ѧ����ʽ_____
��3������������Һ�еμ������Ȼ�����Һ��ǡ����ȫ��Ӧ��ʵ��ʱ���Թ۲쵽��������_____����ͼ��ʾ�÷�Ӧǰ����Һ�д��ڵ���Ҫ���ӣ���Ӧ����Һ�к��е�������_____�������ӷ��ţ�
���𰸡�BD 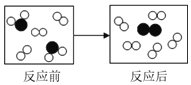 2H2O2
2H2O2![]() H2��+O2�� �а�ɫ�������� Na+��Cl-��H2O
H2��+O2�� �а�ɫ�������� Na+��Cl-��H2O
��������
��1�������ʵĹ��ɿ�֪��ͭ���ڽ�������ԭ�ӹ��ɵģ�ˮ���ɷ��ӹ��ɵģ��Ȼ����������ӹ��ɵģ��Ҵ����ɷ��ӹ��ɵģ�
��2�����������غ㶨�ɷ�Ӧǰ��ԭ�ӵ����༰��Ŀ��֪��Ӧ����һ�����ӣ�����ͼ�� ��
��
�������Ĺ��ɺ���Ŀ��ϵ��֪ˮͨ��ֽ�ķ�Ӧ����������ʾ��ͼ����ѧ����ʽΪ2H2O![]() H2��+O2����
H2��+O2����
��3���������������Ȼ�����Ӧ���������ᱵ�������Ȼ��ƣ���������������Һ�еμ������Ȼ�����Һ��ǡ����ȫ��Ӧ��ʵ��ʱ���Թ۲쵽���������а�ɫ�������ɣ���ͼ2��ʾ�÷�Ӧǰ����Һ�д��ڵ���Ҫ���ӣ���Ӧ����Һ�к��е������У�Na+��Cl-��H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Թ��н�����ʢ�����ˣ��С�����֮�硱֮��������ͼ���������˵IJ���Ӫ���ɷ�,���ͼ�ش�
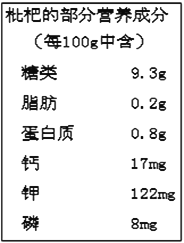
��1��ͼ�еĸƣ��أ�����ָ_____
A���� Bԭ�� CԪ�� D����
��2��ͼ�г���������Ӫ�����е�_____�࣬���ṩ������Ӫ������_____�֡�
��3����������������pHΪ6���ҵ������С���ij������pHΪ3�������������ֲ���ˡ��������ʣ��ȿ����������������ԣ����ܸ�����ʩ�ʵ�������_____��
A��ʯ�� B��ʯ�� C������� D��ľ�ң���Ҫ�ɷ�̼��أ�
��4��С�������������У����������������͵�ʳƷ���������ĭ����(���۰�������ĭ������)������¶���ڳ�ʪ�Ŀ����У��ܿ�������(��Ҫ�ɷ�ΪFe2O3��nH2O)�����з�������˵����ѧ��Ӧ���������������⣬��������_____�仯������ʯ�ұȽϣ���ĭ���۳�����������⣬�����е��ŵ���_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������м��Ҫ�ɷ������������������⣨Fe2O3������������������������ͼ��ʾ��

��1���ڷ�Ӧ���г�����Fe2O3+3H2SO4��Fe2��SO4��3+3H2O��Fe2��SO4��3+Fe�T3FeSO4��������Ӧ�⣬���ᷢ������һ����Ӧ����ѧ����ʽΪ��_____����Ӧ��Ҫ��ǿͨ�磬�Ͻ��̻���ԭ���ǣ�_____��
��2������Ʒ�����������±��գ���ת��ΪFe2O3��SO2��SO3��Ϊ�����SO3�IJ��ʣ�ijʵ��С�������ϵ��̽����ʵ���������£�
��� | ����ͨ����/Ls��1 | �¶�/�� | SO2����% | SO3����/% |
a | 0.02 | 850 | 45.4 | 54.6 |
b | 0.06 | 850 | 30.5 | 69.5 |
c | 0.10 | 810 | 11.1 | 88.9 |
d | 0.10 | 850 | 11.1 | 88.9 |
e | 0.10 | 890 | 11.2 | 88.8 |
����ʵ����Ҫ�о�����Щ���ض�SO3���ʵ�Ӱ��_____��
�������ϱ����ݣ����������в���ʵ��_____�����ţ�����ȡ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�CaO2��������ˮ���������ȶ����ڳ�ʪ������ˮ�л����ų��������㷺Ӧ������ҵ�������ر��������ڳ�;�����У�ͨ����������������ܱյ������ڣ������������������������ܱ�������������������ʱ��ȥ�������CO2�������е�ˮҪ�������ԡ�����������ƺͿ��Խ����Щ���⡣
��1���������ƣ�CaO2���е���Ԫ�صĻ��ϼ�Ϊ_____��
��2���������ƵĹ���ԭ���ǹ������ƿ�����ˮ��Ӧ�����������������ƣ���д������������ˮ��Ӧ�Ļ�ѧ����ʽ_____��
��3��С������ʵ�����ù������ƹ�����ˮ��Ӧ��ȡ������ʵ������з��ֹ���������ˮ��Ӧ����ʼ�н϶�ϸС���ݷų������ų����ݵ����̻�����ԭ�������_____��
��4����ͼ���Դ���ʯ����A12O3������������ˮҲ������������ʣ���Ϊԭ����ȡCaO2������ͼ
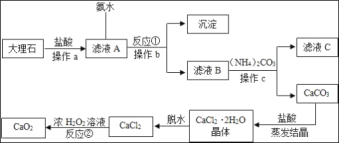
������a��b��c�����ƶ�Ϊ_____��
������ҺC�пɻ��յĸ���Ʒ�Ļ�ѧʽΪ_____������_____�ʡ�
��д����Ӧ���Ļ�ѧ����ʽ_____��
����Ӧ�����ڵ���������������Ũ��Һ��Ͷ����ˮ�Ȼ��ƽ��з�Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ_____��������������_____��
���ڸ����������У���110kg�Ĵ���ʯ�Ƶ���72kg�Ĺ������ƣ���������ǹ����е���Ŀɼ��������ʯ��CaCO3����������Ϊ_____���������һλС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
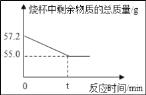
����Ŀ��Ϊ�ⶨij��ʯ��ʯ��Ʒ��̼��Ƶ�������������������ʵ�飻��װ��10.0g ʯ��ʯ��Ʒ���ձ��У�����47.2gϡ���ᣬǡ����ȫ��Ӧ���ձ���ʣ�����ʵ���������ʱ��仯��ϵ��ͼ��ʾ��ʯ��ʯ�е����ʲ��μӷ�Ӧ��������ˮ�����Լ��㣺
��1����ȫ��Ӧʱ���ɶ�����̼������Ϊ_____g��
��2����Ʒ��̼��Ƶ���������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�����Ϊ﮵Ļ�����Σ��㷺���ڲ���������մ����������е����Ӽ���Ҳ���Ʊ�﮵�ص���Ҫԭ�ϡ�̼�������ˮ�е��ܽ�Ⱥ�С����ҵ����﮻�ʯ������Ҫ�ɷ���Li2O������Al2O3��SiO2�����ʣ�Ϊԭ����ȡ̼��﮵����ᷨ����������������
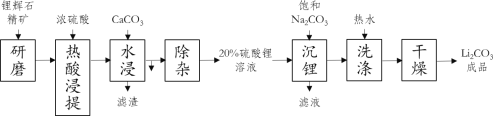
��1��﮻�ʯ�������ǰҪ��������ĥ������Ŀ����_____
��2����ˮ�����м���CaCO3������֮һ��Ϊ�˵���pH=5������Һ�е�Al3+���Al(OH)3����������Ҫȷ����Һ��pHֵΪ5��������pH��ֽ���ⶨ�������������_____
��3����������м����Na2CO3��Һ�DZ�����Һ����������_____����Ӧ�Ļ�ѧ����ʽΪ_____
��4����ϴ������ʹ����ˮ��ԭ����_____��֤��ϴ�Ӹɾ��ķ�����_____
��5��Ϊ��̽�����������������������ʯ��һ�����������4Сʱ���Ԫ�ؽ����ʵ��������±�
��� | ����� | ����Ũ�ȣ�%�� | MgSO4������g�� | �¶ȣ����� | �Ԫ�ؽ����ʣ�%�� |
1 | 1:1 | 90 | 0.00 | 100 | 70.34 |
2 | 1:1 | 98 | 0.00 | 100 | 73.89 |
3 | 1:1 | 98 | 0.00 | 150 | 78.24 |
4 | 1:3 | 98 | 0.00 | 200 | 85.53 |
5 | 1:3 | 98 | 1.25 | 250 | 90.26 |
6 | 1:3 | 98 | 2.50 | 250 | 95.88 |
�ٱ�ʵ���У����Ϊ_____����ʵ����˵���¶ȶ��Ԫ�ؽ����ʵ�Ӱ��
�ڸ����ϱ����ݣ�MgSO4�������Ԫ�ؽ����ʵ�Ӱ����_____
���ڹ�ҵ���������У��൱����������ʹ������˼�ֵ�ϵ͵�Na2SO4�����ʣ��Ӷ�����������ɱ�����ߣ�Ϊ�˽��������ɱ������˾����ܼ�������������⣬������Դ����Ҳ��һ�����棬��ˣ����Լ������ʵ�飬��̽��������Ԫ�ؽ��Ṥ��������������ƺ�������_____������ĸ��
A �����1:2������Ũ��98��MgSO4����0.00���¶�150��
B �����1:2������Ũ��98��MgSO4����1.25���¶�200��
C �����1:2������Ũ��98��MgSO4����2.50���¶�200��
D �����1:2������Ũ��98��MgSO4����2.50���¶�250��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5�֣�ij��ѧ��ȤС���CO2�Ƿ�֧�ֳ���������ȼ�ս���̽�����
���̽����̽��CO2�Ƿ�֧��ʵ���ҳ�������þ��ȼ�ա�
ʵ��٣���ȼ�ŵ�þ���������CO2�ļ���ƿ������þ����ȼ�ա����������ɫMgO�⣬����һ�ֺ�ɫ���塣
��1��þ��CO2�з�Ӧ�Ļ�ѧ����ʽΪ ���˷�Ӧ�Ļ��������� ��
��2��ʵ��ٵĽ����� ���ɸý��ۿ�֪ ��д���ܡ����ܡ�����CO2�����������ý����Ļ��֡�
��3��ͨ��ʵ������ȼ������������ʶ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��Բ�ཻ��������������������֮�����Ӧ��ʾ��ͼ�����жԷ�Ӧ�����˵���У�������ǣ� ��
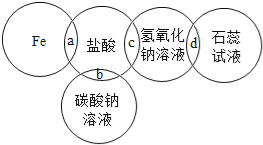
A. a���γ�dz��ɫ��Һ B. b���γɴ�������
C. c����Ӧ���� D. d����Һ�ʺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijδ֪����X���ܺ���CO��CH4�е�һ�ֻ����֣�ijͬѧ���ʵ�����̽����
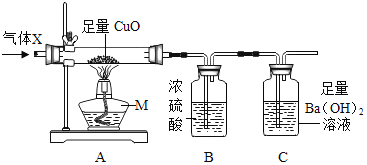
�������ϣ�
������ʱ��CH4����CuO��Ӧ����һ�ֺ�ɫ�������ʡ������������ʽ����С�������
����20��ʱ��Ca��OH��2��Ba��OH��2�ܽ�ȷֱ�Ϊ��0.165g��2.1g
��1������M��������_____��CH4��CuO��Ӧ�Ļ�ѧ����ʽΪ_____��
��2������X�ɷֵIJ�����̽��
����1��ֻ��CO
����2��ֻ��CH4
����3������CO����CH4
��ʵ��ʱ������װ����ͨһ��ʱ���N2����ͨ������X����ȣ�ʵ���������б仯���仯1��A�в������ں�ɫ��ĩ��죬�仯2��Bƿ���ء��仯3��C�г��ֻ��ǡ����ݱ仯_____���1����2����3��������֪����1��������
�����������仯����ȷ������X�ijɷ֣�����Ҫ�ⶨ_____������ţ��������ж����������ܵó����ۡ�
a ʵ��ǰA��CuO������ b Bƿ���ص����� c Cƿ���ص�����
��3�����ۺͷ�˼��
C����Ba��OH��2��Һ������Ca��OH��2��Һ��ԭ����_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com