
【题目】用化学用语填空。
(1)3个氩原子___。
(2)四氧化三铁___。
(3)4个二氧化硅分子___。
(4)汞元素___。
(5)标出SO3中硫元素的化合价___。
【答案】3Ar Fe3O4 4SiO2 Hg ![]()
【解析】
(1)原子的表示方法是用元素符号来表示一个原子,表示多个该原子,在其元素符号前加上相应的数字。3个氩原子表示为3Ar;
(2)四氧化三铁化学式为Fe3O4;
(3) 分子的表示方法,正确书写物质的化学式,表示多个该分子,在其化学式前加上相应的数字。4个二氧化硅分子表示为4SiO2;
(4)汞元素表示为Hg;
(5) SO3中氧元素化合价为-2价,根据化合物中各元素的化合价为零可知,硫元素显+6价,元素化合价的表示方法是确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后。SO3中硫元素的化合价表示为:![]() 。
。


 名题金卷系列答案
名题金卷系列答案科目:初中化学 来源: 题型:
【题目】工业上用石灰石等物质为原料制备轻质碳酸钙,主要流程如图所示。

(1)“石灰窑”中发生反应的化学方程式是_____。
(2)碳化塔中发生反应的化学方程式为_____。
(3)从碳化塔中分离出轻质碳酸钙的操作是_____。
(4)下列说法正确的是_____。
A 窑气是纯净物
B 浆池的作用之一是分离生石灰中的杂质
C 得到的轻质碳酸钙比石灰石中碳酸钙的纯度高
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两物质的溶解度曲线如图所示。下列叙述中,正确的是( )
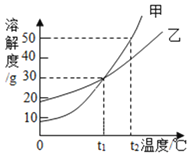
A. 甲溶解度一定大于乙溶解度
B. ![]() 时,甲和乙的饱和溶液中溶质质量分数相等
时,甲和乙的饱和溶液中溶质质量分数相等
C. ![]() 时,在100g水中放入60g甲,其溶质的质量分数为
时,在100g水中放入60g甲,其溶质的质量分数为![]()
D. ![]() 时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面的科普材料。
在人类社会的发展过程中,金属起着重要的作用。从五千年前使用的青铜器,三千年前进入铁器时代,直到20世纪铝合金成为仅次于铁的金属材料,金属材料对于促进生产发展、改善人类生活发挥了巨大的作用。
金属材料包括纯金属和它们的合金。合金具有许多优良的物理性质、化学或机械性能,在许多方面不同于各成分金属。例如:合金的硬度可以大于它的纯金属成分,熔点也可以低于它的成分金属。而且,使用不同的原料,或原料的配比不同,就可以得到具有不同性能的合金。
青铜是我国使用最早的合金。东汉铜奔马身高34.5厘米,身长45厘米,宽13厘米,重7.15千克。形象矫健俊美,别具风姿。充分体现了我国光辉灿烂的古代科技。除青铜外,常见的还有黄铜(含锌及少量的锡、铅、铝等)和白铜(含镍、锌及少量的锰)等合金。
除少数金属外,大多数金属在自然界中都是以化合物的形式存在。为了能够提供人类所需的金属材料,就需要将金属从矿石中冶炼出来。我国古代就发明了湿法炼铜的方法,就是用铁将铜从硫酸铜溶液中置换出来,我国是最早使用该方法的国家。
随着科技水平和冶炼工艺的不断提高,目前,常见的冶炼方法主要有以下几种:
冶炼方法 | 反应表示式(其他生成物略去) | 代表性金属 |
热还原法 | 金属A的氧化物+碳(或一氧化碳等) | 锌、铜 |
电解法 | 金属B的化合物 | 镁、铝 |
热分解法 | 金属C的氧化物 | 汞、银 |
工业上就是利用一氧化碳还有赤铁矿冶炼得到金属铁。
金属材料应用广泛。钛合金是一种性能非常优越的金属,它的化学性质稳定,耐腐蚀,尤其是抵抗海水腐蚀能力很强,目前广泛用于飞机、火箭、导弹、人造卫星和宇宙飞船等领域。
人类每年要从自然界提取数以亿吨计的金属的同时,大量的金属却因腐蚀而报废。每年因腐蚀而报废的金属设备和材料相当于年产量的20%﹣40%.防止金属的腐蚀已成为科学研究和技术领域中的重大问题。回答下列问题:

(1)金属可以做炊具,利用了金属的___性。
(2)赤铁矿石属于___(填“纯净物”“混合物”。)
(3)根据材料,写出工业用氯化镁冶炼镁的化学方程式___。
(4)为了防止金属腐蚀,可以在金属表面附着保护膜,其原理是___。
(5)下列方法,不能鉴别黄铜和纯铜的是___。
A 刻划法 B AgNO3溶液 C HCl D NaNO3溶液
(6)现将一定量的Zn、Fe 投入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后,过滤得到滤渣和滤液。向滤渣中加入稀硫酸,无明显现象,则溶液中可能有的物质是(写化学式)___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸亚铁(FeCO3)是生产补血剂的原料。如图是某同学设计的利用铁矿烧渣(主要成分是Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图:
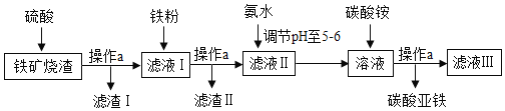
请回答下列问题。
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和______,玻璃棒的作用是______。
(2)滤液Ⅰ中含有的金属阳离子:Fe2+、______(填离子符号)。
(3)滤液Ⅰ中加入铁粉后可能发生的化学反应方程式:
①Fe+Fe2(SO4)3=3FeSO4;②______。
(4)“调节滤液Ⅱ的pH”的操作:用______测定加入氨水后溶液的pH。
(5)加入碳酸铵得到碳酸亚铁反应的化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂废水中含碳酸钠(易溶于水),造成水体污染。化学兴趣小组设计废水处理和利用的方案,进行了如下实验:取过滤后的水样200g,逐滴加入稀盐酸至恰好不再产生气体为止,反应过程中生成气体与所加稀盐酸的质量关系如图所示。请回答下列问题(碳酸钠与盐酸反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑,不考虑水样中杂质的影响):
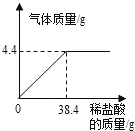
(1)反应生成CO2气体的质量是_____g;
(2)求废水中碳酸钠的质量分数。____(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据下列化学符号中数字“2”所表示的意义,把符合题意的序号填在横线上:
①Mg2+②CO2 ③2CO ④![]() ⑤2NO3﹣
⑤2NO3﹣
(1)表示一个离子所带电荷的是_____;
(2)表示分子个数的是_____;
(3)表示一个分子中所含原子数目的是_____;
(4)表示物质中某元素的化合价的是_____;
(5)表示离子个数的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数一定的氯化钠溶液。下列说法正确的是( )
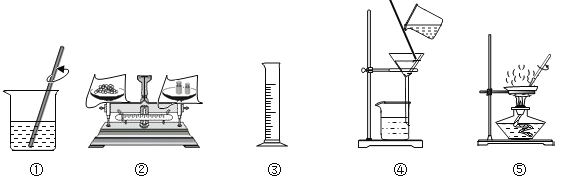
A. 乙实验在操作③时,若俯视读数,会使所配制溶液的溶质质量分数偏小
B. 甲实验三步骤中都要用到玻璃棒,且①和⑤中玻璃棒的作用是相同的
C. 甲实验和乙实验都要用到的实验操作①
D. 甲实验在操作⑤时,将水全部蒸发后停止加热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com