
ijͬѧ�ڲμ�ѧУ��չ���ۺ�ʵ����У�������ѧУ����һ�һ������ڡ�����ж���ǰ�����ˮ���������������ж����ǹ��ұ���̫������ˮ��Դ����ȡ��ר���ж�������ͬѧ�ڿ���������ռ������������ϣ��ٸû������ŷŵ���ˮ����Ҫ�ɷ������ᡢ��ȡδ��������ˮˮ������pH��ֽ���pH=3��
�ڴ�����ˮ����֮һ�ǣ���ˮ�����кͳؽ����кʹ��������õIJ����ǽϾ��õ�ʯ��ˮ��
����ȡ��������������ŷŵ�ˮ�������pH��7���ң�
���������ṩ�����ϣ��ش��������⣺
��1����ͬѧ�����ֿ��������������飨��ֱ�ӻ��ӣ�
��2��Ҫ�����ˮ�����ȣ�������pH��ֽ����ѡ��������������
A����ָ̪ʾ������ B���к͵ζ� C����ɫʯ����Һ����
��3���������֪pH=3����ˮ�У��������������Ϊ0.00365%���ּ����кͳ�����1.0��106kg��ˮ����ˮ���������ʾ������������Ʒ�Ӧ����������Ҫ����ǧ���������Ʋ�����ȫ�кͣ�
�����㡿�ᡢ���Է�ˮ�Ĵ�����
����������������������кͷ�Ӧ���ͷ�ˮ�����ԣ���ˮ�е���Ҫ�ɷ������ᣬ��ʯ��ˮ�����кʹ����������Ȼ��ƺ�ˮ���Ӷ�������Ⱦ��
��1������ֱ�ӵõ�������������û�ѧ�����õ���
��2�������ˮ�����ȣ��й̶���ֵ��A��C��ֻ�ܴ��Թ��ƣ����к͵ζ����Եó���ȷ��ֵ��
��3����������к͵ķ�Ӧ���Լ���õ���
����𡿽⣺��1�����������֪���Ѽ����ϣ�������ѧ�ķ��������п��죬�ʴ�Ϊ����ӣ�
��2����Ҫ�����ˮ�����ȣ�ѡ����ֻ���к͵ζ����Բ��ȷ��ֵ����ѡB��
��3������ȫ�к���Ҫ�������Ƶ�����Ϊx����
Ca��OH��2+2HCl�TCaCl2+2H2O
74 2��36.5
x 1.0��106kg��0.00365%
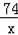
 �T
�T

��ã�x�T37kg
����Ҫ37ǧ���������Ʋ�����ȫ�кͣ�
��


 �Űٷֿ�ʱ����ϵ�д�
�Űٷֿ�ʱ����ϵ�д� ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��۲�ͼ������ͼʾ�ش��������⣮
��1��ͼA��֪Mg�ĺ˵����Ϊ������þԪ�ص����ԭ������Ϊ������
��2��ͼB��ʾ���� ��ѡ��������ǽ�������Ԫ�ص�ԭ�ӣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�û�ѧ������գ�
��1��2����ԭ��������2��������������3��̼���������
��4���ؿ��к�������Ԫ�������� ��5��������������Ԫ����+3�ۣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾ�����ߵ��ᡢ���֮����Է������ֽⷴӦ���±��ṩ���������ʷ�����ͼҪ����ǣ�������
| ���� ��� | �� | �� | ��1 | ��2 |
| A | H2SO4 | Ca��OH��2 | BaCl2 | K2CO3 |
| B | H2SO4 | KOH | Na2CO3 | Ba��NO3��2 |
| C | HCl | NaOH | K2CO3 | BaCl2 |
| D | H2SO4 | Ba��OH��2 | Na2CO3 | CuSO4 |


A��A B��B C��C D��D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
С��ͬѧ��ѧϰ��ø��֪ʶ����ϵ�������ؽ����ж��¼�����������Լ���һ�����룺ø�Ĵ����ÿ��ܻ��ܵ��ؽ������ӵ�Ӱ�죮��ϲ���С�ս���������̽����
���������ϡ�ͭ�����ؽ������Ʋ����ؽ�����
�����ʵ�顿ȡ�Թ�4֧����ţ������ֱ�����Լ���ҡ�ȣ�Ѹ������37���ˮԡ�У�10���Ӻ�ȡ������ȴ��ֱ�����Һ3�Σ��۲�����ɫ�仯��
| ��� | 0.25%������Һ��ml�� | ����ˮ��ml�� | 0.9%NaCl��Һ��ml�� | 0.9%CuSO4��Һ��ml�� | ��Һ��Һ��ml�� | �����Һ3�κ����� |
| 1 | 3 | 2 | �� | �� | �� | ����ɫ |
| 2 | 3 | 1 | �� | �� | 1 | ������ |
| 3 | 3 | �� | 1 | �� | 1 | ������ |
| 4 | 3 | �� | �� | 1 | 1 | ����ɫ |
ʵ����ۡ�ø�Ĵ�����������
�������뽻����
��1��ʵ�������ΪʲôҪ��37���ˮԡ�н��У�����
��2��С��ͬѧ�������������ǣ�ø��һ�������������ؽ������ӻᷢ�����ʸı䣮������ࡱ����֬�������������ʡ�����
��3���ڿ���С�յ���Ƽ�ʵ���ͬ����С����Ϊƾ����ʵ�黹������֤��С�յIJ��룮����ΪС�����������ʵ��Ľ��������е��ǣ�����
�ף�������ͭ��Һ�������Ȼ�ͭ��Һ �ң����Ȼ�����Һ��������������Һ
����������ͭ��Һ����������ͭ��Һ �������Ȼ�����Һ��������������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Һ���ճ�������Ӧ�ù㷺�����ж���Һ���й�˵����ȷ���ǣ�������
A����Һ������ɫ������Һ�� B����Һ��ֻ����һ������
C����Һ�и������ܶȲ�ͬ D����Һ�и�����������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�û�ѧ������գ�
��Ԫ��������2��������������һ��������������������������Ԫ�صĻ��ϼ�����
��2����Ȼ������Ҫ�ɷ��Ǽ���д��������ȫȼ�յĻ�ѧ����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��AgNO3��Zn��NO3��2��Cu��NO3��2�Ļ����Һ�м���һ���������ۣ���ַ�Ӧ����ˣ��������м���ϡ���ᣬ�����ݲ��������������������н�����ȷ���ǣ�������
A��������һ����Zn B�������п�����Ag��Cu
C����Һ�Щ�����Fe��NO3��2��Zn��NO3��2 D����Һ�п�����AgNO3��Cu��NO3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������������������Ҫ���壬��ˮ��Һ�������ᣨH2SO3�������⣨H2S����һ�־��г�������ζ�ľ綾���壬��ˮ��Һ�������ᣮ��֪��ͬ�������£���������������������ᣮ���������͵���������Һ��ͨ��������������壬��Ӧ�Ļ�ѧ����ʽΪ��2H2S+H2SO3=3S��+3H2O������ͼ����Һ��pH��ͨ����������ı仯����ʾ��ͼ��ȷ���ǣ�������
A��
 B��
B��
 C��
C��
 D��
D��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com