
����Ŀ��ij��ȤС�鰴�տα�ʵ�鷽����ͼ����ľ̿������ͭ��Ӧʵ��ʱ�����ֺ��ѹ۲쵽�Ϻ�ɫͭ�����ɣ�ȴ�����а���ɫ������֡����Ǿ��������ʵ�����̽���Ľ���

��������⣩����ɫ�Ĺ�����ʲô�����ѡ����ʵ�������ʹľ̿��ԭ����ͭ��ʵ����������ԣ�
�����ϣ�ͭ��+1��+2���ֻ��ϼۣ�ͨ������£����Ļ��ϼ�Ϊ��2��̼�Ļ��ϼ�Ϊ+4��4��
��1��д��ľ̿��ԭCuO�Ļ�ѧ����ʽ_____��
����������裩
��2��ͬѧ����Ϊ���ְ���ɫ���������һ��ͭ�Ļ�������²����Ļ�ѧʽΪ_____��
��3��ͬѧ�ǻ���Ϊ��ͨ���ı䷴Ӧ���״̬�������ȣ��Լ���Ӧװ�ã�����ʹ��ʵ������������ԣ����ٳ��ְ���ɫ����������
�������뽻����
��С�⽨���ó�ϸ̿��������ͭ��ĩ����ʵ�顣����Ϊ���������ԭ����_____��
��С�ܽ�����ͼ��װ�������װ�á������Ƚϣ���װ���н��Թ�ֱ�����õ�������_____��
��4����ʵ������ۣ�
ͬѧ�Ǿ������Ľ���ķ�������ʵ�飬�����ڼ�������װ�õ�_____�����Թ��м����Ѹ����ҩƷ����ʼ���ȣ������������ʯ��ˮ���ֻ���ʱ������ȷ������ͭ��̿���Ѿ���ʼ��Ӧ��д������ʯ��ˮ����ǵ�ԭ��_____���û�ѧ����ʽ��ʾ�������ã����ɿ����Թܵײ�����ȣ�ֹͣ���Ⱥ����ܿ��������������Թܵײ����¶������ӣ��������˵���÷�Ӧ��_____���������������������ȷ�Ӧ������Ӧ�������Ƚ������ܴ�ʯ��ˮ��ȡ����Ȼ��ر�ֹˮ�У��ò�����Ȼ��ȴ�������ر�ֹˮ�У����ܳ��ֵ�������_____����������ȴ��ͬѧ�������ҵ����ڴ����õ��Ϻ�ɫͭ�飬ʵ������Բ���ɹ���
���𰸡�2CuO+C![]() 2Cu+CO2�� Cu2O��Cu4C��Cu2C�� ��ϸ̿��������ͭ��ĩ�Ӵ�������� �����ڼ��м��ȣ���ó������� �����ԣ� CO2+Ca��OH��2��CaCO3��+H2O�� �ţ� ��������뷴Ӧ���Թ��У�ʹ���ɵ���Ȼ���ȵ�ͭ���±�����
2Cu+CO2�� Cu2O��Cu4C��Cu2C�� ��ϸ̿��������ͭ��ĩ�Ӵ�������� �����ڼ��м��ȣ���ó������� �����ԣ� CO2+Ca��OH��2��CaCO3��+H2O�� �ţ� ��������뷴Ӧ���Թ��У�ʹ���ɵ���Ȼ���ȵ�ͭ���±�����
��������
��1������ͭ��̼�ڸ����·�Ӧ����ͭ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ2CuO+C![]() 2Cu+CO2����
2Cu+CO2����
��2����Ϊͭ��+1��+2���ֻ��ϼۣ�ͨ������£����Ļ��ϼ�Ϊ��2��̼�Ļ��ϼ�Ϊ+4��4�����ݻ�������Ԫ�صĻ��ϼ۴�����Ϊ���ԭ����ɫ����Ļ�ѧʽ����Ϊ��Cu2O��Cu4C��Cu2C����
��3����С�⽨���ó�ϸ̿��������ͭ��ĩ����ʵ�飬���������ԭ���dz�ϸ̿��������ͭ��ĩ�Ӵ��������
�������Ƚϣ���װ���н��Թ�ֱ�����õ������ǣ������ڼ��м��ȣ���ó������£�
��4��ʵ��ʱ����Ҫ���װ�õ������ԣ�����ʯ��ˮ����ǵ�ԭ���Ƕ�����̼��ʯ��ˮ��Ӧ���ɰ�ɫ̼��Ƴ�����ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+Ca��OH��2��CaCO3��+H2O��ֹͣ���Ⱥ����ܿ��������������Թܵײ����¶������ӣ��������˵���÷�ӦҪ�ų���������Ӧ������Ҫ�ر�ֹˮ�У������ر�ֹˮ�У����ܳ��ֵ������ǣ���������뷴Ӧ���Թ��У�ʹ���ɵ���Ȼ���ȵ�ͭ���±�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ˮ��������������أ������ÿ��ˮ������������3mgʱ����ͻ���������������(CaO2)��һ�ֻ�ѧ����������Ӧԭ����2CaO2+2H2O��2Ca(OH)2+O2������7.2g�Ĺ������Ƽ���װ��500Lˮ������С�ͨ������ش�(д���������)��
(1)��ȫ��Ӧʱ������������������_______��
(2)���ɵ�������ȫ����ˮʱ�������ÿ��ˮ����������_____mg��_____(����������������)�������Ҫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ�ش����⣺

��1��д�����������ƣ�A��_____ B��______
��2���ⶨ�������������������ʵ�飬����˵���У�����ȷ����_____������ĸ��ţ���
A��ʵ��ʱ������������Ӱ�����ս�� B��ʵ��ǰ��Ӧ�ȼ���װ�õ�������
C����ȼ����ǰ�����õ��ɼмн���Ƥ�� D������Ϩ���Ӧ�������ɼ�
��3��þ�ڵ�����ȼ�����ɵ���þ����Ԫ�صĻ��ϼ�Ϊ��3�ۣ���д����Ӧ�Ļ�ѧ����ʽ��____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��Ϊ�ⶨij�����(̼��ƺ��Ȼ���)��̼��Ƶĺ���,ȡ�û����11.11g���ձ��У���ε���73gϡ���ᣬǡ����ȫ��Ӧ����¼���й��������±�����������ȫ���������
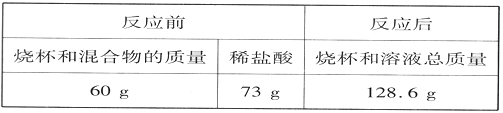
���㣺
��1�����ɶ�����̼������Ϊ___________g
��2���������̼�������Ϊ____________ g(��д���������)
��3����Ӧ������,�ձ��и�Ԫ�ص�����Ϊ_________ g(��д���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȤС��ͬѧΪ�˲ⶨij��̼��Ƶ�������������ȡ25.0g�������Ʒ�������Ĵθ������ա���ȴ������ʣ�������ظ����������ʲ��μӷ�Ӧ������¼�������£�
�������� | ��1�� | ��2�� | ��3�� | ��4�� |
ʣ�����������g�� | 21.6 | 19.2 | 16.2 | 16.2 |
�Լ��㣺
��1����ȫ��Ӧ�����ɶ�����̼��������__g��
��2�����������̼��Ƶ�������������д��������̣�__________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
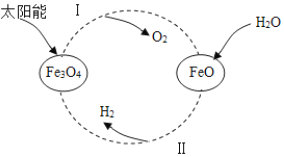
����Ŀ��Ŀǰ����ʹ�õ�ȼ�ϴ�����Ի�ʯȼ�ϣ���______��ʯ�͡���Ȼ���ȡ���Ȼ������Ҫ�ɷ��Ǽ��飨CH4����������ȫȼ�յĻ�ѧ����ʽ��______������������������Դ����̫����Ϊ��Դ����������������ѭ���ֽ�ˮ�Ĺ�����ͼ��ʾ��
��1����Ӧ1�Ļ�����Ӧ����Ϊ______��
��2��д����һ�������·����ķ�Ӧ��Ļ�ѧ����ʽ______��
��3��������ѭ�������У����յõ��IJ�Ʒ��______��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ�ã������ѧ֪ʶ�ش����⡣
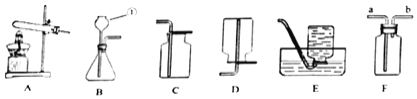
![]() ��������ٵ�������______��
��������ٵ�������______��
![]() ����������______����ʹ��Fװ���ռ�����������Ӧ�ô�______�ڽ���
����������______����ʹ��Fװ���ռ�����������Ӧ�ô�______�ڽ���![]() �a����b��
�a����b��![]() ��
��
![]() ʵ����ѡ��װ��B��C��ȡ������̼����Ӧ�Ļ�ѧ����ʽ�ǣ�______�������ķ�����______�������ռ�������ͨ����ɫʯ����Һ�У�������������______��
ʵ����ѡ��װ��B��C��ȡ������̼����Ӧ�Ļ�ѧ����ʽ�ǣ�______�������ķ�����______�������ռ�������ͨ����ɫʯ����Һ�У�������������______��
![]() �����н���������Ȼ��ȡů����Ȼ������Ҫ�ɷ��Ǽ��飬ijͬѧͨ���������ϣ�֪��ʵ�������ˮ�����ƹ�������ʯ�Ҽ�����ȡ���飬ͨ������¼�����ܶȱȿ���С��������ˮ��ʵ������ȡ����ѡ��ķ���װ����______
�����н���������Ȼ��ȡů����Ȼ������Ҫ�ɷ��Ǽ��飬ijͬѧͨ���������ϣ�֪��ʵ�������ˮ�����ƹ�������ʯ�Ҽ�����ȡ���飬ͨ������¼�����ܶȱȿ���С��������ˮ��ʵ������ȡ����ѡ��ķ���װ����______![]() ����ĸ
����ĸ![]() �����ռ�����ļ��������ѡ��______װ��
�����ռ�����ļ��������ѡ��______װ��![]() ��
��![]() ��ѡ��
��ѡ��![]() �������ʹ����Ч�ظ����˿���������������ȫȼ�յĻ�ѧ����ʽ��______��
�������ʹ����Ч�ظ����˿���������������ȫȼ�յĻ�ѧ����ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ķ����к��д���CuS�������������Ļ������ҵ���Ը÷���Ϊԭ������CuCl2����������:
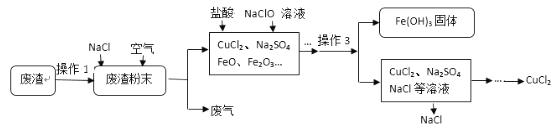
��1������1�ǣ����飬�����������Ŀ����_____________________________��
��2������3��������_________�����������������__________________��
��3�� ��֪CuS��������Ӧ�������ֳ��������д����ѧ����ʽ__________________��
��4���������������п�ѭ�����õ�������__________��NaClO����Ԫ�ػ��ϼ�____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͻ��н����и��ʱ��ʹ�õ���Ȳ��(��Ȳ��������ȼ�ղ����Ļ���)��
(1)��ѧ��Ӧ�������������仯����Ȳȼ���ǻ�ѧ��ת��Ϊ____�ܣ�
(2)��Ȳ�����ȼ�գ������____��ˮ���ɼ���Ȳ�����ȼ�ռ��˷�ȼ������Ⱦ������Ϊ��ʹ��Ȳ���ȼ�գ����������____��
(3)�ڵ�ȼ��Ȳ(C2H2)ǰ������____���Է�ֹ������ը����д��C2H2���ȼ�յĻ�ѧ����ʽ____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com