
【题目】NaCl是重要的工业原料,工业上可用电解饱和食盐水的方法获取烧碱、氯气、氢气等物质。实验小组的同学现欲对一份久置的工业烧碱的成分进行探究。
(查阅资料)电解饱和食盐水的化学方程式为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(提出问题)小组同学根据相关信息,对工业烧碱的成分作了如下猜想:
猜想一:NaOH、NaCl
猜想二:Na2CO3、NaCl
猜想三:_________________;
(实验探究)
为了验证猜想,小组同学进行了实验探究。首先取工业烧碱样品少许,配成溶液,待用。
(1)取样品溶液少许,滴加足量稀盐酸,有气泡产生,说明样品中含有________(填化学式),写出产生气泡的化学反应的方程式_________________;工业烧碱中含有该物质的原因是________(用化学方程式表示)。
(2)为了证明样品中含有NaCl,小组同学设计实验方案如下:先取样品溶液少量,向其中滴加足量的稀盐酸至不再产生气泡时,再向溶液中滴加AgNO3溶液,出现白色沉淀,加入稀硝酸后,沉淀不溶解,则样品中一定含有氯化钠。老师指出上述方案不合理,请说明理由_____;
(3)小组同学为进一步确认样品是否还含有氢氯化钠,设计了如下实验方案,请你将其补充完整。
实验操作步骤 | 实验现象 | 实验结论 |
①取样品溶液少许,加入足量氯化钙溶液,充分反应后静置 ②取反应后的溶液适量,滴加无色酚酞试液 | ①___________ ②____________ | 该样品中一定含有NaOH |
(反思与评价)
经过研究,小组同学认为,上述方案中,除了使用氯化钙以外,利用下列物质也可得到同样的效果,你认为下列哪些试剂是可行的_________(填序号)。
A Ca(OH)2 B Ca(NO3)2 C Ba(NO3)2 D Ba(OH)2
(数据处理)
最终实验证实,该久置工业烧碱样品中含有氢氧化钠、氯化钠和碳酸钠。为了进一步确定该混合物中Na2CO3的质量分数,实验小组的同学取了10克该工业烧碱样品,加入足量的溶质质量分数为7.3%稀盐酸,实验测得生成CO2气体的质量与所加盐酸质量关系如图所示,请据图计算:
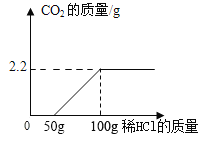
(1)该样品与稀盐酸完全反应时产生CO2的质量是____g。
(2)该样品中Na2CO3的质量分数____。
【答案】NaOH、Na2CO3、NaCl Na2CO3 ![]() 2NaOH+CO2═Na2CO3+H2O 过量的稀盐酸、生成的氯化钠能和硝酸银反应生成白色沉淀氯化银 没有产生白色沉淀 溶液变红 BC 2.2 53%
2NaOH+CO2═Na2CO3+H2O 过量的稀盐酸、生成的氯化钠能和硝酸银反应生成白色沉淀氯化银 没有产生白色沉淀 溶液变红 BC 2.2 53%
【解析】
[提出问题]根据猜想一:NaOH、NaCl和猜想二:Na2CO3、NaCl,可推出猜想三是:NaOH、Na2CO3、NaCl;
(1)取样品溶液少许,滴加足量稀盐酸,观察到有气泡产生,说明样品中含有碳酸钠,这是因为碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,化学反应的方程式![]() ;氢氧化钠必须密封保存,否则和二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
;氢氧化钠必须密封保存,否则和二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
(2)老师对该结论提出了质疑,认为不一定含有氯化钠,理由是过量的稀盐酸、生成的氯化钠能和硝酸银反应生成白色沉淀氯化银;
(3)①取样品溶液少许,加入足量氯化钙溶液,充分反应后静置,没有产生白色沉淀,说明没有碳酸钠;②取反应后的溶液适量,滴加无色酚酞试液,溶液变红,说明有氢氧化钠;
[反思与评价]硝酸钙、硝酸钡溶液显中性,不能和氢氧化钠溶液反应,能和碳酸钠反应生成碳酸钙或碳酸钡沉淀和硝酸钠,硝酸钠溶液显中性,所以硝酸钙或硝酸钡溶液能代替步骤①中的氯化钙溶液;加入氢氧化钙溶液时,因为氢氧化钙或氢氧化钡溶液显碱性,能使酚酞试液变红色,不能用来验证氢氧化钠是否存在;
[数据处理](1)由图中数据可知,生成二氧化碳的质量是2.2g,
(2)设参加反应的碳酸钠的质量为x,
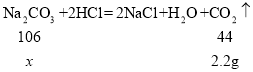
![]()
x=5.3g,
该样品中Na2CO3的质量分数![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下列关于燃烧现象的解释或分析正确的是
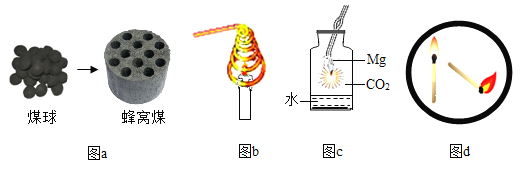
A.图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B.图b中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
C.图c中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
D.图d中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国化学家侯德榜创立了侯氏制碱法,为世界制碱工业作出了突出贡献在实际生产的产品碳酸钠中会混有少量的氯化钠,现有该样品混合物20.4g,将其放入洁净的烧杯中,向其中逐滴滴入7.3%的稀盐酸,放出气体质量与滴加稀盐酸质量的关系如图所示。请回答下列问题:
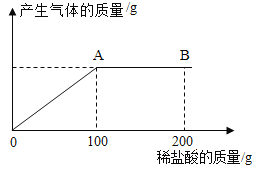
(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH_____7(填“<”“>”或“=”)
(2)该样品混合物中碳酸钠的质量_____g;
(3)当滴加稀盐酸至图中A点时,烧杯中所得溶液为不饱和溶液,请计算此时溶液中的溶质质量分数。(写出计算过程,计算结果保留至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列曲线能正确表达对应的反应或过程的是( )
A. NH4NO3固体溶于水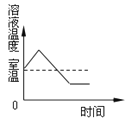
B. 煅烧石灰石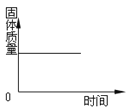
C. 等质量等浓度的稀H2SO4加入金属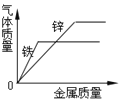
D. CuSO4和H2SO4混合液中加入NaOH溶液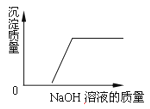
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国研制的一种新型催化剂可将CO2和H2转化为甲醇(CH3OH)和X,该反应的微观示意图如图,下列说法错误的是
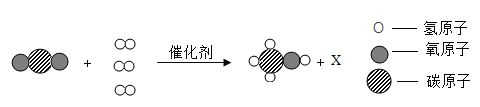
A.X的化学式为H2OB.反应前后原子的种类发生改变
C.化学变化的实质是原子的重新组合D.该反应遵循质量守恒定律
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】控制变量法是实验探究的重要方法.下列设计方案不能实现探究目的是( )
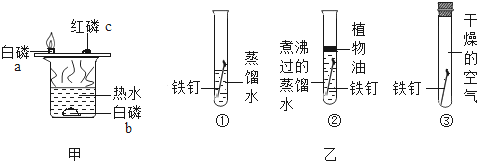
A. 甲实验可探究可燃物的燃烧需要与氧气接触且温度达到着火点
B. 甲实验中a、b对比可探究可燃物的燃烧是否需要达到一定温度
C. 乙中①②对比可探究铁的锈蚀条件是否与氧气有关
D. 乙中①②③对比可探究铁的锈蚀条件是否与氧气和水等物质有关
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
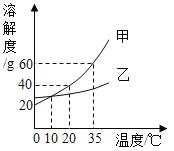
A.甲的溶解度大于乙的溶解度
B.35℃时100g甲的溶液中含甲的质量60g
C.降低温度可使接近饱和的甲溶液变成饱和溶液
D.10℃时甲、乙两种溶液的溶质质量分数一定相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某种手机电路板中含有Fe、Cu、Au、Ag、Ni(镍,银白色金属)等金属,如图是某工厂回收部分金属的流程图。

(1)操作①中,使用的玻璃仪器除烧杯、漏斗外,还需_______________;
(2)写出滤液②中阳离子符号_____________。
(3)根据以上工艺流程图,可以得到Cu、Ni、Fe、H的活动性由强到弱的顺序依次是__________。
(4)已知滤渣①中的铜与稀硫酸、氧气在加热的条件下会生成硫酸铜,写出该反应的化学方程式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com