
【题目】实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
(提出问题1)该样品中含有哪些物质?
(提出猜想)猜想Ⅰ:全部是NaOH;
猜想Ⅱ:已完全变质,该样品中只含Na2CO3;
猜想Ⅲ:部分变质,该样品中含有NaOH和Na2CO3。
(实验探究1)为确定该样品成分,小明设计了如下实验方案,请你一起完成下列实验报告。
实验操作 | 实验现象 | 实验结论 |
①取少量样品溶于水,加入 足量的________; | 白色沉淀产生 | 该反应的化学方程式为 ________ |
②将上述反应后的混合液过滤, 取滤液加入________; | ________ | 证明猜想Ⅲ成立 |
(提出问题2)怎样提纯该样品得到纯净的氢氧化钠固体?
(实验探究2)为得到纯净的氢氧化钠固体,设计的实验过程如下图。请回答下列问题

⑴长期暴露在空气中的氢氧化钠固体样品极易变质,原因是________(用化学方程式表示)。操作B的名称为________,所需的玻璃仪器有________、烧杯和玻璃棒。
⑵该实验中发生反应的化学方程式为________。
⑶最终所得氢氧化钠固体质量________(选填“<”、“=”或“>”)变质后样品中氢氧化钠的质量。
(实验探究3)为了测定NaOH的纯度,某同学设计如图装置。
已知:CO2在饱和碳酸氢钠溶液中几乎不溶解。

⑷B中集气瓶盛放的饱和碳酸氢钠溶液不能用水代替,其理由是________。
⑸取10g样品进行实验,根据实验数据,通过计算可知产生了CO20.44g,求原样品中NaOH的质量分数,写出计算过程_____________。
【答案】 氯化钡溶液 BaCl2+Na2CO3=BaCO3↓+2 NaCl 酚酞 红 2NaOH+ CO2= Na2CO3+H2O 过滤 漏斗 Ba(OH)2+Na2CO3=BaCO3↓+2 NaOH > 二氧化碳能够溶于水 89.4%
【解析】本题在氢氧化钠的变质后的成分及含量的探究的情境下,考查了碱、盐的化学性质和根据化学方程式的计算。
实验探究1:若猜想Ⅲ成立,则溶液存在碳酸钠和氢氧化钠。氯化钡溶液和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,可用足量的氯化钡溶液检验碳酸钠并完全除去碳酸钠。氢氧化钠呈碱性,能使酚酞变红色,再用酚酞检验氢氧化钠的存在。因此:
实验操作 | 实验现象 | 实验结论 |
①取少量样品溶于水,加入足量的氯化钡溶液; | 白色沉淀产生 | 该反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl |
②将上述反应后的混合液过滤,取滤液加入酚酞; | 溶液变红 | 证明猜想Ⅲ成立 |
实验探究2:
⑴氢氧化钠变质是与二氧化碳反应生成碳酸钠和水;反应方程式为:2NaOH+ CO2= Na2CO3+H2O;操作B得到固体和溶液,所以操作B是过滤;所需的玻璃仪器有漏斗、烧杯和玻璃棒;
⑵碳酸钠能与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,能除去杂质且没有引入新的杂质,方程式为Ba(OH)2+Na2CO3=BaCO3↓+2NaOH;
⑶根据反应看出,变质生成的碳酸钠通过反应生成氢氧化钠,最终所得氢氧化钠固体质量比变质后样品中氢氧化钠的质量多,故填“>”;
⑷本题的实验目的是通过测量二氧化碳的体积来计算药品中碳酸钠的含量,所以必须保证二氧化碳的准确性,因为二氧化碳能够溶于水,所以用饱和的碳酸氢钠水溶液,可以避免二氧化碳溶于水;
⑸设:样品中含碳酸钠的质量为x。
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
106 44
x 0.44g
![]() 解之得:x=1.06g。
解之得:x=1.06g。
样品中碳酸钠的质量分数=![]() ×100%≈89.4%。
×100%≈89.4%。


科目:初中化学 来源: 题型:
【题目】最近,我国研发出了“发电玻璃”,又名叫碲化镉薄膜太阳能电池,其原理是在绝缘的普通玻璃上涂抹上4微米厚的碲化镉光电薄膜,由此制成可导电、可发电的半导体材料。镉元素的信息如下,以下说法正确的是( )

A. 图中x=8
B. 镉元素属于非金属元素
C. 镉原子的中子数是64
D. 镉的相对原子质量是112.4g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的微观示意图,下列说法错误的是
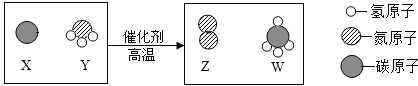
A.化学反应前后原子的种类、个数、质量均保持不变
B.W物质中碳元素的质量分数为75%
C.参加反应的X、Y两物质的粒子个数比为3:4
D.该反应不属于置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料在生产、生活中应用广泛。
(1)图A、B、C是金属属的应用实例,根据这些实例可推断出金属具有的物理性质有____________(需答两点)。

(2)图D中,最容易生锈的部位是___________(填“a”“b”或“c”)。
(3)焊锡(主要含锡、铅)与其组成它的纯金属相比具有_______________的特性,可用来焊接金属。
(4)将纯铜片和黄铜片互相刻画画,纯铜片上留下明显的划痕(实验如图E所示),该实验说明了________________________________.
(5)用磁铁矿(Fe3O4)炼铁的原理是:在高温下,用一氧化碳把铁从磁铁矿里还原出来,该反应的化学方程式为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钡广泛用于陶瓷、光学玻璃等行业。有一种碳酸盐矿石,其主要成分是碳酸钡和碳酸钙,现以此矿石为原料生产碳酸钡,并得到副产品氢氧化钙,其流程如下图所示:
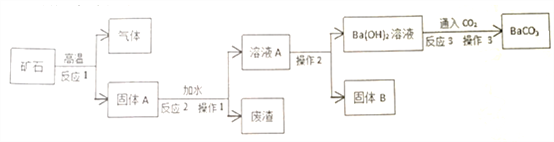
已知,氢氧化钡和氢氧化钙在不同温度下的溶解度是:
温度/℃ | 0 | 40 | 80 |
氢氧化钡溶解度/g | 1.67 | 8.22 | 101.4 |
氢氧化钙溶解度/g | 0.187 | 0.141 | 0.094 |
请回答
(1)碳酸钡与碳酸钙的化学性质相似,高温下能分解成两种氧化物,碳酸钡在高温下分解的化学方程式为______________。
(2)氧化钡与氧化钙的化学性质相似,能与水反应。溶液A中存在的阳离子是___________(写离子符号)。
(3)在实验室里完成操作1,需要用到的玻璃仪器除漏斗、玻璃棒外,还有______________。
(4)操作2采用的操作方法依次为____________(填序号)。
A.过滤 B.降温 C.加热 D.蒸馏 E.灼烧
(5)反应3的化学方程式为___________________________________________。
(6)废渣要经过洗涤后才能弃渣,原因是________________________。
(7)假设该碳酸盐矿石中含有40%的碳酸钙,那么50kg该矿石理论上可制得氢氧化钙的质量是________kg。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化工厂排放的废水含有较多FeSO4,为综合利用FeSO4,他们设计一下工艺流程:
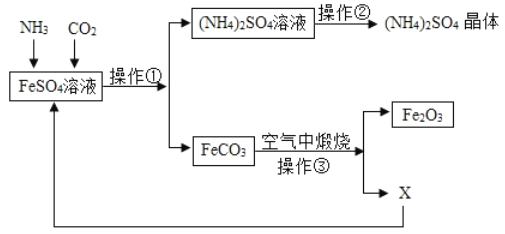
(1)操作![]() 的名称是 ______ ,其中用到的玻璃仪器有玻璃棒、烧杯和 ______ ,
的名称是 ______ ,其中用到的玻璃仪器有玻璃棒、烧杯和 ______ ,
(2)在上述流程图中使物质中元素的化合价发生改变的是操作_____
(3)整个实验流程中可以循环利用的物质是 ______ (用名称表示);煅烧生成的Fe2O3可用于工业炼铁,其反应的化学反应方程式为 ______ .
(4)该工艺流程中制取的(NH4)2SO4在农业上可以用作 ______ .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜是人类最早利用的金属之一。 冶炼铜常用铜矿石——孔雀石,其主要成分为碱式碳酸铜[Cu2(OH)2CO3],生成铜的简要流程如下:
(查阅资料)碱式碳酸铜是一种绿色的不溶于水的固体,受热易分解,从组成上分析,它兼备碱和碳酸盐的化学性质,所以能与酸发生反应。
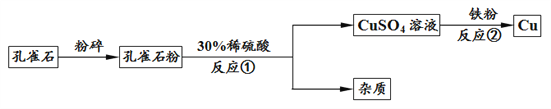
(1)反应前,将孔雀石粉碎的目的是_________________________。
(2)写出反应②的化学方程式_____________________。
(3)反应①后进行的操作名称是__________,若所得CuSO4溶液为浑浊的,则可能的原因是___________(写一种即可)。
(4)反应①除生成CuSO4外,还生成了两种氧化物,其化学式分别为_________、__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】早在春秋战国时期,我国就开始生产和使用铁器,工业上炼铁的原理是利用一氧化碳和氧化铁反应,某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
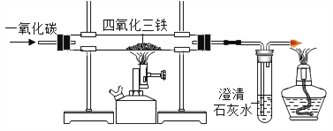
(1)写出CO还原氧四氧化三铁的化学反应方程式_________。
(2)能说明一氧化碳还原四氧化三铁属于化学变化的现象是________。
(3)右边导气管口放置点燃的酒精灯的目的是______________。
(4)若把四氧化三铁换成一定量的磁铁矿样品W克(该反应完全进行),并想测定该磁铁矿样品中四氧化三铁的质量分数,需要测量的数据是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气、水都是宝贵的资源。
(1)自然界中的水都不是纯水,净水时,需加入明矾的目的是_____。 在生活中常采用_____的方法降低水的硬度。
(2)利用空气、水制取硝酸的一种流程如下图所示。
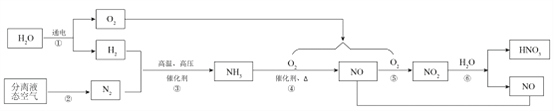
(Ⅰ)步骤①中发生反应的化学方程式为_____。
(Ⅱ)从微观角度解释 NO 和 NO2 化学性质不同的原因_____。
(Ⅲ)实验室制取氧气的化学方程式是______任写一个)。
(3)下列保护空气措施合理的是_____(填标号)。
A. 工厂通过加高烟囱直接排放废气 B. 使用清洁能源
C. 提倡步行、骑自行车等“低碳”出行方式 D. 推广使用乙醇汽油代替普通汽油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com