
| A. | 单质熔、沸点逐渐降低 | B. | 单质的氧化性逐渐增强 | ||
| C. | 气态氢化物沸点逐渐升高 | D. | 气态氢化物稳定性逐渐减弱 |
分析 卤族元素从上到下,随着原子序数的增大,原子半径逐渐增大,元素的非金属性逐渐减弱,对应单质的氧化性逐渐减弱,气态氢化物的稳定性减弱,分子晶体的熔沸点与相对分子质量成正比,还与氢键有关.
解答 解:A.卤素单质都是分子晶体,其熔沸点与相对分子质量成正比,随着原子序数增大,其相对分子质量增大,单质的熔沸点逐渐升高,故A错误;
B.随着原子序数增大,元素的非金属性逐渐减弱,则其单质的影响逐渐减弱,故B错误;
C.卤化氢都是分子晶体,但HF中含有氢键,所以卤化物熔沸点高低顺序是HF>HI>HBr>HCl,故C错误;
D.元素的非金属性越强,其氢化物的稳定性越强,卤素随着原子序数增大其非金属性减弱,则气态氢化物稳定性逐渐减弱,故D正确;
故选D.
点评 本题考查卤素性质,为高频考点,明确同一主族元素性质递变规律是解本题关键,注意分子晶体的熔沸点与相对分子质量成正比,还与氢键有关,为易错点.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 对于一定条件下已平衡的可逆反应,增加反应物的物质的量,正反应速率一定增大 | |
| B. | 改变外界条件使化学反应速率发生改变,则化学平衡一定发生移动 | |
| C. | 催化剂能改变活化分子百分数,所以一定可以改变化学反应速率和化学平衡 | |
| D. | 升高温度,正、逆反应速率均增大,平衡向吸热反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol NH5中含有5NA个N-H键 | |
| B. | NH5中N元素的化合价为-5价 | |
| C. | 与水反应时,原理和NaH与水反应相同 | |
| D. | 与乙醇反应时,NH5被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LHCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) | |
| B. | 1L0.1mol•L-1 CuSO4•(NH4)2SO4•6H2O的溶液中:c(${SO}_{4}^{2-}$)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) | |
| C. | 0.1mol/LNaHCO3溶液中:c(H+)+c(H2CO3)=c(${CO}_{3}^{2-}$)+c(OH-) | |
| D. | 将0.2mol/LHCN溶液和0.1mol/L的NaOH溶液等体积混合后,溶液显碱性:c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA | |
| B. | 通常状况下,NA个CO2分子占有的体积为22.4 L | |
| C. | 常温常压下,1.06g Na2CO3含有的Na+数为0.02 NA | |
| D. | 标准状况下,22.4L 乙醇含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. ;含有离子键和非极性共价键的化合物的电子式为
;含有离子键和非极性共价键的化合物的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 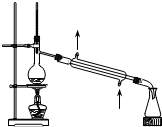 装置可用于分离苯和溴苯的混合物 | B. | 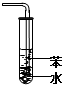 装置可用于吸收HCl或NH3气体 | ||
| C. | 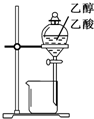 用图所示装置分离乙醇与乙酸 | D. | 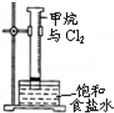 图中量筒中发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
 ①实验1中以v (CO2) 表示的反应速率为0.13mol/(L.min); (取小数二位,下同).
①实验1中以v (CO2) 表示的反应速率为0.13mol/(L.min); (取小数二位,下同).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com