
【题目】通过实验得出的结论正确的是
A.某溶液中加入酸性KMnO4溶液褪色,则原溶液一定含有I-
B.某固体试样加水溶解,取上层清液,加KSCN溶液出现红色,原固体中一定含Fe3+
C.通过元素分析测定某无机固体样品的组成是MgH2C2O6,该固体不可能是碱式碳酸镁
D.某碱性水样滴加稀盐酸无沉淀,再加BaCl2溶液,出现白色沉淀,则原水样中一定含![]()
【答案】C
【解析】
A.向某溶液中加入酸性KMnO4溶液,溶液褪色,说明原溶液可能含Fe2+或碘离子、亚硫酸根离子等还原性离子,故A错误;
B.某固体试样加水溶解,若溶解后为亚铁离子,易被空气中氧气氧化为铁离子,取上层清液,加KSCN溶液出现红色,原固体中不一定含Fe3+,可能是亚铁离子,故B错误;
C.若为碱式碳酸镁,化学式应为:Mg2(OH)2CO3,通过元素分析测定某无机固体样品的组成是MgH2C2O6,不能写出碱式碳酸镁,故C正确;
D.某碱性水样滴加稀盐酸无沉淀,可能是碳酸根离子和滴入的氢离子反应生成部分碳酸氢根离子,再加BaCl2溶液,原溶液中碳酸根离子也会生成碳酸钡沉淀,出现白色沉淀,则原水样中不一定含SO42-,故D错误;
故答案为C。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol/LNaOH溶液滴定10mL0.1mol/LH2X溶液,溶液的pH与NaOH溶液的体积关系如图所示,下列说法正确的是

A.水电离出来的c(OH):D点<B点
B.C点存在关系式:c(Na+)=c(HX)+2c(X2)c(H+)
C.B点:c(Na+)>c(HX)>c(H+)>c(X2)>cH2X)
D.A点溶液中加入少量水:![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)下列右侧对左侧物质的描述与左侧任何物质都不对应的是_________(填右侧小写的编号);
物质 描述
A.四氧化三铁 a.自来水消毒剂
B.过氧化钠 b.工业制玻璃
C.碳酸氢钠 c.红色油漆和涂料
D.硅酸钠 d.木材防火剂
E.明矾 e.呼吸面具中氧气的来源
F.青铜 f.制光纤的材料
G.硅 g.用量最大的金属材料
H.氯气 h.焰色反应为绿色
II.(2)明矾溶液中加少量Ba(OH)2溶液的离子方程式 ______________;
(3)漂白粉溶液中通过量CO2的离子方程式________________;
(4)将KFe2Si3O8(OH)2改写为氧化物的形式________________,1mol KFe2Si3O8(OH)2和足量稀盐酸反应,消耗HCl的物质的量为________mol;
(5)配平下面的离子方程式,并用双线桥表示反应的电子转移:______
SO32- + MnO4- + — SO42-+ Mn2+ +______
III.(6)若要除去下列物质中的杂质(括号内为杂质),请将选用的试剂填入表格。
物质(杂质) | 试剂 |
NaHCO3溶液(Na2CO3) | ①______ |
FeCl3溶液(FeCl2) | ②______ |
SiO2(CaCO3) | ③______ |
Fe2O3(SiO2) | ④______ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,W是同周期主族元素中原子半径最小的,下列说法正确的是
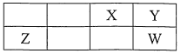
A.W位于第3周期Ⅶ族
B.原子半径![]()
C.Y的非金属性比W强,所以Y的最高价氧化物的水化物的酸性比W的强
D.X、Y、Z、W的简单氢化物中X的沸点最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,1L0.1mol·L-1的NaOH溶液中缓慢通入CO2,溶液的pH随CO2的物质的量变化如下图所示(实验过程中溶液体积变化忽略不计),下列说法正确的是
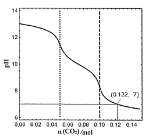
A.在整个过程中,溶液中一定不存在![]()
B.![]() 时,
时,![]()
C.当![]() 时,溶液中不存在H2CO3分子
时,溶液中不存在H2CO3分子
D.当![]() 时,一定有
时,一定有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)甲烷和氯气在光照条件下发生卤代反应,其反应机理如下:
反应①:![]() △H=242.7kJ·mol-1
△H=242.7kJ·mol-1
反应②:![]() △H=7.5kJ·mol-1
△H=7.5kJ·mol-1
反应③:![]() △H=-112.9kJ·mol-1
△H=-112.9kJ·mol-1
反应②、③反复循环,反应物浓度逐渐降低,自由基逐渐消失,反应停止。
(1)在该反应条件下断裂1mol CH3Cl中C—Cl键,需要吸收的能量为______。
(2)反应②与反应③的反应过程,如下图所示:
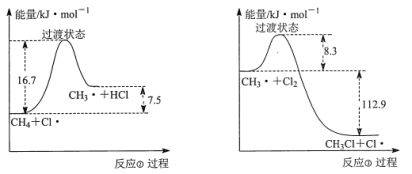
则该条件下,反应②的速率______反应③的速率(填“>”、“<”或“=”)。
(3)根据以上的反应机理,我们可以推测甲烷和氯气在光照条件下反应,除生成CH3Cl、CH2Cl2、CHCl3、CCl4外,还会有乙烷等有机物,原因是______。
(二)煤燃烧排放的SO2和NO2可形成严重的大气污染,某兴趣小组提出利用反应![]() 来处理。
来处理。
(4)在一定温度下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,达到平衡时NO2和SO2的体积之比为1:5,则该温度下平衡常数K为______。
(5)若向绝热恒容密闭容器中通入SO2和NO2,v正随时间变化如下图。下列结论正确的是______。
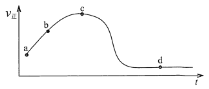
A. a点颜色比b点深
B. c点正反应速率等于逆反应速率
C. 若升高温度,d点SO2的转化率将增大
D. 反应的过程中,容器内气体压强保持不变
E. 若外界条件不发生改变,d点NO2和NO的体积比将保持不变
(6)若用一定浓度的NaClO2溶液(已调节其初始pH为5)充分吸收煤燃烧排放的烟气后,测得溶液中各物质的浓度如下表所示:

其中 NaClO2溶液吸收SO2的主要离子反应方程式为______。
(7)为消除NOx,科学家开发了一种能传导O2-的固态高温陶瓷电池,一极通氨气,另一极通NOx,生成无污染的常见气体和液体。写出该电池的正极反应式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)![]() 的系统名称是_________;
的系统名称是_________;
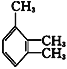 的系统名称为__________。
的系统名称为__________。
(2)2,4-二甲基-3-乙基戊烷的结构简式是_____,1mol该烃完全燃烧生成二氧化碳和水,需消耗氧气_______mol。
(3)键线式![]() 表示的物质的结构简式是__________________。
表示的物质的结构简式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
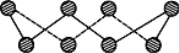
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是______;
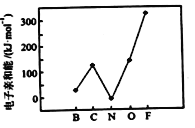
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是_______;氮元素的E1呈现异常的原因是________。
(3)Se原子序数为_______,其核外M层电子的排布式为_________;
(4)H2Se的稳定性比H2S_____________(填“强”或“弱”)。SeO3分子的立体构型为______。
(5)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从原子核外电子结构角度来看,Fe2+ 易被氧化成Fe3+的原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究一种不含结晶水的盐X(仅含5种元素)的组成和性质,将X隔绝空气加热(发生非氧化还原反应)并完成如下实验:
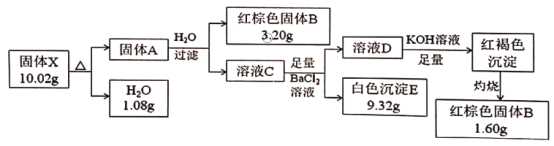
请回答:
(1)X含有的元素有H、O和_____(用元素符号表示)。
(2)X的化学式为____。
(3)向溶液C中通入SO2气体,溶液的酸性增强,其原因是(用离子方程式表示)_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com