
| ① |
| ② |
| ③ |
| ④ |
| ⑤ |
| H2 |
| ① |
| ② |
| ③ |
| ④ |
| ⑤ |
| H2 |
| ① |
| ② |
| ③ |
| ④ |
| ⑤ |
| H2 |


科目:高中化学 来源: 题型:
| A、①④ | B、⑥⑧ |
| C、②⑥⑦ | D、③⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上常用电解的方法制备X、Y的单质 |
| B、元素Q和Z能形成QZ2型的共价化合物 |
| C、原子半径的大小顺序:r(X)>r(Y)>r(W)>r(Q) |
| D、元素X、Y的最高价氧化物对应的水化物之间能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下:
某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

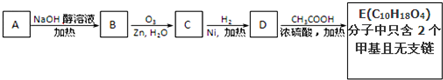
查看答案和解析>>
科目:高中化学 来源: 题型:
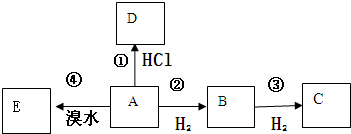
查看答案和解析>>
科目:高中化学 来源: 题型:

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | 加入试剂 | 离子方程式 |
| SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com