
如图所示的是某原子晶体A空间结构的一个单元,A与某物质B反应生成C,其实质是每个A﹣A键中插入一个B原子,则C物质的化学式为( )

|
| A. | AB | B. | AB4 | C. | AB2 | D. | A2B5 |
考点:
晶胞的计算.
专题:
化学键与晶体结构.
分析:
A空间结构的一个单元中含有5个A原子,每个A﹣A键中插入一个B原子,5的A原子含有10个A﹣A键,所以插入了10个B原子,根据A、B两种原子的个数比确定C物质的化学式.
解答:
解:A空间结构的一个单元中含有5个A原子,每个A﹣A键中插入一个B原子,5的A原子含有10个A﹣A键,所以插入了10个B原子,所以该单元中含有5个A原子10个B原子,所以A、B原子个数比是1:2,所以其化学式是AB2,故选C.
点评:
本题考查了化学式的确定,明确该单元中含有的A﹣A键的个数是解本题的关键,易漏记正四面体顶点上的A﹣A键而导致错误,难度较大.


科目:高中化学 来源: 题型:
将一定体积密度为1.32g/cm3的硫酸溶液逐
滴滴入到BaCl2溶液中,直到沉淀恰好完全为止。已知反应后所得溶液的质量等于原BaCl2溶液的质量,则
原硫酸溶液浓度为( )
A.23.9% B.11.0% C.13.5mol/L D.5.67mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.固体氯化钠不导电,所以氯化钠不是电解质
B.虽然NaHSO4溶于水能电离出H+,但它不是酸
C.“纳米材料”是粒子直径1~100 nm的材料,它属于胶体
D.在一个氧化还原 反应中,有一种元素被氧化肯定有另一种元素被还原
反应中,有一种元素被氧化肯定有另一种元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是(NA为阿伏加德罗常数)( )
|
| A. | 124g P4含有P﹣P键的个数为4NA |
|
| B. | 12g石墨中含有C﹣C键的个数为3NA |
|
| C. | 12g金刚石中含有C﹣C键的个数为2NA |
|
| D. | 60g SiO2中含Si﹣O键的个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于晶体的下列说法正确的是( )
①在晶体中只要有阴离子就一定有阳离子,只要有阳离子就一定有阴离子;②分子晶体的熔点一定比金属晶体的低;③晶体中分子间作用力越大,分子越稳定;④离子晶体中,一定存在离子键;⑤分子晶体中,一定存在共价键;⑥原子晶体中,一定存在共价键;⑦熔融时化学键没有破坏的晶体一定是分子晶体.
|
| A. | ②④⑥ | B. | ④⑤⑦ | C. | ④⑥⑦ | D. | ③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第八列 |
(1)已知BA5为离子化合物,是由 、 两种微粒构成的(填化学符号).
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,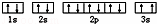 该同学所画的电子排布图违背了 .
该同学所画的电子排布图违背了 .
(4)G位于 族,G3+价电子排布式为 .GE3常温下为固体,熔点282℃,沸点315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断GE3的晶体类型为 .
(5)DE3中心原子的杂化方式为 ,其空间构型为 .
(6)前四周期中与F同一族的所有元素分别与E元素形成化合物,其晶体的熔点由高到低的排列顺序为(写化学式) ,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
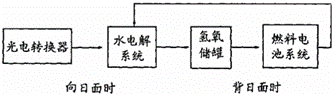
右图是某太空空间站能量转化系统的局部示意图,基中燃料电池采用KOH为电解液,下列有关说法中正确的是( )
|
| A. | 该能量转化系统工作时,需不断补充H2O |
|
| B. | 该转化系统的能量本质上来源于太阳能 |
|
| C. | 水电解系统中的阴极反应:4OH﹣﹣4e﹣=O2+2H2O |
|
| D. | 燃料电池放电时的负极反应:H2﹣2e﹣=2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
火力发电厂在发电过程中会释放大量的
SO2,CO,NO而造成污染,对燃煤烟气进行脱硫、脱碳、脱硝等处理,以实现绿色环保、废物利用的目的.
(1)脱硫.
①用采用活性炭吸附含SO2废气,2SO2+O2⇌2SO3
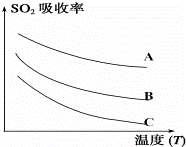
某研究小组研究燃煤烟气流速、温度、水蒸气含量等因素对SO2吸收效率的影响,实验结果如左图所示.
A 水蒸气含量10%,燃煤烟气流速0.01L/s
B 水蒸气含量5%,燃煤烟气流速0.01L/s
C水蒸气含量5%,燃煤烟气流速0.025L/s
根据左图所示,要提高燃煤烟气中SO2的吸收效率,烟气流速应选择 L/s,温度应选择 (填“高温”或“低温”),应该 水蒸气含量(填“提高”或“降低”)
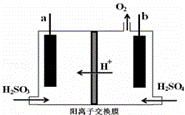
②用惰性电极电解SO2水溶液:H2SO3 O2↑+S↓+H2O
O2↑+S↓+H2O
装置如右图所示,S单质将在 极得到(填“a”或“b”)
该电极的电极反应式
不考虑溶液体积的变化,电解槽右池的pH将
(填“上升”、“降低”或“不变”)
| 物质 | CO | H2O | HCOOH |
| 浓度/mol•L﹣1 | 0.5 | 1.5 | 0.5 |
(2)脱碳.将CO转化为甲酸HCOOH的反应为CO(g)+H2O(g)⇌HCOOH (g),某温度下的平衡常数为1.5.此温度下,密闭容器中加入CO(g)与H2O(g),某时刻测得各组分的浓度如右表:
反应的平衡常数表达式 K= ;比较此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”).到达平衡时H2O的平衡转化率为 .
(3)脱硝.①烟气联合脱硝脱硫,可以有效提高可以显著提高SO2吸收效率,其主要原因在于NO对2SO2+O2⇌2SO3起催化作用,试用化学方程式表示该过程(提示:催化剂参与反应,但是质量和化学性质在反应前后都没有改变) 、 (不必配平)
②可以利用烟气中CO作为还原剂,催化还原NO,同步脱硝脱碳,
CO(g)+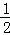 O2(g)=CO2(g)△H=﹣283.0kJ•mol﹣1;N2(g)+O2(g)=2NO(g)△H=182.6kJ•mol﹣1
O2(g)=CO2(g)△H=﹣283.0kJ•mol﹣1;N2(g)+O2(g)=2NO(g)△H=182.6kJ•mol﹣1
NO与CO反应得到无污染产物的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组表述中,两个微粒不属于同种元素原子的是( )
|
| A. | 3p能级有一个空轨道的基态原子和核外电子的排布 为1s22s22p63s23p2的原子 |
|
| B. | 2p能级无空轨道且有一个未成对电子的基态原子和原子的最外层电子排为2s22p5的原子 |
|
| C. | M层全充满而N层为4s2的原子和核外电子排布为 1s22s22p63s23p64s2的原子 |
|
| D. | 最外层电子数是核外电子总数的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com