
| A. | 1 L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol•L-1 | |
| B. | 从1 L 2mol•L-1的H2SO4溶液中取出0.5L,剩余溶液的浓度仍为2mol•L-1 | |
| C. | 制成0.5L 10mol•L-1的盐酸,需标准状况下氯化氢气体112L | |
| D. | 中和100mL 1mol•L-1的H2SO4溶液,需NaOH的质量为4g |
分析 A、溶液的体积与溶剂的体积不等;
B、溶液的物质的量浓度与溶液的体积无关;
C、0.5L 10mol•L-1的盐酸溶液中的溶质物质的量=0.5L×10mol•L-1=5mol,n=$\frac{V}{Vm}$计算气体的体积;
D、根据关系式H2SO4~2NaOH来求解,结合n=$\frac{m}{M}$计算.
解答 解:A、1 L水中溶解了58.5 g NaCl,溶质物质的量=$\frac{58.5g}{58.5g/mol}$=1mol,溶液的体积不是1L,溶液的物质的量浓度小于1mol/L,故A错误;
B、从1 L 2 mol•L-1的H2SO4溶液中取出0.5 L,剩余溶液的浓度仍为2mol•L-1,故B正确;
C、制成0.5L 10mol•L-1的盐酸,溶质为HCl物质的量=0.5L×10mol•L-1=5mol,需标准状况下氯化氢气体体积=5mol×22.4L/mol=112L,故C正确;
D、由关系式H2SO4~2NaOH可知:n(NaOH)=2n(H2SO4)=2×0.1L×1 mol•L-1=0.2mol,m(NaOH)=0.2mol×40g/mol=8g,故D错误;
故选AD.
点评 本题主要考查了物质的量浓度、气体摩尔体积概念及其计算,难度不大,掌握基础是解题关键.


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铝和氢氧化钾都是重要的工业产品,请回答问题:
铝和氢氧化钾都是重要的工业产品,请回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应速率增大,逆反应速率减小 | B. | X的转化率变大 | ||
| C. | Y的转化率变大 | D. | 新平衡时X的体积分数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水 阴极:Na++e-═Na | |
| B. | 电镀铜时(电解质溶液为CuSO4溶液) 阳极:Cu-2e-═Cu2+ | |
| C. | 电解熔融NaCl 阴极:Na++e-═Na | |
| D. | 电解NaOH溶液 阳极:4OH--4e-═2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
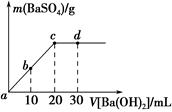 常温下,向0.25mol•L-1的硫酸氢钠溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是( )
常温下,向0.25mol•L-1的硫酸氢钠溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是( )| A. | 硫酸氢钠溶液的体积为10 mL | |
| B. | 溶液的导电能力:c<b<a | |
| C. | d时刻溶液的pH为13 | |
| D. | b时刻溶液中SO42-的浓度约为0.125 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com