
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:多选题
| A. | 1 L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol•L-1 | |
| B. | 从1 L 2mol•L-1的H2SO4溶液中取出0.5L,剩余溶液的浓度仍为2mol•L-1 | |
| C. | 制成0.5L 10mol•L-1的盐酸,需标准状况下氯化氢气体112L | |
| D. | 中和100mL 1mol•L-1的H2SO4溶液,需NaOH的质量为4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10:2:1 | B. | 5:2:1 | C. | 15:3:2 | D. | 15:3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸 | B. | Ba(OH)2稀溶液 | C. | MgCl2溶液 | D. | CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
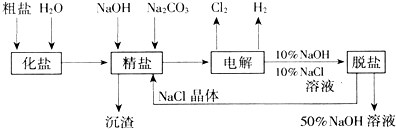
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com