
| A. | 6mol | B. | 5mol | C. | 4mol | D. | 3mol |
分析 根据C2H4生成六氯代烷先发生加成反应,发生加成反应时,双键的物质的量与氯气的物质的量之比为1:1,1,2-二氯乙烷和氯气发生取代反应生成六氯乙烷,1,2-二氯乙烷中所有氢原子被氯原子取代时,氢原子与Cl2的物质的量之比为1:1来解答;
解答 解:根据C2H4+Cl2→CH2ClCH2Cl知,1mol乙烯与氯气发生加成反应需要氯气1mol;
根据CH2ClCH2Cl+4Cl2$\stackrel{光照}{→}$C2Cl6+4HCl知,1mol 1,2-二氯甲烷生成C2Cl6时需要氯气的物质的量为4mol,所以两个过程一共消耗氯气的物质的量为5mol,
故选B.
点评 本题以取代反应和加成反应为载体考查了物质的量的计算,根据加成反应中氯气和双键的关系、取代反应中取代的氢原子和氯气之间的关系来分析解答,难度不大.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
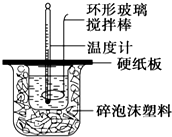 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol/L | B. | 0.4mol/L | C. | 0.6mol/L | D. | 0.8mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤ | C. | ①④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

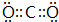 ;N的最高价氧化物与NaOH溶液反应离子方程式:SiO2+2OH-=SiO32-+H2O.
;N的最高价氧化物与NaOH溶液反应离子方程式:SiO2+2OH-=SiO32-+H2O.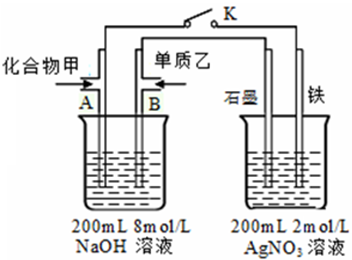
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:Br2>Cl2>F2 | B. | 氧化性:Cl2>Br2>I2 | ||
| C. | 酸性:HClO4>HBrO4>HIO4 | D. | 稳定性:HI>HBr>HCl>HF |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 必定是可溶性氯化物 | B. | 可能是可溶性碳酸盐 | ||
| C. | 可能含有Cl- | D. | 必定是氯水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com