
| A、稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| B、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
| C、硫酸铜溶液与氢氧化钠溶液混合:CuS04+20H-=Cu(OH)2↓+SO42- |
| D、硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-=AgCl↓+NO3- |


科目:高中化学 来源: 题型:
| A、混合气体的压强不变 |
| B、混合气体的密度不变 |
| C、每消耗2molB,同时消耗1molC |
| D、C和D的浓度比不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
2- 3 |
+ 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝制饮具最好不要盛放酸性、或碱性较强的液体食物,因为Al和Al2O3既可以与酸反应、又可以与碱反应 |
| B、将SO2通入含HClO的溶液中,生成H2SO4,说明HClO酸性比H2SO4 强 |
| C、FeCl3溶液可以腐蚀线路板上的Cu,说明Fe的金属活动性大于Cu |
| D、过量的铜屑与稀硝酸作用,反应停止后,再加入1mol/L稀硫酸,铜屑又逐渐溶解是因为铜可直接与1mol/L稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol/L H2SO4 溶液 |
| B、2mol/L NaOH溶液 |
| C、2mol/L MgSO4溶液 |
| D、硅酸溶胶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
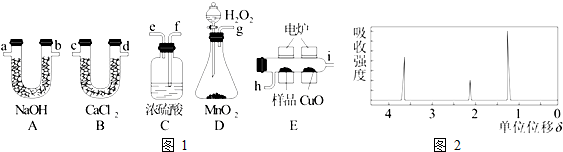
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com