
分析 甲、乙两容器中C的体积分数都为0.2,说明为等效平衡,恒温恒容下,若反应气体气体的物质的量发生变化,按化学计量数转化到左边满足A为6mol、B为2mol,D为固体,增大D物质的量不影响平衡,且n(D)≥$\frac{1}{x}$n(C),若反应气体气体的物质的量不变,按化学计量数转化到左边满足n(A):n(B)=1:3,且n(D)≥$\frac{1}{x}$n(C),而平衡时甲、乙两容器中A的物质的量相等,则只能为按化学计量数转化到左边满足A为6mol、B为2mol,且n(D)≥$\frac{1}{x}$n(C).
解答 解:甲、乙两容器中C的体积分数都为0.2,说明为等效平衡,恒温恒容下,若反应气体气体的物质的量发生变化,按化学计量数转化到左边满足A为6mol、B为2mol,D为固体,增大D物质的量不影响平衡,且n(D)≥$\frac{1}{x}$n(C),若反应气体气体的物质的量不变,按化学计量数转化到左边满足n(A):n(B)=1:3,且n(D)≥$\frac{1}{x}$n(C),
而平衡时甲、乙两容器中A的物质的量相等,则只能为按化学计量数转化到左边满足A为6mol、B为2mol,且n(D)≥$\frac{1}{x}$n(C),即1.5+3×$\frac{3}{x}$=6,0.5+3×$\frac{1}{x}$=2,则x=2,
故答案为:2.
点评 本题考查等效平衡,关键是对等效平衡规律的理解掌握,注意反应前后气体体积是否发生变化,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题

| A. | 2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2 | B. | 2HI+Cl2═2HCl+I2 | ||
| C. | CO2+C $\frac{\underline{\;高温\;}}{\;}$2CO | D. | 2HCl+CuO═CuCl2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
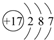 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有1.25mol NaN3被氧化 | B. | 被还原的N原子的数目是0.2NA | ||
| C. | 转移电子的物质的量为2mol | D. | 标准状况下生成44.8L N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采取低碳、节俭的生活方式 | |
| B. | 太阳能、海洋能、地热能和生物质能等都是新能源 | |
| C. | 石油、煤、天然气属于可再生能源 | |
| D. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(Ac-)>c(OH-)>c(H+) | B. | c(Na+)=c(Ac-)>c(OH-)>c(H+) | ||
| C. | c(Na+)>c(OH-)>c(Ac-)>c(H+) | D. | c(Na+)>c(OH-)>c(H+)>c(Ac-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)
实验室制备溴乙烷(C2H5Br)的装置和步骤如图:(已知溴乙烷的沸点38.4℃)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 250 | 350 |
| K | 2.041 | x |
| c(CO) | c(H2) | c(CH3OH) | |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
 VO2++V3++H2O,试推写出放电时正极的电极反应式VO2++2H++e-=VO2++H2O.
VO2++V3++H2O,试推写出放电时正极的电极反应式VO2++2H++e-=VO2++H2O. Mg2++2OH-,当加入Fe3+后与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动,最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3.
Mg2++2OH-,当加入Fe3+后与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动,最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com