
| A. | 采取低碳、节俭的生活方式 | |
| B. | 太阳能、海洋能、地热能和生物质能等都是新能源 | |
| C. | 石油、煤、天然气属于可再生能源 | |
| D. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
分析 保护环境,是我国的基本国策,理解该词可从减少污染物的排放、开发新能源等角度分析解答,注意对新能源与可再生能源概念的理解.
解答 解:A.采取低碳、节俭的生活方式,可以节省大量的能源,符合保护环境的理念,故A正确;
B.煤、石油、天然气是化石燃料,太阳能、核能、地热能、潮汐能、风能、氢能、生物质能等都是新能源,故B正确;
C.石油、煤、天然气不能短期内从自然界得到补充,是不可再生能源,故C错误;
D.大量燃烧化石燃料可产生有害气体和烟尘,是造成雾霾天气的一种重要因素,故D正确;
故选:C.
点评 本题考查了化学与社会生活,涉及常见生活中的环境污染与治理、新能源的概念、可再生能源的概念,侧重考查学生对基础知识掌握,题目难度不大,注意对相关知识的积累.


科目:高中化学 来源: 题型:填空题
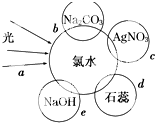 氯气是一种重要的化工原料.
氯气是一种重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有4 mol硝酸被还原 | B. | 有2 mol硝酸被还原 | ||
| C. | 转移6 mol电子 | D. | 转移3 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放. | NO | CO | E | F |
| 初始 | 0.100 | 0.100 | 0 | 0 |
| T1 | 0.020 | 0.020 | 0.080 | 0.040 |
| T2 | 0.010 | 0.010 | 0.090 | 0.045 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com