
| A.一定没有N2,CO和HCl中至少有一种 |
| B.一定有N2、HCl和CO |
| C.一定有N2,CO和HCl中至少有一种 |
| D.一定有N2和HCl,没有CO |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| | 实验操作 | 现象 | 结论 |
| A | 某有机物与溴的四氯化碳溶液混合 | 溶液褪色 | 有机物含碳碳双键 |
| B | 乙醇与重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 常温下,将二氧化碳通入苯酚钠溶液 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| D | 苯和苯酚稀溶液分别与浓溴水混合 | 后者产生白色沉淀 | 羟基影响了苯环的活性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 Na2SO4 + SO2↑+ H2O,据此设计如下图所示装置进行相关实验。
Na2SO4 + SO2↑+ H2O,据此设计如下图所示装置进行相关实验。 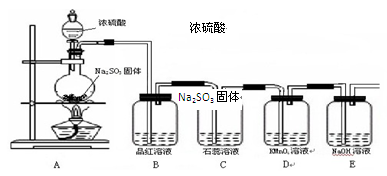
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.检验溶液中是否含有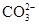 :滴加稀盐酸,将产生的气体通入澄清石灰水 :滴加稀盐酸,将产生的气体通入澄清石灰水 |
| B.从含I-的溶液中提取碘:加入适量稀硫酸与3%的H2O2溶液,再用酒精萃取 |
C.检验溶液中是否含有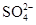 :先滴加稀硝酸,再滴加BaCl2溶液 :先滴加稀硝酸,再滴加BaCl2溶液 |
| D.分离NaCl和NH4Cl:将固体加热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
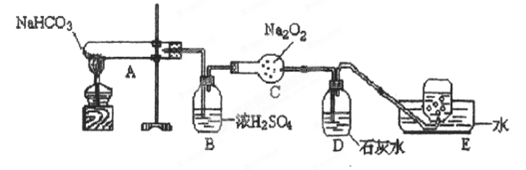
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向AlCl3溶液中加入过量的氨水,过滤,洗涤,干燥,加热灼烧 | 制取Al2O3 |
| B | 将浓硫酸与碳混合加热,生成的气体通入足量的澄清石灰水 | 检验气体产物中的CO2 |
| C | 向某溶液中加入NaOH溶液后再加热,若产生的气体能使湿润的红色石蕊试纸变蓝, | 验证该溶液中肯定有NH4+ |
| D | 将SO2通入品红溶液中,品红溶液褪色,加热褪色后的溶液,恢复红色 | 验证亚硫酸的不稳定性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
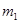 g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2
g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2 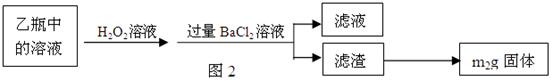
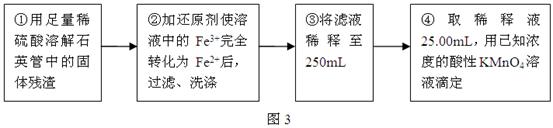
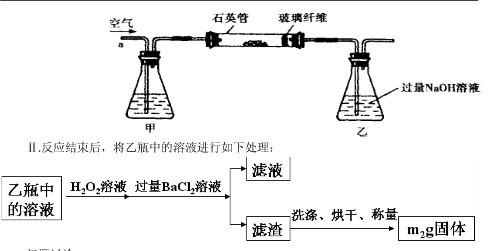
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com