
ʵ��Ŀ�ģ�Ϊ�о����ʲ�������Ũ����ķ�Ӧ
��1����ȡ������̼�ظ���12��0g����30��0mLŨ�����У����ȣ���ַ�Ӧ��õ���ҺX���ռ�������Y��
�ټ�ͬѧ��ΪX�г�Fe3+����ܺ���Fe2+����Ҫȷ�������Ƿ���Fe2+��Ӧѡ�������Լ�Ϊ ��ѡ����ţ�
a��KSCN��Һ����ˮ b�����ۺ�KSCN��Һ c��Ũ��ˮ d������KMnO4��Һ
����ͬѧȡ672 mL����״��������Yͨ��������ˮ�У�������Ӧ��SO2+Br2+2H2O=2HBr+H2SO4Ȼ���������BaCl2��Һ�����ʵ�������õ��������4��66g���ݴ���֪����Y ��SO2���������Ϊ ��
��������ʵ����SO2��������Ľ������ͬѧ��Ϊ����Y�л����ܺ�����H2��CO2���塣Ϊ�����������̽��ʵ��װ�ã�ͼ�мг�����ʡ�ԣ���
��2������Y�� ����H2��ԭ���� ��
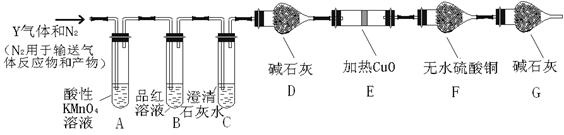
��3��װ��A���Լ��������� ����Ӧ�����ӷ���ʽ ��
��4������ȷ������Y�к���CO2��ʵ������ ��
��5���������Y�к���H2��Ԥ��ʵ������Ӧ�� ��
 �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д� ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴Ӧ�ﵽ��ѧƽ��ı�־�ǣ�������
| �� | A�� | �����淴Ӧ���ٽ��� | B�� | ��Ӧ���Ũ��Ϊ�� |
| �� | C�� | �����淴Ӧ�����ڼ������� | D�� | �����淴Ӧ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ������ܶ�Ϊ1��32g/cm3��������Һ��
�ε��뵽BaCl2��Һ�У�ֱ������ǡ����ȫΪֹ����֪��Ӧ��������Һ����������ԭBaCl2��Һ����������
ԭ������ҺŨ��Ϊ�� ��
A��23��9% B��11��0% C��13��5mol/L D��5��67mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Һ���ܴ������棬����OH���г�������������H+������ ��
��
�����ǣ� ��
A��Na+��Cu2+��Cl����SO42�� B��Na+��Ca2+��Cl����HCO3��
C��H+��Al3+��OH����NO3�� D��Fe3+��K+��SO42����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Һ���ܺ���Cl����SO ��CO
��CO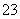 ��NH
��NH ��Fe3����Fe2����
��Fe3����Fe2����
Al3����Na����ijͬѧΪ��ȷ����ɷ֣�ȡ������Һ����Ʋ����������ʵ�飺
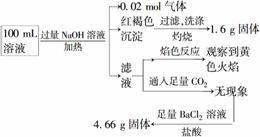
����˵����ȷ����(����)
A��ԭ��Һ��c(Fe3��)��0.2 mol·L��1
B��Ҫȷ��ԭ��Һ���Ƿ���Fe2���������Ϊȡ����ԭ��Һ���Թ��У���KSCN��Һ���ټ�������
��ˮ����Һ��Ѫ��ɫ������Fe2��
C��SO ��NH
��NH ��Na��һ�����ڣ�CO
��Na��һ�����ڣ�CO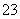 ��Al3��һ��������
��Al3��һ��������
D����Һ��������4�����Ӵ��ڣ�����Cl��һ�����ڣ���c(Cl��)��0.2 mol·L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�����������Һ���ܴ���������ǣ� ��
A��Na����Al3����NO3����H�� B��Ba2����Na����Cl����SO42��
C��Mg2����H����SO42����OH�� D��H����Na����CO32����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ���ǣ� ��
A�������Ȼ��Ʋ����磬�����Ȼ��Ʋ��ǵ����
B����ȻNaHSO4����ˮ�ܵ����H��������������
C�������ײ��ϡ�������ֱ��1��100 nm�IJ��ϣ������ڽ���
D����һ��������ԭ ��Ӧ�У���һ��Ԫ�ر������϶�����һ��Ԫ�ر���ԭ
��Ӧ�У���һ��Ԫ�ر������϶�����һ��Ԫ�ر���ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ�NAΪ�����ӵ���������������
| �� | A�� | 124g P4����P﹣P���ĸ���Ϊ4NA |
| �� | B�� | 12gʯī�к���C﹣C���ĸ���Ϊ3NA |
| �� | C�� | 12g���ʯ�к���C﹣C���ĸ���Ϊ2NA |
| �� | D�� | 60g SiO2�к�Si﹣O���ĸ���Ϊ2NA |
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������糧�ڷ�������л��ͷŴ�����
SO2��CO��NO�������Ⱦ����ȼú��������������̼�������ȴ�������ʵ����ɫ�������������õ�Ŀ�ģ�
��1������
���ò��û���̿������SO2������2SO2+O2⇌2SO3
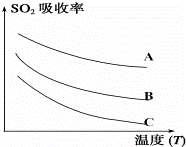
ij�о�С���о�ȼú�������١��¶ȡ�ˮ�������������ض�SO2����Ч�ʵ�Ӱ�죬ʵ��������ͼ��ʾ��
A ˮ��������10%��ȼú��������0.01L/s
B ˮ��������5%��ȼú��������0.01L/s
Cˮ��������5%��ȼú��������0.025L/s
������ͼ��ʾ��Ҫ���ȼú������SO2������Ч�ʣ���������Ӧѡ������L/s���¶�Ӧѡ������������¡����¡�����Ӧ������ˮ�������������ߡ����͡���
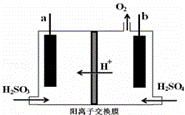
���ö��Ե缫���SO2ˮ��Һ��H2SO3 O2��+S��+H2O
O2��+S��+H2O
װ������ͼ��ʾ��S���ʽ����������õ����a����b����
�õ缫�ĵ缫��Ӧʽ����
��������Һ����ı仯�������ҳص�pH������
����������������͡����䡱��
| ���� | CO | H2O | HCOOH |
| Ũ��/mol•L﹣1 | 0.5 | 1.5 | 0.5 |
��2����̼����COת��Ϊ����HCOOH�ķ�ӦΪCO��g��+H2O��g��⇌HCOOH ��g����ij�¶��µ�ƽ�ⳣ��Ϊ1.5�����¶��£��ܱ������м���CO��g����H2O��g����ijʱ�̲�ø���ֵ�Ũ�����ұ���
��Ӧ��ƽ�ⳣ������ʽ��K=�����Ƚϴ�ʱ�����淴Ӧ���ʵĴ�С��v������ v�������������������=����������ƽ��ʱH2O��ƽ��ת����Ϊ������
��3������������������������������Ч��߿����������SO2����Ч�ʣ�����Ҫԭ������NO��2SO2+O2⇌2SO3������ã����û�ѧ����ʽ��ʾ�ù��̣���ʾ���������뷴Ӧ�����������ͻ�ѧ�����ڷ�Ӧǰ��û�иı䣩������������������ƽ��
�ڿ�������������CO��Ϊ��ԭ��������ԭNO��ͬ��������̼��
CO��g��+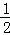 O2��g��=CO2��g����H=﹣283.0kJ•mol﹣1��N2��g��+O2��g��=2NO��g����H=182.6kJ•mol﹣1
O2��g��=CO2��g����H=﹣283.0kJ•mol﹣1��N2��g��+O2��g��=2NO��g����H=182.6kJ•mol﹣1
NO��CO��Ӧ�õ�����Ⱦ������Ȼ�ѧ����ʽΪ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com