
在密闭容器中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
A.A的转化率变小 B.平衡向正反应方向移动
C.D的体积分数变大 D.a > c+d
科目:高中化学 来源:2016-2017学年湖北省高二上学期期中化学试卷(解析版) 题型:选择题
常 温下某溶液中,由水电离出的c(H+)为1×10-12mol/L,该溶液中一定能大量共存的离子组是( )
温下某溶液中,由水电离出的c(H+)为1×10-12mol/L,该溶液中一定能大量共存的离子组是( )
A.K+、Na+、S2-、CO32- B. Na+、K+、SO42-、NO3-
Na+、K+、SO42-、NO3-
C.Fe2+、Mg2+、Cl-、SO42- D.NH4+、Cl-、K+、SO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期第一次月考化学试卷(解析版) 题型:填空题
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示
(1)该气体的物质的量为_____________mol。
(2)该气体所含原子总数为_____________个。
(3)该气体在标准状况下的体积为_____________L。
(4)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期第一次月考化学试卷(解析版) 题型:选择题
要从硝酸钾和食盐(少量)的混合物中,分离出较纯净的硝酸钾,应把它们 ( )
A.溶解、过滤
B.制成热饱和溶液,降温 后再过滤
后再过滤
C.加热、冷却后蒸发
D.溶解、过滤后结晶
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:填空题
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应 来合成甲醇(于固定容器中进行):2H2(g) + CO(g)
来合成甲醇(于固定容器中进行):2H2(g) + CO(g) CH3OH(g)
CH3OH(g)
(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
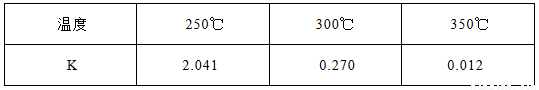
①该反应的熵变△S 0(填:“<,>,=”)。该反应在 (填:高温或低温)条件下能自发进行。
②要提高CO的转化率,可以采取的措施是_____________(填序号)。
a.升温
b.加入催化剂
c.增加CO的浓度
d.加入H2加压
e.加入惰性气体加压
f.分离出甲醇
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A__________C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A___________C,由状态B到状态A,可采用___________的方法(填“升温”或“降温”)。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:选择题
在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小20%。下列说法正确的是( )
A.该温度下此反应的平衡常数K=400
B.其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大
C.平衡时,SO2的转化率为95%
D.前2min SO2的平均反应速率0.02mol/(L·s)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:选择题
下列叙述不正确的是( )
A.原电池是将化学能转化为电能的装置
B.铁船底镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁腐蚀的负极反应:Fe﹣3e﹣═Fe3+
D.把锌片放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上期中化学试卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是
A.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
B.合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
C.反应CO(g)+NO2(g) CO2(g)+NO(g)(正反应为放热反应),达平衡后,升温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应),达平衡后,升温度体系颜色变深
D.对于2HI(g) H2(g)+I2(g),达平衡后,缩小容器体积可使体系频色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系频色变深
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:选择题
25 ℃时某些弱酸的电离平衡常数如下表所示:
CH3COOH | HClO | H2CO3 |
K(CH3COOH) =1.8×10-5 | K(HClO) =3.0×10-8 | K(H2CO3)a1=4.4×10-7 K(H2CO3)a2=4.7×10-11 |
常温下,稀释CH3COOH、HClO两种酸时,溶液的pH随加水量变化的曲线如图所示,下列说法正确的是( )

A.相同浓度的CH3COOH和HClO的混合溶液中,各离子浓度的大小关系是:
c(H+)>c(ClO-)>c(CH3COO-)>c(OH-)
B.图像中a、c两点所处的溶液中 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
C.图像中a点酸的浓度大于b点酸的浓度
D.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com