
 转变为
转变为 的方法为( )
的方法为( )| A. | 与足量NaOH溶液共热后,再通入CO2 | |
| B. | 与稀H2SO4共热后,加入足量Na2CO3 | |
| C. | 与稀H2SO4共热后,加入足量NaOH | |
| D. | 与足量NaOH溶液共热后,再加入稀硫酸 |
 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:选择题
| A. |  检验溶液中是否有K+ | B. |  制取并收集少量NH3 | ||
| C. | 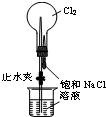 进行喷泉实验 | D. | 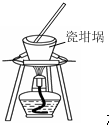 加热熔融NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离出少量氮化硅 | B. | 降低温度 | ||
| C. | 充入氮气 | D. | 充入氦 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 植物油和裂化汽油都能使溴水褪色 | B. | 食用植物油是人体的营养物质 | ||
| C. | 汽油、煤油、卤代烃均为烃 | D. | 甲醛可大量用作食品防腐剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
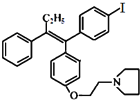 (不考虑立体结构).
(不考虑立体结构).
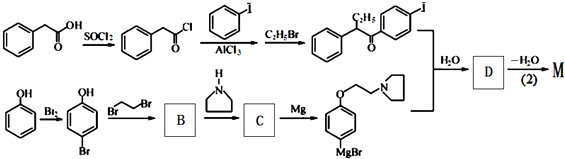


 D
D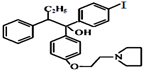
 有多种同分异构体,其中满足①遇FeCl3显色②苯环上的一溴取代物只有一种,符合条件的同分异构体数目有6种.
有多种同分异构体,其中满足①遇FeCl3显色②苯环上的一溴取代物只有一种,符合条件的同分异构体数目有6种. 中任一种.
中任一种. +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +HBr.
+HBr. 及含二个碳原子的有机化合物为原料,制备芳香醇
及含二个碳原子的有机化合物为原料,制备芳香醇 的合成路线
的合成路线 (不超过5步反应).
(不超过5步反应).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
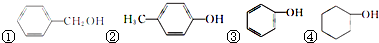 (填序号)
(填序号)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ; Z在周期表中的位置是第三周期ⅥA族;B元素的名称为碳.
; Z在周期表中的位置是第三周期ⅥA族;B元素的名称为碳.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com