
【题目】(1)人造象牙的主要成分的结构简式是![]() ,它是通过加聚反应制得的,则合成人造象牙的单体的结构简式是____________________。
,它是通过加聚反应制得的,则合成人造象牙的单体的结构简式是____________________。
(2)聚丙烯酸甲酯的结构简式可用![]() 表示,则其单体的结构简式是_________。
表示,则其单体的结构简式是_________。
(3)某药物的结构简式为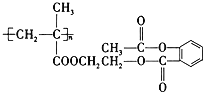 ,1 mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为_______________。
,1 mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为_______________。
【答案】HCHO CH2=CH-COOCH3 4n mol
【解析】
(1)由加聚产物判断单体的方法是:凡链节的主链上只有两个碳原子(或碳和氧)的高聚物,其合成单体必为一种,将链节上的两个原子形成双键即可;
(2)将聚丙烯酸甲酯链节上的两个C原子形成碳碳双键,就得到其单体;
(3)由结构可知,分子中含-COOC-及水解生成的酚-OH均与NaOH反应,以此来解答。
(1)人造象牙的结构简式为![]() ,将C、O单键形成C=O,去掉中括号和n,就得到其单体,单体的结构简式为HCHO,名称是甲醛;
,将C、O单键形成C=O,去掉中括号和n,就得到其单体,单体的结构简式为HCHO,名称是甲醛;
(2)聚丙烯酸甲酯的结构简式可用![]() 表示,去掉中括号和n,将碳碳单键改为碳碳双键,可得其单体,结构简式为CH2=CH-COOCH3,名称为丙烯酸甲酯;
表示,去掉中括号和n,将碳碳单键改为碳碳双键,可得其单体,结构简式为CH2=CH-COOCH3,名称为丙烯酸甲酯;
(3)由物质结构可知,分子中含-COOC-为3n个,碱性条件下水解生成的酚-OH为n个,它们与NaOH均以1:1反应,则1 mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为4n mol。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数,下列说法正确的是
A.用氢氧燃料电池电解饱和食盐水得到 0.4mol NaOH,在燃料电池的负极上消耗氧气分子数为 0.1 NA
B.2 mol H3O+中含有的电子数为 20 NA
C.密闭容器中 1 mol N2(g)与 3 mol H2 (g)反应制备氨气,形成 6 NA 个 N-H 键
D.32 g N2H4中含有的共用电子对数为6 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在金属或非金属底物材料上,用NaBH4进行“化学镀”镀镍,可以得到坚硬、耐腐蚀的保护层(3Ni3B+Ni),反应的离子方程式为:
20Ni2++16BH4-+34OH-+6H2O===2(3 Ni3B+ Ni)+10B(OH)4-+35H2![]()
(1)Ni2+基态核外电子排布式为________。
(2)与BH4-互为等电子体的一种分子为______________![]() 填化学式
填化学式![]() 。
。
(3)B(OH)4-中硼原子轨道的杂化类型是________;1mol B(OH)4-含有σ键的数目为________mol。
(4)Ni的晶胞结构如图所示,镍晶体中每个镍原子周围距离最近的镍原子数目为________。
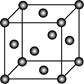
(5)NiCl2![]() 6H2O在SOCl2气流中加热时,生成NiCl2和两种酸性气体。写出该反应的化学方程式:__________________。
6H2O在SOCl2气流中加热时,生成NiCl2和两种酸性气体。写出该反应的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1,2-二氯乙烷在常温下为无色液体,沸点为83.5 ℃,密度为1.23 g·mL-1,难溶于水,易溶于醇、醚、丙酮等有机溶剂;乙醇的沸点为78.5 ℃。某化学课外活动小组为探究1,2-二氯乙烷的消去反应,设计了如图所示的实验装置。请回答下列问题:

(1)为了检查整套装置的气密性,某同学将导气管末端插入盛有水的烧杯中,用双手捂着装置A中大试管,但该方法并不能准确说明装置的气密性是否良好。则正确检查整套装置气密性的方法是_______________。
(2)向装置A中大试管里先加入1,2-二氯乙烷和NaOH的乙醇溶液,再加入______,目的是______,并向装置C中试管里加入适量稀溴水。
(3)为了使反应在75 ℃左右进行,常用的方法是_______________________________。
(4)与装置A中大试管相连接的长玻璃管的作用是______,装置B的作用是______。
(5)能证明1,2-二氯乙烷已发生消去反应的实验现象是______,装置A、C中发生反应的化学方程式分别为_________________________;________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有烃的衍生物A,还原A时形成醇B,氧化A时形成酸C。B、C反应可生成高分子化合物![]() ,下列叙述错误的是( )
,下列叙述错误的是( )
A.A属于醛类,其相对分子质量为58,1 mol A与足量的银氨溶液反应可生成4 mol Ag
B.B在一定条件下可通过缩聚反应得到新的高聚物
C.高分子化合物![]() 的组成与B、C等物质的量的混合物的组成相同
的组成与B、C等物质的量的混合物的组成相同
D.B、C生成该高聚物的反应为缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某中草药提取的有机物结构如图所示,该有机物的下列说法中错误的是( )
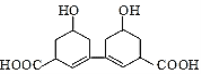
A.分子式为C14H18O6
B.1mol该有机物最多可与2mol的H2发生加成反应
C.既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应
D.1mol该有机物最多可反应2mol氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几种物质:
①![]() ②
②![]() ③
③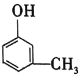 ④
④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧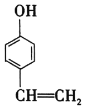 ⑨
⑨![]()
请回答下列问题。
(1)属于醇的是__(填序号,下同)。
(2)属于酚的是__。
(3)互为同分异构体的是__。
(4)互为同系物的是___。
(5)与Br2按物质的量之比为1:3反应的是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钙钛矿(主要成分是CaTiO3)太阳能薄膜电池制备工艺简单、成本低、效率高,引起了科研工作者的广泛关注,科学家认为钙钛矿太阳能电池将取代硅基太阳能电池的统治地位。
(1)基态Ti原子的价电子排布式为__,能量最高的能级有__个空轨道;Si、P、S第一电离能由小到大顺序是__。
(2)碳和硅的有关化学键键能如表所示:
化学键 | CC | CH | CO | SiSi | SiH | SiO |
键能/kJmol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___。
(3)一种新型熔融盐燃料电池以Li2CO3和Na2CO3的熔融盐混合物作电解质,则CO32-的空间构型为___。
(4)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:
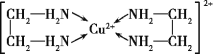
该配离子中含有的化学键类型有__(填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有__个σ键,C原子的杂化方式为__。
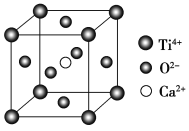
(5)CaTiO3的晶胞为立方晶胞,结构如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角)Ca2+的配位数为__,与Ti4+距离最近且相等的O2-有__个;晶体的密度为ρg/cm3,最近的Ti4+和O2-之间的距离为__nm(填计算式)。(CaTiO3的摩尔质量为136g/mol,NA为阿伏加德罗常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子晶体是由原子直接通过共价键形成的空间网状结构的晶体,又称共价晶体,因其具有高熔沸点、硬度大、耐磨等优良特性而具有广泛的用途。
(1)晶体硅是良好的半导体材料,被广泛用于信息技术和能源科学等领域。晶体硅是与金刚石结构类似的晶体(其晶胞如图乙所示),硅晶体的1个晶胞中含_____个Si原子,在晶体硅的空间网状结构中最小环为_____元环,每最小环独立含有__________个Si原子,含1molSi原子的晶体硅中Si-Si键的数目为_____。
(2)金刚砂(SiC)也与金刚石具有相似的晶体结构(如图丙所示),在金刚砂的空间网状结构中,碳原子、硅原子交替以共价单键相结合。试回答下列问题:
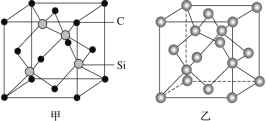
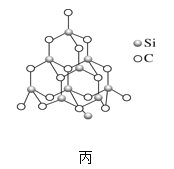
①金刚砂、金刚石、晶体硅的熔点由低到高的顺序是_____(均用化学式表示)。
②在金刚砂的结构中,一个碳原子周围结合了_____硅个原子,其键角是_____。
③金刚砂的结构中含有C、Si原子以共价键结合形成的环,其中一个最小的环上独立含有_个C-Si键
④金刚砂的晶胞结构如图甲所示,在SiC中,每个C原子周围最近等距的C原子数目为_____;若金刚砂的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶体中最近的两个碳硅原子之间的距离为_________pm(用代数式表示即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com