
| A、氯气 | B、铜 | C、氢氧化钠 | D、铁 |
科目:高中化学 来源: 题型:
| A、一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通道 |
| B、明矾可以用来净水 |
| C、胶态金属氧化物分散于玻璃中制成有色玻璃 |
| D、三氯化铁溶液中加入NaOH溶液出现红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
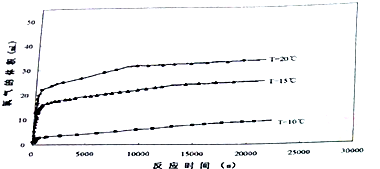 新型绿色硝化剂N205较传统硝化剂具有反应热效应小、温度容易控制、产物分离简单等优点,因而得到广泛的应用.
新型绿色硝化剂N205较传统硝化剂具有反应热效应小、温度容易控制、产物分离简单等优点,因而得到广泛的应用.| t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol.L-1 | 4.00 | 3.52 | 2.00 | 2.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制二氧化氮时,用水或NaOH溶液吸收尾气 |
| B、制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
| C、制乙烯时,用排水法或向上排空气法收集气体 |
| D、制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:
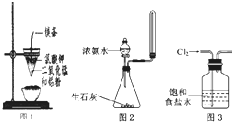
| A、图1装置可制得金属锰,用同样的装置可制得金属铬 |
| B、实验室用图2所示装置制取少量纯净的氨气 |
| C、用玻璃棒蘸取某溶液做焰色反应实验,火焰呈黄色不能说明该溶液中含有钠元素 |
| D、实验室用图3所示装置除去Cl2中的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCN | HF | CH3COOH | HNO2 |
| 电离常数 | 6.2×10-10 | 6.8×10-4 | 1.8×10-5 | 6.4×10-4 |
| A、HCN>HNO2>CH3COOH>HF |
| B、HF>HNO2>CH3COOH>HCN |
| C、HCN>CH3COOH>HNO2>HF |
| D、HCN>CH3COOH>HF>HNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该混盐在酸性溶液中产生1 molCl2时转移的电子数为2NA |
| B、该混盐的水溶液显碱性 |
| C、该混盐中氯元素的化合价为-1价 |
| D、该混盐具有较强的还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com