
����Ŀ���⻯����ҽ�Ƽ�ʳƷ��������Ҫ�����á�ʵ������NaOH�����ʵ��ˮ����(N2H4��H2O)Ϊԭ���Ʊ��⻯�ơ���֪��ˮ���¾��л�ԭ�ԡ��ش��������⣺
(1)ˮ���µ��Ʊ���Ӧԭ��Ϊ��CO(NH2)2(����)+NaClO+2NaOH= N2H4��H2O +NaCl+Na2CO3
����ȡ�������ƺ��������ƻ��Һ������˳��Ϊ__________(������������Сд��ĸ��ʾ)������ʵ���¶ȿ��Ʋ�������Ӧ��������ƿ��ClO-��ClO3-�����ʵ���֮��Ϊ5��1�����������������Ʒ�Ӧʱ������ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��Ϊ____��
���Ʊ�ˮ����ʱ��Ӧ��__________�ε�__________�У�����NaClO��Һ������������Һ�������ҵμ��ٶȲ��ܹ��졣
�����صĵ���ʽΪ__________________
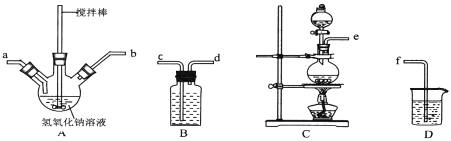
(2)�⻯�Ƶ��Ʊ�������ˮ���»�ԭ����ȡ�⻯�ƹ��壬���Ʊ�������ͼ��ʾ��
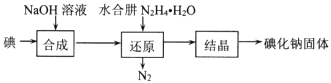
������ԭ�������У���Ҫ���ķ�Ӧ���������ɵĸ�����IO3-���ù��̵����ӷ���ʽΪ ___��
(3)�ⶨ��Ʒ��NaI������ʵ�鲽�����£�
a����ȡ10.00 g��Ʒ���ܽ⣬��500 mL����ƿ�ж��ݣ�
b����ȡ25.00 mL����Һ����ƿ�У�Ȼ�����������FeCl3��Һ����ַ�Ӧ���ټ���M��Һ��ָʾ����
c. ��0.2000 mol��L1�� Na2S2O3�� �� Һ �� �� �� �� ��(�� Ӧ �� �� ʽ2Na2S2O3+I2=Na2S4O6+2NaI)���ظ�ʵ���Σ�������ı���Һ�����Ϊ15.00 mL��
��MΪ____________(д����)��
�ڸ���Ʒ��NaI����������Ϊ_______________��
���𰸡�ecdabf 5��3 NaClO��Һ ������Һ 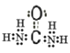 2IO3-+3N2H4��H2O=3N2��+2I-+9H2O ���� 90%
2IO3-+3N2H4��H2O=3N2��+2I-+9H2O ���� 90%
��������
(1)�ٸ����Ʊ����������ӣ��Ʊ��������ƺ��������ƣ�����β������������ƿ��ClO-��ClO3-�����ʵ���֮��Ϊ5��1����ClO-��ClO3-�����ʵ����ֱ�Ϊ5 mol��1 mol�����ݵ�ʧ�����غ㣬����5 molClO- �������Cl-5 mol������1 molClO3-�������Cl-5 mol���ݴ˷����ɵã�
��NaClO����ˮ���£�
��������Cԭ����Oԭ���γɹ���˫������2��-NH2��Nԭ���γɹ��۵�����
(2)���NaOH��Ӧ����NaI��NaIO��������IO3-������ˮ���»�ԭNaIO��������IO3-���õ������Ӻ͵������ᾧ�õ��⻯�ƣ��������̿�֪��������IO3-��ˮ�������ɵ����Ӻ͵������ݴ���д��
(3)�ٵⵥ�ʲ��룬�õ�����Һ��ָʾ����
�ڸ��ݵ�Ԫ���غ㣬2I-��I2��2Na2S2O3����n(NaI)=n(Na2S2O3)��������Ʒ��NaI���������������䴿�ȡ�
(1)��װ��C�ö������̺�Ũ�����ϼ����Ʊ���������Bװ�õı���ʳ��ˮ��ȥ����HCl���壬Ϊ��֤���ӳ�֣������ܳ����̳���������NaOH��A�з�Ӧ�Ʊ��������ƣ�Ϊʹ��Ӧ���ַ�Ӧ��Ҫʹ������a��ȥ����Dװ������δ��Ӧ���������Է�ֹ��Ⱦ�������ʵ���������˳��Ϊ��ecdabf������ƿ��ClO-��ClO3-�����ʵ���֮��Ϊ5��1����ClO-��ClO3-�����ʵ���֮��Ϊ5��1�����ʵ����ֱ�Ϊ5 mol��1 mol�����ݵ�ʧ�����غ㣬����6 molClO-�������Cl-�����ʵ���Ϊ5 mol������1mol ClO3-�������Cl- 5 mol����ԭ����Ԫ��Ϊ���ϼ۽��͵���Ԫ�أ���ΪCl-��n(Cl-)=5 mol+5 mol=10mol������������Ԫ��Ϊ���ϼ����ߵ���Ԫ�أ������ʵ���ΪClO-��ClO3-���ʵ����ĺͣ���5 mol+1 mol=6mol���ʱ���ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��Ϊ10��6=5��3��
���Ʊ�ˮ����ʱ�������صε�NaClO��Һ�л����μӣ�����ʹ������NaClO��Һ����ˮ���£����Ͳ��ʣ���ʵ�����Ʊ�ˮ���µIJ����ǣ�ȡ����A�еĻ��Һ��μ��뵽������������Һ���Ʊ�ˮ���£��μ�˳���ܵߵ����ҵμ��ٶȲ��ܹ��죻
������CO(NH2)2��Cԭ����Oԭ���γɹ���˫������2����NH2��Nԭ���γɹ��۵��������������ʽΪ��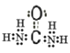 ��
��
(2)�������̿�֪��������IO3-��ˮ�������ɵ����Ӻ͵�������Ӧ�����ӷ���ʽΪ��2IO3-+3N2H4H2O=3N2��+2I-+9H2O��
(3)��ʵ���еζ��ⵥ�ʣ�Ӧ���õ�����ָʾ��������M�ǵ��ۣ�
�ڸ��ݵ�Ԫ���غ㣬2I-��I2��2Na2S2O3����n(NaI)=n(Na2S2O3)������Ʒ��NaI������m(NaI)=![]() ��150 g/mol=9.00 g������Ʒ��NaI����������Ϊ
��150 g/mol=9.00 g������Ʒ��NaI����������Ϊ![]() ��100%=90.0%��
��100%=90.0%��


 �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�д��ڵ���ƽ��CH3COOH![]() H++CH3COO-��������������ȷ����
H++CH3COO-��������������ȷ����
A. �����¶ȣ�ƽ�������ƶ�������ĵ��볣��Kaֵ����
B. 0.l0mol/L��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c(OH-)����
C. CH3COOH��Һ�м�������CH3COONa���壬ƽ�������ƶ�
D. �����£���ʹ0.1mol/L������Һ��pH�������a����С���ɼ�������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС����˽̰�̲�ʵ�顰��200mL�ձ��з���20g���ǣ�C12H22O11������������ˮ��������ȣ�Ȼ���ټ���15mL��������Ϊ98%Ũ���ᣬѸ�ٽ��衱��������̽����
��1���۲����������ȱ�ƣ�����ڣ�������ͣ��γ����ɶ�ĺ���״��ɫ���ʣ�ͬʱ�ŵ��̼�����ζ����ѹ�˺�ɫ����ʱ���о���Ӳ������ˮ�г�Ư��״̬��ͬѧ�������������Ʋ�����н��ۣ�
��Ũ�������ǿ������ ��Ũ���������ˮ�� ��Ũ���������ˮ�Ԣ�Ũ����������� �ݺ�ɫ���ʾ���ǿ������
�������ݲ���ֵ���_________������ţ���
��2��Ϊ����֤������Ũ���ᷴӦ���ɵ���̬���ͬѧ�����������װ�ã�

�Իش��������⣺
��ͼ1��A�����ѡ������װ��_________�����ţ���
��ͼ1�� Bװ����װ�Լ���_________��Dװ�����Լ���������_________��Eװ���з�����������_________��
��ͼ1��Aװ����ʹ�����ȱ�ڵĻ�ѧ��Ӧ����ʽΪ_________����������͵Ļ�ѧ����ʽΪ��_________��
��ijѧ����ͼ2����ʵ��ʱ������DƿƷ�첻��ɫ��Eװ�����������ݳ���Fװ�������Ը��������Һ��ɫ��dz���Ʋ�Fװ�������Ը��������Һ��ɫ��dz��ԭ��_________���䷴Ӧ�����ӷ���ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ���ó�����Ӧ������ȷ����
ʵ����ʵ | ���� | |
A | ����ͬ�¶��£���1 mL0.2 mol/LNaOH��Һ�е���2��0.1 mol/LMgCl2��Һ��������ɫ�������ٵμ�2��0.1 mol/LFeCl3��Һ�������ɺ��ɫ���� | �ܽ�ȣ�Mg(OH)2>Fe(OH)3 |
B | ij������ʹʪ�����ɫʯ����ֽ��� | ������ˮ��Һһ���Լ��� |
C | ͬ��ͬѹ�£������pH=3��HA��HB������ֱ���������п��Ӧ����ˮ���ռ����壬HA�ų����������ҷ�Ӧ���ʿ� | HB�����Ա�HAǿ |
D | SiO2����������ᷴӦ������Ӧ | SiO2������������ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I���ݱ������ҹ����Ϻ��������������еĿ�ȼ��(�����ˮ����)�Բɻ�óɹ���������һ����Ҫ�Ļ���ԭ�ϡ�
(1)��������������������ʵ���Ҫ��ʽ����������������������֣�
ˮ����������CH4(g)+H2O(g)![]() CO(g)+3H2(g) ��H1=+205.9 kJ/mol ��
CO(g)+3H2(g) ��H1=+205.9 kJ/mol ��
CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H2=-41.2 kJ/mol ��
CO2(g)+H2(g) ��H2=-41.2 kJ/mol ��
������̼������CH4(g)+CO2(g)![]() CO(g)+2H2(g) ��H3 ��
CO(g)+2H2(g) ��H3 ��
��Ӧ���Է����е�������______________ ��H3=________ kJ/mol��
���Ļ������Լ����Ĺ̶�һֱ�ǿ�ѧ���о�����Ҫ���⣬�ϳɰ������˹��̵��Ƚϳ���ļ�������ԭ��ΪN2(g)+3H2(g)![]() 2NH3(g)��
2NH3(g)��
(2)�ڲ�ͬ�¶ȡ�ѹǿ����ͬ���������£���ʼN2��H2�ֱ�Ϊ0.1 mol��0.3 molʱ��ƽ��������а����������(��)��ͼ��ʾ��

�����У�p1��p2��p3�ɴ�С��˳����____________���÷�Ӧ��H_______0(����>����<������=��)��
�����ֱ��� vA(N2)�� vB(N2)��ʾ�ӷ�Ӧ��ʼ����ƽ��״̬ A��B ʱ�Ļ�ѧ��Ӧ���ʣ���vA(N2)________vB(N2)(����>����<������=��)��
������250�桢p1Ϊ10 5Pa�����£���Ӧ�ﵽƽ��ʱ���������Ϊ1 L�����������B��N2�ķ�ѹp(N2)Ϊ_______Pa (��ѹ=��ѹ�����ʵ�������������һλС��)��
(3)��NO2��O2������NaNO3��ɵ�ȼ�ϵ��װ������ͼ��ʾ��ʯī��ĵ缫����Ϊ _______����ʹ�ù�����ʯī��缫��Ӧ����һ��������Y��ʯī��缫��Ӧ�ɱ�ʾΪ______________________��
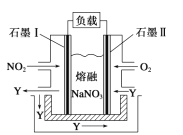
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���Һϳ����������IJ������£���ͼ��Բ����ƿ�ڼ����Ҵ���Ũ��������ᣬ���Ȼ���һ��ʱ�䣬Ȼ��ͼ��װ�ý������õ������Ҵ��������ˮ�����������ֲ�Ʒ��
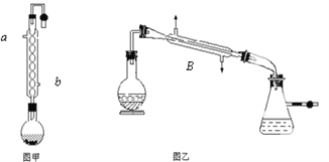
��ش���������
��1��ͼ��������ˮ��______��a��b������ͼ����Bװ�õ�����Ϊ_______��
��2��ͼ������ƿ�г��˼����Ҵ���Ũ����������⣬��Ӧ�����ʯ��Ŀ����_______��
��3����Ӧ�м���������Ҵ���Ŀ����_______��
��4���������ֲ�Ʒ����������������Ҵ��Ļ�������п�ͼ�Ƿ��������������ͼ��
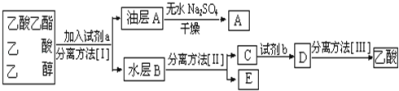
���Լ�a��______�����뷽��I��_______�����뷽��II��_______������E��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��� ��˵��������ȷ����
��˵��������ȷ����
A.�ڳ��³�ѹ�£�1mol �������������� NaOH ��Һ��Ӧ��������� 1mol NaOH
B.��������һ�������¿��Է����Ӿ۷�Ӧ
C.�л���ķ���ʽΪ C13H12O4Cl2
D.һ�������£�1mol ������������� 5mol �����ӳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������нϹ㷺�Ŀ������ã���ṹ��ʽ����ͼ��ʾ��

���ڿ������������������ȷ����(����)
A������ʽΪC16H13O9
B��1 mol����������뺬8 mol NaOH����Һ��Ӧ
C����ʹ����KMnO4��Һ��ɫ��˵�����ӽṹ�к���̼̼˫��
D����Ũ��ˮ�ܷ����������͵ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ����ñ���ͪ��ӵ��������ϳɱ����ᣬԭ����ͼ��ʾ������˵����ȷ���ǣ� ��
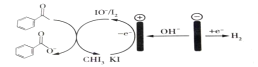
A.���װ���ǽ���ѧ��ת��Ϊ����
B.������Ӧ��2H++2e�TH2��
C.����I-ʧȥ���Ӻ�IJ�����OH-��Ӧ�����ӷ���ʽΪI2+2OH-=I-+IO-+H2O
D.��װ����Ҫ������������Һ������KI��Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com