
25℃时,用0.0500 mol·L-1H2C2O4(二元弱酸)溶液滴定 25.00 mL 0.100 0 mol • L-1NaOH溶液所得滴定曲线如右图。下列说法正确的是( )
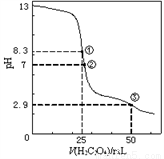
A. 点①所示溶液中:c(H+)+c(H2C2O4)+ c(HC2O4-)=c(OH-)
B. 点②所示溶液中:c(HC2O4-)+c(C2O42-)=c(Na+)
C. 点③所示溶液中:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D. 滴定过程中可能出现:c(Na+) > c(C2O42-) =c(HC2O4-)>C(H+)>c(OH-)
科目:高中化学 来源:2016-2017学年湖南师范大学附属中学高一下学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列物质中,既含离子键又含共价键的是
A. Na2O B. NH3·H2O C. NaOH D. CaBr2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省北校高一3月月考化学试卷(解析版) 题型:推断题
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E三种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出元素的名称:C__________,D___________。
(2)写出元素的原子结构示意图:A______________,B______________,二者离子半径:_______>_________ (填化学式,下同)。
(3)A、B的最高价氧化物的水化物的碱性:______________>______________。
(4)D、E的气态氢化物的稳定性:______________>______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省北校高一3月月考化学试卷(解析版) 题型:选择题
关于元素周期表的叙述中不正确的是( )
A. 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素
B. 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素
C. 在元素周期表的右上角可以寻找制备新型农药的元素
D. 在地球上元素的分布和它们在元素周期表中的位置有密切关系
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(二)化学试卷(解析版) 题型:实验题
三氯化铁是合成草酸铁的重要原料。
(1)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:
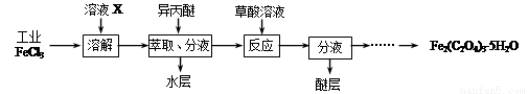
①为抑制FeCl3水解,溶液X为 。
②上述流程中FeCl3能被异丙醚萃取,其原因是 ;检验萃取、分液后所得水层中是否含有Fe3+的方法是 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是 。
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于如图所示仪器 (填“甲”或“乙”)中。下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是 。

a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
(2)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3,再由FeCl3合成Fe2(C2O4)3·5H2O。请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤;__________;___________;调节溶液pH,将溶液蒸发浓缩、冷却结晶、过滤、洗涤干燥得FeCl3·6H2O; ___________,得到无水FeCl3。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(二)化学试卷(解析版) 题型:选择题
给定条件下,下列选项中所示的物质间转化均能通过一步反应实现的是( )
A. 0.1 mol • L-1 HC1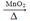 C12
C12  Ca(ClO)2(aq) B. Al3+
Ca(ClO)2(aq) B. Al3+ A1O2-
A1O2-  Al(OH)3
Al(OH)3
C. A1 NaA1O2(aq)
NaA1O2(aq)  NaAlO2(s) D. MgO(s)
NaAlO2(s) D. MgO(s)  Mg(NO3)2(aq)
Mg(NO3)2(aq)  Mg(s)
Mg(s)
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(二)化学试卷(解析版) 题型:选择题
下列有关钠元素及其化合物的表示正确的是( )
A. 钠原子的结构示意图: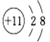
B. 过氧化钠的电子式: 
C. 小苏打在水中的电离方程式:NaHCO3=Na++HCO3-
D. 硫化钠的水溶液呈碱性的原因:S2-+2H2O H2S+2OH-
H2S+2OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省淮北市高二下学期第一次月考化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是
元素符号 | X | Y | Z | M | R | Q | |
原子半径(1×10-10m) | 0.37 | 1.86 | 1.43 | 0.99 | 0.75 | 0.74 | |
主要化合价 | 最高正价 | +1 | +1 | +3 | +7 | +5 | — |
最低负价 | -1 | — | — | -1 | -3 | -2 | |
A. 离子半径:Y>Z>M
B. Y、Z、M兰种元素的最高价氧化物的水化物两两之间会反应
C. 化合物XM、YM都是电解质,熔融状态下都能导电
D. 元素Z、M、R的离子均能破坏水的电离平衡
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一下学期第一次月考化学试卷(解析版) 题型:选择题
依据元素周期表及元素周期律,下列推断正确的是( )
A. Mg(OH)2的碱性比Be(OH)2的弱 B. H3BO3的酸性比H2CO3的弱 
C. HCl、HBr、HI的热稳定性依 次增强 D. 若M+和R2﹣的核外电子层结构相同,则原子序数:R>M
次增强 D. 若M+和R2﹣的核外电子层结构相同,则原子序数:R>M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com