
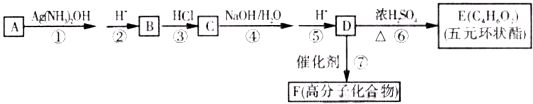
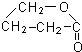 ,D发生缩聚反应生成高分子化合物F,据此解答.
,D发生缩聚反应生成高分子化合物F,据此解答.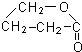 ,
,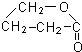 ,反应方程式为:
,反应方程式为:| 浓硫酸 |
| △ |
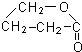 +2H2O,
+2H2O,| 浓硫酸 |
| △ |
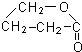 +2H2O;
+2H2O;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
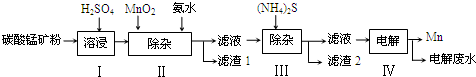
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
查看答案和解析>>
科目:高中化学 来源: 题型:
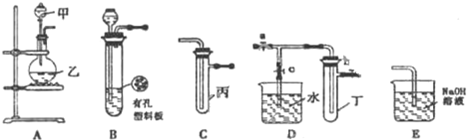
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同一支钢笔使用不同品牌墨水时,容易发生堵塞现象 |
| B、江河入海口,容易形成沙洲 |
| C、医学上治疗肾衰竭等疾病时,血液的净化手段利用血液透析 |
| D、向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在豆浆中加入盐卤点豆腐 |
| B、河流入海处易形成三角洲 |
| C、一束平行光线照射蛋白质溶液时,从侧面可以看到光亮的通路 |
| D、氯化铁溶液中滴入NaOH溶液出现红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com